高效光致电子转移光敏蛋白质的理性设计方面获进展
来源:生物物理所 2021-06-18 12:50
CCS Chemistry发表了中国科学院生物物理研究所研究员王江云课题组、中科院化学研究所研究员夏安东课题组和植物研究所研究员于龙江课题组题为Ultrafast photo-induced electron transfer in a photosensitizer protein的研究文章。研究设计报告了可以基因编码的27 kDa
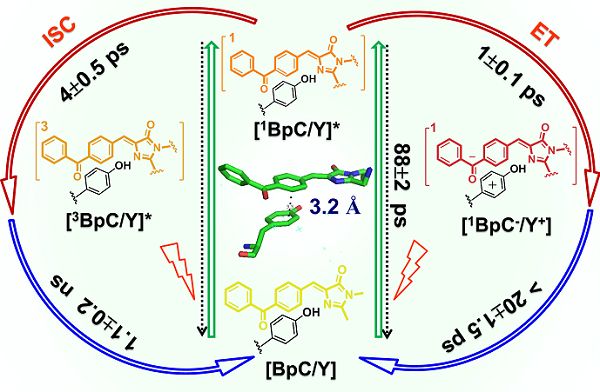
CCS Chemistry发表了中国科学院生物物理研究所研究员王江云课题组、中科院化学研究所研究员夏安东课题组和植物研究所研究员于龙江课题组题为Ultrafast photo-induced electron transfer in a photosensitizer protein的研究文章。研究设计报告了可以基因编码的27 kDa光敏蛋白质(PSP3),具有PSII系统原初光诱导电子转移等关键特性。通过将二苯甲酮丙氨酸(BpA)基因掺入PSP蛋白质和飞秒瞬态吸收光谱测量,发现从残基Tyr203到PSP3生色团发生了高效快速光诱导电子转移(~1皮秒)过程。光驱动实现了强还原性物种BpC-(E0 = -1.47 V vs SHE)和强氧化性酪氨酸物种Y+(E0 ~ 1.34 V vs SHE)的生成。
在藻类和植物中,光系统I(PSI)和光系统II(PSII)协同工作,将水氧化成O2,并将NAD(P)+还原成NAD(P)H,最后用于CO2还原生成细胞生长需要的碳基能量物质。科学家致力于提高光合作用效率和创造人工光合作用系统,以推动具有挑战性的化学转化。然而,由于光系统是含有多种辅因子的大型膜蛋白复合物,通过基因工程直接增强光系统的功能仍然困难。王江云课题组前期研究发现,通过使用基因密码子扩展技术可以将非天然氨基酸插入荧光蛋白(PSP),从而改造发色团光驱动生成具有高还原活性的物种(PSP2·,E0=-1.47 V)。进一步在蛋白表面特定位置引入小分子镍配合物或者融合含有铁硫簇的小蛋白,可以驱动二氧化碳光还原(Nat. Chem., 2018;Acc. Chem. Res.,2019;ACS Catal., 2021)、光能驱动卤代芳烃羟化脱卤反应(JACS., 2021)等,PSP蛋白在上述工作中表现出优异的光化学性质。
基于上述研究,该论文报道了一种新型光敏剂蛋白(PSP3)的合理设计和光致电子转移途径的综合表征。PSP3囊括了PSII中原初的光诱导电子转移相关关键特性,包括:可见光吸收,405 nm;超快光诱导电子转移(PET,~1皮秒),与PSII中的原初PET速度相当;在吸收光后产生了强还原性物种BpC-(E0 = -1.47 V vs SHE)和强氧化性酪氨酸物种Y+(E0 ~ 1.34 V vs SHE)。由于PSP3较容易在大肠杆菌中高产量的过表达,通过进一步有效的定向进化,其可能有助于发展具有体内外挑战性的氧化和还原反应。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


