Abivax口服抗炎药治疗溃疡性结肠炎IIa期试验成功
来源:新浪医药新闻 2020-09-05 12:10
Abivax是一家临床阶段的生物技术公司,致力于开发可刺激人体自然免疫机制的创新疗法来治疗炎症性疾病、病毒性疾病和癌症。近日,该公司公布了ABX464治疗溃疡性结肠炎(UC)IIa期研究的2年维持治疗数据。该研究入组的患者,先前对至少一种现有疗法不耐受和/或难治。2年维持治疗结果显示,69%的患者获得临床缓解、94%的患者受益于临床应答。这些数据
Abivax是一家临床阶段的生物技术公司,致力于开发可刺激人体自然免疫机制的创新疗法来治疗炎症性疾病、病毒性疾病和癌症。近日,该公司公布了ABX464治疗溃疡性结肠炎(UC)IIa期研究的2年维持治疗数据。该研究入组的患者,先前对至少一种现有疗法不耐受和/或难治。2年维持治疗结果显示,69%的患者获得临床缓解、94%的患者受益于临床应答。
这些数据证实了ABX464在维持期治疗第二年具有良好的安全性和疗效,这在该研究的诱导期以及维持期治疗第一年已经观察到。最新发现加强了ABX464作为一种耐受性良好、有效、每日一次口服疗法治疗中重度UC患者的潜力。
在最初诱导期被纳入活性药物组或安慰剂组的32例患者中,有22例被纳入IIa期维持期研究,接受每日一次50mg剂量ABX464开放标签治疗。其中,19例完成了第一年(52周)ABX464维持治疗;这19例患者中,16例完成了第二年ABX464维持治疗。
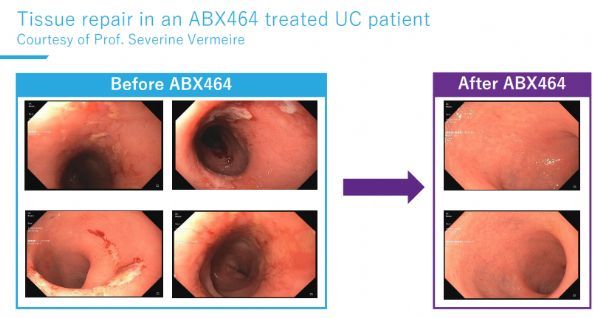
所有内窥镜结果读出由独立审查员集中进行。数据显示,完成第二年维持治疗的16例患者中,有11例(69%)处于临床缓解、15例(94%)受益于临床应答。7例(44%)处于内镜缓解(包括结肠/直肠病变完全消失[内镜梅奥评分=0])。UC疾病活动的关键生物标志物粪便钙卫蛋白(calprotectin)在第一年治疗期间正常化,在第二年期间维持在31.6μg/g(正常水平是低于50μg/g)。研究中,ABX464安全、耐受性好,无严重不良反应报告。在ABX464治疗的第二年,没有患者因不良事件而过早停药。
UC是一种炎症性肠病,会极大地影响患者的生活质量,需要昂贵而繁琐的治疗。上述IIa期研究维持期2年治疗结果证实,ABX464的创新机制将为接受现有疗法(包括生物制剂)无反应或停止反应的中重度UC患者带来很有前途的新方法,提供一种简单易行、每日一次口服、长期有效的治疗选择。
ABX464是从Abivax公司化合物文库中筛选出来的一个小分子药物,该文库包括超过2200个可调节RNA剪接的小分子。ABX464的RNA剪接调节作用所产生的效应构成了一种强大的抗炎作用和抗病毒作用,并有减少HIV病毒库(HIV reservoir)的能力。目前,ABX464正开发用于多种炎症性疾病(包括UC、克罗恩病、类风湿性关节炎)和多种病毒性疾病(COVID-19、HIV)。
ABX464的抗炎作用是由该分子结合至靶点帽子结合复合物(CBC)所触发的,CBC位于每个胞内非编码RNA分子的5'端。这种结合可导致一种长的、非编码RNA的剪接,从而诱导单个微小RNA(miRNA)产物miR-124的过度表达。miR-124随后启动一种级联反应,产生强大的抗炎作用。
临床开发方面,ABX464治疗中重度UC患者的IIb期诱导和维持研究正在欧洲、加拿大、美国进行,到目前为止,已经有69%(159/232)的患者随机进入诱导研究。该研究的患者入组预计今年底完成,首批顶线结果将在2021年第二季度公布。在完成诱导期的85例患者中,84例进入维持期,目前正在接受每日一次口服50mg剂量ABX464治疗,并显示出与先前研究一致的良好安全性。
此外,ABX464治疗类风湿性关节炎IIa期研究的患者入组进展顺利,预计年底前完成患者入组。
同时,ABX464治疗新型冠状病毒肺炎(COVID-19)患者的IIb/III期试验已经在所有参与的欧洲国家和巴西获得批准,正在进行患者招募,预计第四季度完成。根据关键领袖的建议,Abivax公司正计划将ABX464推进至克罗恩病关键IIb/III期试验,预计2021年开始招募患者。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。