新型冠状病毒2019-nCoV/COVID-19研究进展(第8期)
来源:本站原创 2020-06-12 22:03
2020年6月15日讯/生物谷BIOON/---自2019年12月8日以来,中国湖北省武汉市报告了几例病因不明的肺炎。大多数患者在当地的华南海鲜批发市场工作或附近居住。在这种肺炎的早期阶段,严重的急性呼吸道感染症状出现了,一些患者迅速发展为急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)、急性呼吸衰竭和
2020年6月15日讯/生物谷BIOON/---自2019年12月8日以来,中国湖北省武汉市报告了几例病因不明的肺炎。大多数患者在当地的华南海鲜批发市场工作或附近居住。在这种肺炎的早期阶段,严重的急性呼吸道感染症状出现了,一些患者迅速发展为急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)、急性呼吸衰竭和其他的严重并发症。2020年1月7日,中国疾病预防控制中心(China CDC)从患者的咽拭子样本中鉴定出一种新型冠状病毒,最初被世界卫生组织(WHO)命名为2019-nCoV。大多数2019-nCoV肺炎患者的症状较轻,预后良好。到目前为止,一些患者已经出现严重的肺炎,肺水肿,ARDS或多器官功能衰竭和死亡。
2020年2月11日,世卫组织将这种疾病病重命名为2019年冠状病毒病(COVID-19)。同一天,负责分类和命名病毒的的国际病毒分类学委员会的冠状病毒研究小组在bioRxiv上发表了一篇文章,指出该研究小组已经决定,新型冠状病毒2019-nCoV是导致2002-2003年爆发严重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)的变种。因此,将这种新病原体重新命名为严重急性呼吸综合征冠状病毒2号(severe acute respiratory syndrome coronavirus 2),或SARS-CoV-2。值得注意的一点是,尽管国际病毒分类委员会冠状病毒研究小组将病毒命名为SARS-CoV-2,但该研究小组主席John Ziebuhr认为这个名字(SARS-CoV-2)和SARS(严重急性呼吸综合征,也称非典型肺炎)没有关联。不过,这种病毒的重新命名引起了不少争议。据《科学》网站报道,世界卫生组织不满意SARS-CoV-2这个名字,而且不打算采用此名称。
冠状病毒可引起多种动物的多系统感染。在此之前已有6种冠状病毒可以感染人类,它们主要引起人类的呼吸道感染:两种高度致命性的冠状病毒,即严重急性呼吸道综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV);4种可导致温和的上呼吸道疾病的冠状病毒,即HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1。
基于此次疫情给中国和全世界带来严重的危害,小编针对近期2019-nCoV/COVID-19研究取得的进展进行一番梳理,以飨读者。
1.bioRxiv:揭示SARS-CoV-2在人细胞和雪貂中引起了减弱的抗病毒反应
doi:10.1101/2020.03.24.004655
根据2020年3月24日发表在预印本服务器bioRxiv上的一项未经过同行评审的研究,导致COVID-19疫情爆发的新型冠状病毒SARS-CoV-2似乎在人细胞和雪貂中引起了减弱的抗病毒反应。这项研究的作者提出宿主对这种冠状病毒的独特转录反应可能是这种冠状病毒高病死率的原因。相关研究的论文标题为“SARS-CoV-2 launches a unique transcriptional signature from in vitro, ex vivo, and in vivo systems”。

美国西奈山伊坎医学院微生物学家Benjamin tenOever和他的研究团队在SARS-CoV-2出现时就已经在研究呼吸道病毒了,因此他们将早期的研究工作纳入到他们正在进行的研究中。为了比较这种冠状病毒和季节性呼吸道病毒,他们让甲型流感病毒(IAV)、呼吸道合胞病毒(RSV)或SARS-CoV-2感染肺癌细胞系,并对来自受感染细胞的RNA进行测序。他们发现正如IAV和RSV一样,SARS-CoV-2能够在这些细胞中复制,而且它表现出的转录反应在强度上与IAV相类似,但强度不如RSV。
当研究哪些基因会因病毒感染而上调时,他们发现SARS-CoV-2刺激了一组宿主基因的表达,而且相比于IAV,这种冠状病毒激活的转录程序与RSV更为相似。但是SARS-CoV-2似乎没有诱导RSV和IAV都能诱导的两个重要的抗病毒基因---编码I型和III型干扰素的基因---的表达,它们是通过发出战斗号角提醒邻近细胞存在病毒入侵者的抗病毒程序的一部分。这种冠状病毒确实增强了两种独特的细胞因子的表达,它们是先前已经证实与肺部炎症有关的分泌因子。
2.AJR:CT评分新标准可定量、准确地评估COVID-19肺炎进展
doi:10.2214/AJR.20.23078
新型冠状病毒SARS-CoV-2(之前称为2019-nCoV)导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。在一项新的研究中,来自中国芜湖市第二人民医院、山东大学、芜湖市第三人民医院和安徽医科大学第一附属医院等研究机构的研究人员报道,经更新后考虑肺叶受累和CT表现变化的CT评分新标准,可以定量、准确地评估COVID-19肺炎的进展。相关研究结果发表在American Journal of Roentgenology期刊上,论文标题为“Timely Diagnosis and Treatment Shortens the Time to Resolution of Coronavirus Disease (COVID-19) Pneumonia and Lowers the Highest and Last CT Scores From Sequential Chest CT”。
论文第一作者、芜湖市第二人民医院的Guoquan Huang总结说,“COVID-19诊断和治疗越早,疾病消退的时间越短,CT最高评分和最后一次评分越低。”
3.全文编译!流行病学研究揭示COVID在意大利伦巴第地区的早期流行趋势
文献来源: The early phase of the COVID-19 outbreak in Lombardy
根据最近发表在预印本学术平台arXiv网站上的一篇文章,来自意大利博科尼大学,米兰大学等机构的研究者们揭示了在首例病例确诊之前,意大利境内伦巴第(Lombardy)早期的COVID19流行趋势。
2020年2月20日晚,在意大利的伦巴第大区确认了首例新型冠状病毒病(COVID-19)。 该患者是一名38岁的健康男性,患有轻度肺炎,没有相关的旅行史,也没有明显接触患病人群的经历。在随后的一周中,伦巴第地区的病例数量迅速增加。对此,研究者们对伦巴第地区报告的首批5830例实验室确诊病例进行了相关分析(统计症状发生日期为2020年1月14日至2020年3月8日),包括对上述确诊病例进行的流行病学分析,背景人口统计和暴露特征分析,以及该区域内感染的传播动态等等。此外,研究者们还基于报告病例的子样本进行病毒学特征分析,从而对有症状和无症状的病例的病毒载量水平进行了初步评估。该研究为西方国家早期的COVID19传播提供了新的线索。
根据调查结果,研究者们认为:COVID19在意大利境内的流行实际上早在2020年2月20日之前就已经开始。在发现第一例COVID-19病例时,该疾病已在南部伦巴第的大部分城市中广泛传播。
根据估计,意大利伦巴第地区患者从感染到症状出现平均间隔为6.6天,介于中国湖北省(平均7.5天)和其他中国省份(平均5.1天)之间。 作者认为我国其它省份的时间间隔比伦巴第地区少1.5天的原因是伦巴第的COVID-19病例没有像在中国的那些省份那样被迅速隔离,因此继续传播感染时间更长。 在流行的指数增长阶段,作者估计其平均R0值在2.3-3.1质检。 每天的繁殖数量随时间波动很大,但在各个地理区域内却相当一致。 2月20日之后Rt值会略有下降。但是仍远高于流行阈值。
4.Ann Intern Med:在咽拭子样本呈阴性后,一些患者的痰液和粪便样本仍为SARS-CoV-2阳性
doi:10.7326/M20-0991
在一项新的研究中,来自中国首都医科大学和中国疾控中心的研究人员发现在一些患者的咽拭子样本的实时荧光聚合酶链反应(RT-PCR)测试结果为SARS-CoV-2阴性后,他们的痰液或粪便样本的RT-PCR测试结果为SARS-CoV-2阳性。咽拭子被广泛用于确定患者是否适合出院和/或是否需要继续隔离。这些发现引起了人们的关注:咽拭子阴性的患者是否真地不携带病毒,或者是否需要对其他身体部位进行采样。相关研究结果近期发表在Annals of Internal Medicine期刊上,论文标题为“SARS-CoV-2–Positive Sputum and Feces After Conversion of Pharyngeal Samples in Patients With COVID-19”。
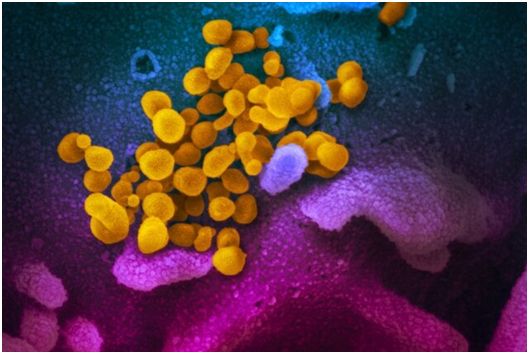
这些研究人员回顾性地确定了入住首都医科大学附属北京地坛医院的COVID-19患者的便利样本(convenience sample),并对这些患者的咽拭子与痰液或粪便进行了RT-PCR配对测试。在2020年1月20日至2月27日因患上COVID-19而住院的133例患者中,这些作者鉴定出22例患者的初次或随访痰液或粪便样本呈阳性,但是他们的随访咽拭子样本呈阴性;在咽拭子样本呈阴性后,痰液和粪便的RT-PCR测试结果为SARS-CoV2阳性的时间分别长达39天和13天。
5.EbioMedicine:重磅!COVID-19候选疫苗在首次同行评议研究中展现巨大希望!
doi:10.1016/j.ebiom.2020.102743
日前,一项刊登在国际杂志EbioMedicine上的研究报告中,来自匹兹堡大学等机构的科学家们通过研究公布了一项能抵御SARS-CoV-2的新型疫苗策略,SARS-CoV-2是引发COVID-19流行的一种冠状病毒,当通过指尖大小的贴片运输疫苗在小鼠机体中进行测试时,研究者发现,其所产生的针对SARS-CoV-2的特异性抗体就足以中和病毒了。
相关研究结果或为有效遏制COVID-19的传播和流行奠定坚实的基础,医学博士Andrea Gambotto表示,此前我们经历过2003年的SARS-CoV和2014年的MERS-CoV,这两种病毒与SARS-CoV-2非常相似,在研究的过程中,研究者发现,一种名为刺突蛋白(spike protein)的特殊蛋白对于有效诱导机体抵御病毒的免疫力非常重要,这样研究人员或许就知道如何有效抵御这种病毒了。
相比仅能进入临床试验的实验性mRNA疫苗而言,这种名为PittCoVacc(Pittsburgh Coronavirus Vaccine)的疫苗策略采用了一种更为成熟的方法,其能利用在实验室中制造的病毒蛋白片段来帮助机体建立免疫力,这与当前流感疫苗的开发理念是一样的。随后研究者还利用一种名为微针阵列(Microneedle Array)的新方法来运输药物从而增加其作用潜力,这种阵列是一个由400根微型针组成的指尖大小的贴片,其能将刺突蛋白片段运送到免疫反应最强的皮肤,这种贴片就好像创可贴一样,贴到皮肤上以后,其中由糖和蛋白质组成的针状结构就会溶解到皮肤中。
6.Nat Med:最新研究表明佩戴口罩确定可以降低冠状病毒传播
doi:10.1038/s41591-020-0843-2
在一项新的研究中,来自中国香港大学和美国马里兰大学的研究人员发现,医用口罩(surgical mask, 也译为外科口罩)可能有助于阻止感染者让其他人感染包括冠状病毒在内的季节性病毒,这可能有助于解决涉及临床和文化规范的激烈辩论。相关研究结果于2020年4月3日在线发表在Nature Medicine期刊上,论文标题为“Respiratory virus shedding in exhaled breath and efficacy of face masks”。论文通讯作者为香港大学医学院公共卫生学院流行病学与生物统计学部门负责人、世界卫生组织传染病流行病学与控制合作中心联合主任Benjamin J. Cowling博士。论文第一作者为香港大学的Nancy H. L. Leung博士。
在实验室实验中,根据利用马里兰大学公共卫生学院应用环境卫生学教授Don Milton博士开发的“Gesundheit II机器(Gesundheit II machine)”进行的呼吸测量结果,医用口罩可显著减少受感染患者产生的各种空气传播病毒的数量。
7.Science:利用追踪近距离接触者的移动应用程序控制冠状病毒传播
doi:10.1126/science.abb6936
在一项新的研究中,来自英国牛津大学的研究人员在Science期刊上发布的研究结果进一步加深了我们对冠状病毒SARS-CoV-2传播的了解。这一证据使得包括英国NHSX机构和挪威公共卫生研究所在内的多个国际合作伙伴能够评估在创纪录的时间内开发即时追踪接触者的移动应用程序的可行性。如果这些移动应用程序得到迅速和广泛的开发,那么它们可能有助于显著降低传播速率,并在限制逐渐放松的情况下,帮助各国安全地走出封锁。相关结果于2020年3月31日在线发表在Science期刊上,论文标题为“Quantifying SARS-CoV-2 transmission suggests epidemic control with digital contact tracing”。
论文通讯作者、牛津大学大数据研究所纳菲尔德医学系的Christophe Fraser教授说,“我们需要一种移动接触者追踪应用程序来紧急支持卫生服务,以控制冠状病毒传播、制定针对性的干预措施和并确保人们的安全。我们的分析表明,大约有一半的传播发生在感染的早期,也就是感染者未显示任何感染症状之前。我们的数学模型还强调,传统的公共卫生接触者追踪方法提供的数据不完整,无法跟上这次疫情的传播步伐。”
论文共同作者、牛津大学纳菲尔德医学系高级研究员、牛津大学约翰-拉德克利夫医院临床医生David Bonsall博士解释道,“我们在数学上建模的这种移动应用程序概念很简单,不需要追踪你所在的位置;它使用低能耗版本的蓝牙来记录所有应用程序用户最近几天有过近距离接触的人。如果你随后被感染,则这些与你接触的人会被立即匿名提醒,并且建议他们回家进行自我隔离。如果应用程序用户决定共享其他数据,那么他们可以支持卫生服务来确定疫情趋势,并针对最需要的人群采取针对性的干预措施。”
这些作者认为移动应用程序可以在疫情的任何阶段减少传播,即在疫情刚刚出现的国家或地区、在疫情高峰期,或支持安全解除移动限制或封锁。它还可能有助于减少因广泛封锁而造成的严重社会、心理和经济影响。至关重要的是,这些研究人员认为,在疫苗和抗病毒药物得到广泛应用之前,移动应用程序可以帮助减缓感染的传播。
8.Cell:重磅!体外研究表明试验用药物APN01可显著阻断SARS-CoV-2感染
doi:10.1016/j.cell.2020.04.004
在一项新的研究中,来自加拿大、瑞典、西班牙和奥地利的研究人员发现一种试验用药物可有效阻断SARS-CoV-2感染宿主所使用的细胞进入受体。这一发现有望开发出一种阻断这种新型冠状病毒早期感染的治疗方法。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Inhibition of SARS-CoV-2 infections in engineered human tissues using clinical-grade soluble human ACE2”。针对SARS-CoV-2及其在细胞水平上与宿主细胞相互作用的关键方面,以及这种病毒如何感染血管和肾脏,这项研究提供了新的见解。
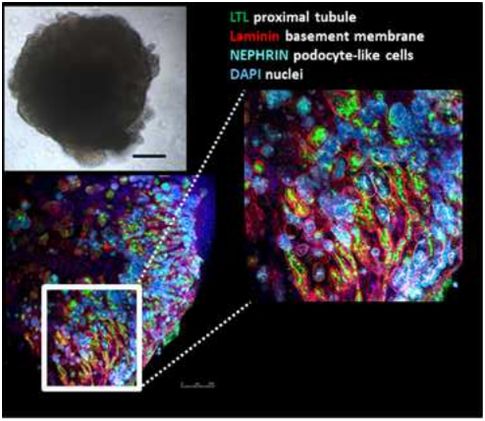
论文共同通讯作者、加拿大英属哥伦比亚大学生命科学研究所所长Josef Penninger教授说,“我们希望我们的结果对治疗这种史无前例的疫情的新型药物的开发产生影响。这项研究源于学术研究人员和公司之间的惊人合作,包括来自位于温哥华市的STEMCELL Technologies公司的Ryan Conder博士及其在胃肠道方面的研究团队、来自西班牙的Nuria Montserrat、来自多伦多市的Haibo Zhang博士和Art Slutsky博士,尤其是来自瑞典的Ali Mirazimi及其在传染生物学方面的研究团队。他们日夜不懈地工作了几个星期,旨在更好地了解这种疾病的病理和提供突破性的治疗选择。”
Slutsky博士说,“我们的新研究提供了极其需要的直接证据表明一种称为APN01(human recombinant soluble angiotensin-converting enzyme 2, 人重组可溶性血管紧张素转化酶2, 简称hrsACE2)的药物可作为一种抗病毒药物用于治疗COVID-19。欧洲生物技术公司Apeiron Biologics即将在临床试验中测试这种药物。”
在这项新研究分析的细胞培养物中,hrsACE2将SARS-CoV-2的病毒载量抑制了1000~5000倍。在由人干细胞培养出的人类血管和肾脏类器官中,这些研究人员证实这种病毒可以直接感染这些组织并在其中进行自我复制。这提供了有关这种疾病发展以及严重的COVID-19病例出现多器官衰竭和心血管损伤的重要信息。临床级hrsACE2还减少了这些体外培养出的人体组织中的SARS-CoV-2感染。
9.Science重磅!SARS-CoV-2的致命弱点或是其与SARS抗体的结合位点!
doi:10.1126/science.abb7269
Scripps研究所的科学家进行的一项研究显示,21世纪初从一名非典(SARS)幸存者身上发现的一种抗体揭示了最近这种导致COVID-19的新型冠状病毒的潜在弱点。
4月3日发表在Science杂志上的这项研究,首次以接近原子尺度的分辨率描绘了人类抗体与新型冠状病毒的相互作用。这种抗体是在SARS(严重急性呼吸系统综合症)感染时产生的,尽管SARS是由SARS-CoV病毒引起的,但它可以与新型冠状病毒SARS-CoV-2发生交叉反应。该 结构图谱揭示了抗体结合两个冠状病毒上几乎相同的位点,这表明该位点是冠状病毒家族重要的功能和易损位点。
"像这种位点保守的知识可以帮助对SARS-CoV-2疫苗和疗法基于结构的设计,而这些疗法也将防止其他可能出现在未来的冠状病毒,"这项研究的资深作者Ian Wilson说道,他是Scripps研究所计算生物学和综合结构系主任以及结构生物学的Hansen教授。
10.bioRxiv:科学家鉴别出抵御SARS-CoV-2感染的新型潜在药物靶点
doi:10.1101/2020.03.02.968388
近日,发表在预印版网站bioRxiv上的一篇研究报告中,来自加利福尼亚大学等机构的科学家们通过研究鉴别出了治疗SARS-CoV-2感染的新型潜在药物靶点;文章中,研究人员绘制出了两个关键SARS-CoV-2蛋白组成的复合体nsp10/16的原子结构,这两种蛋白能够修饰病毒 的遗传物质从而使其更像人类的RNA,这样就能促进病毒躲避宿主机体的抗病毒免疫机制并进行病毒复制。
研究者认为,如果有一种药物能抑制nsp10/16复合体的功能,那么宿主免疫系统或许就能检测到病毒并对其快速清除;研究者Godzik表示,我们首先设计出了一部分DNA来表达两种蛋白,随后对所产生的两种蛋白的结构进行分析;nsp10/nsp16蛋白复合体称之为RNA甲基转 移酶或MTase,其由于结合在一起的两种蛋白质组成,根据此前研究人员对SARS的研究,需要将这两部分结合在一起才能让蛋白复合体发挥作用。
研究者表示,他们需要多种药物来治疗SARS-CoV-2的感染,因为这种疾病会伴随人类很长一段时间,目前仅仅开发出一种药物是远远不够的,如果SARS-CoV-2对一种药物产生了耐受性,那么研究人员就需要开发出其它治疗性药物了。nsp15核酸内切酶、nsp3 ADP磷酸核糖 和nsp9复制酶,这三种蛋白质的结构对于病毒复制释放非常重要;如今研究人员绘制出了SARS-CoV-2的完整蛋白质结构体系,通过解决附加结构来扩大蛋白质结构的覆盖范围或许是后期科学家们的研究方向,第二个方向就是与潜在药物的共结晶实验,研究人员想知道冠 状病毒是如何与药物进行结合的,如果能解析清楚其中的机制,或能帮助研究者更高效地改进药物从而靶向作用SARS-CoV-2。
11.J Travel Med:ACE抑制剂和血管紧张素受体阻滞剂或会增加人群患严重COVID-19的风险
doi:10.1093/jtm/taaa041
近日,一项刊登在国际杂志Journal of Travel Medicine上的研究报告中,来自路易斯安那州立大学等机构的科学家们通过研究解释了为何某些被诊断为COVID-19的患者会出现严重的肺部并发症,相关研究结果或有望帮助开发治疗COVID-19的新型疗法。
2003年,SARS-CoV(SARSβ冠状病毒)引发了非典(严重急性呼吸综合征),如今SARS-CoV-2引发了COVID-19,SARS-CoV-2能与机体下呼吸道中的受体ACE2(血管紧张素转换酶2,angiotensin converting enzyme 2)结合从而进入到肺部,病毒性肺炎和可能致命的呼吸 衰竭会在10-14天后在易感人群中发生。
研究者Diaz表示,血管紧张素转换酶抑制剂(ACEIs)和血管紧张素受体阻滞剂(ARBs)是推荐给心血管疾病患者的常用药物,其能治疗包括心脏病、高血压、糖尿病和慢性肾脏疾病等多种人类疾病;其中许多患者均为老年人,医生通常会给其开具上述药物让患者每天服 用。
对实验性模型研究结果表明,当静脉输注ACE抑制剂后,机体呼吸系统中ACE2受体的数量会发生增加;由于利用ACEIs和ARBs治疗的患者的肺脏中ACE2受体的水平会增加,且能与冠状病毒S蛋白相互结合,因此患者会因遭遇SARS-CoV-2感染表现出严重疾病患病风险增加的状 况。
12.Nature:当COVID-19症状相对较轻时,患者较高水平地脱落病毒SARS-CoV-2
doi:10.1038/s41586-020-2196-x
在一项新的研究中,来自德国联邦国防军微生物研究所、慕尼黑施瓦宾格医院、柏林大学夏丽特医学院和慕尼黑大学医院的研究人员详细分析了来自德国慕尼黑的9名患上COVID-19呼吸道疾病且症状相对较轻的成年患者。这项研究表明冠状病毒SARS-CoV-2在这些患者的上 呼吸道中活跃复制,这表明患者在症状出现的第一周内可能较高水平地‘脱落’或者说排泄这种病毒。相关研究结果于2020年4月1日在线发表在Nature期刊上,论文标题为“Virological assessment of hospitalized patients with COVID-2019”。
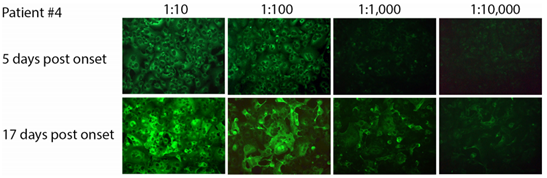
论文共同通讯作者Christian Drosten及其同事们研究了9名诊断为COVID-19的中青年成年人的病毒脱落情况,这些患者因轻度上呼吸道症状在慕尼黑的一家医院接受治疗。他们分析了在临床治疗过程中从这些患者体内采集的喉部和肺部样本、痰液(即呼吸道粘液)、粪 便、血液和尿液。
这些作者发现在上呼吸道组织中SARS-CoV-2病毒复制水平较高,并且报告在症状发作的第一周内在上呼吸道中病毒脱落的水平也较高。他们都可以从这些患者体内采集的喉咙和肺部样本中分离出这种病毒的传染性形式,直到症状消失的第八天。其中的两名表现出一些早 期肺炎症状的患者持续在痰液中脱落较高水平的SARS-CoV-2直到症状消失的第十天或第十一天。在症状结束后,痰液中仍可检测到这种病毒的RNA。
血液和尿液样本中未检测到这种病毒,而且这些作者发现粪便样本中虽然存在较高浓度的病毒RNA,但是并未发现这种病毒的复制形式,这支持了它可能无法通过粪便传播的理论。但是,还需要在较大样本中进一步研究这种可能的传播途径。
13.万万没想到!研究下水道废水可以帮助对抗COVID-19疫情!
doi:10.1021/acs.est.0c01174
克兰菲尔德大学(Cranfield University)的研究人员正在研究一种新的检测方法,以检测感染了这种病毒的社区废水中的SARS-CoV-2。
基于废水的流行病学(WBE)方法可以通过收集进入下水道系统的疾病携带者的粪便和尿液中的生物标志物,为预测新型冠状病毒肺炎(COVID-19)的潜在传播提供一种有效和快速的方法。
使用基于纸张的设备的快速测试包可以在废水处理厂现场使用,以跟踪来源并确定在当地是否存在潜在的COVID-19载体。
克兰菲尔德水科学研究所传感器技术讲师Zhugen Yang博士说:"在社区或无症状感染的情况下当人们不知道他们是否被感染,通过简单的分析检测设备实时检测社区污水可以确定在一个地区有COVID-19的情况下支持快速筛查,隔离和预防。
14.Aging Dis:好消息!干细胞疗法有效对抗COVID-19肺炎
doi:10.14336/AD.2020.0228
当冠状病毒的消息出现时,Kunlin Jin博士和一组国际研究人员迅速联合起来对抗这种神秘的疾病。Jin博士说,"我们的研究表明,静脉输注临床级的人骨髓间充质干细胞是治疗COVID-19肺炎--包括老年重症肺炎患者的一种安全有效的方法。"
作为实验治疗的一部分,干细胞被静脉注射到北京的7名重症患者的血液中。研究称,三名患者被注射了安慰剂。
Jin博士说,接受检测的是北京佑安医院的病人。研究显示,检测从1月30日开始。Jin博士说,接受干细胞治疗的七名患者获得了成功,并在14天内出院。在接受安慰剂的患者中,一名死亡,一名病情严重,第三名患有急性呼吸窘迫综合征(ARDS)。
该研究小组的发现将发表在即将出版的2020年4月的《Aging and Disease》杂志上。这篇文章的标题是"Transplantation of ACE2-Mesenchymal Stem Cells Improves the Outcome of Patients with COVID-19 Pneumonia。"
15.bioRxiv:突破!合成多肽药物可以阻断SARS-CoV-2病毒与人类细胞结合
doi:10.1101/2020.03.19.999318
为了开发出治疗COVID-19的可能方法,麻省理工学院的一组化学家设计了一种候选药物,他们认为这种药物可以阻止冠状病毒进入人体细胞。这种潜在的药物是一种短的蛋白质片段,或肽段,它模仿一种在人类细胞表面发现的蛋白质。
研究人员已经证明,他们的新肽可以与冠状病毒用来进入人类细胞的病毒蛋白结合,从而有可能解除这种蛋白的武装。
"我们有我们真的想要探索的主要化合物,因为它事实上可以与病毒蛋白以一种我们预测的方式相互作用,所以它有机会抑制病毒进入宿主细胞,"领导该研究的麻省理工学院的化学副教授Brad Pentelute说道。
麻省理工学院的研究小组在3月20日发布在bioRxiv(一个在线预印本服务器)上的预印本中报告了他们的初步发现。他们已经将肽的样品寄给了计划在人体细胞中进行试验的合作者。
16.Ophthalmology:新型冠状病毒通可以通过眼泪传播?
doi:10.1016/j.ophtha.2020.03.026
虽然研究人员确定冠状病毒是通过咳嗽或打喷嚏排出的粘液和飞沫传播的,但目前还不清楚这种病毒是否通过其他体液传播,比如眼泪。最新发表的研究提供了证据,表明受感染的病人不太可能通过眼泪传播病毒,但有一个重要的警告。在这项研究中,没有一个病人患 有结膜炎,也被称为粉红眼。然而,卫生官员认为,只有1%到3%的冠状病毒感染者会出现粉红色眼睛。该研究的作者得出结论,他们的发现,加上感染患者中粉红色眼睛的发病率较低,表明通过眼泪传播病毒的风险较低。他们的研究发表在《眼科学》(Ophthalmology)杂 志网络版上,该杂志是美国眼科学会(American Academy of Ophthalmology)的期刊。
为了进行这项研究,新加坡国立大学医院的临床医学学士Ivan Seah和他的同事收集了17名COVID-19患者的眼泪样本,从他们出现症状到大约20天后恢复。无论是病毒培养还是逆转录聚合酶链反应(RT-PCR)都没有在患者的眼泪中检测到病毒。
在同一时期,Seah博士还从鼻子后部和喉咙处取样。虽然病人的眼泪里没有病毒,但他们的鼻子和喉咙里却充满了病毒。Seah博士说,他希望他们的工作有助于指导更多的研究,防止病毒通过更重要的途径传播,如飞沫和粪便-口腔传播。
17.重磅!两篇Nature揭示SARS-CoV-2结合ACE2受体的晶体结构
doi:10.1038/s41586-020-2180-5; doi:10.1038/s41586-020-2179-y
一种新型高致病性冠状病毒(SARS-CoV-2)自2019年12月以来肆掠全球,应对这一疫情的关键是了解病毒的受体识别机制,调节其感染性、发病机制和宿主范围。而在分子和原子水平了解SARS-CoV-2如何感染细胞有利于科学家们更快开发出更有效地预防或者治疗性药物。
3月30日,Nature杂志在线发表了两项最新研究,揭示了SARS-CoV-2识别和结合人ACE2的机制及形成的复合物的晶体结构,两项研究分别为清华大学王新泉课题组和张林琦课题组合作发表的"Structure of the SARS-CoV-2 spike receptor-binding domain bound to the ACE2 receptor"以及明尼苏达大学李放教授课题组发表的"Structural basis of receptor recognition by SARS-CoV-2"。
为了在原子水平上更好地理解感染的初始步骤,我们王新泉课题组和张林琦课题组以2.45 A的分辨率确定了与细胞受体ACE2结合的SARS-CoV-2 刺突蛋白受体结合域(spike receptor binding domain,RBD)的晶体结构。SARS-CoV-2 RBD和ACE2的整体结合模式与SARS-CoV RBD几乎相同,后者也利用ACE2作为细胞受体。研究人员在SARS-CoV-2 RBD中结构分析发现了对ACE2结合至关重要的残基,其中大部分要么高度保守,要么与SARS-CoV RBD中的残基具有类似的侧链性质。研究人员发现虽然SARS-CoV-2不会在SARS和SARS相关的冠状病毒中聚 集,但这种结构和序列上的相似性有力地证明了SARS-CoV-2和SARS-CoV RBDs之间的趋同进化可以改善它们与ACE2的结合。研究人员还分析了以RBD为靶点的两种SARS-CoV抗体的表位,为今后交叉反应性抗体的鉴定提供了思路。
在另一项研究中,李放教授课题组确定了与hACE2配合物中SARS-CoV-2受体结合域(RBD)的晶体结构(利用一种可以促进结晶的工程化RBD)。研究人员发现与SARS-CoV RBD相比,在SARS-CoV-2 RBD中,hACE2的结合具有更紧密的构象;此外,SARS-CoV-2 RBD中的几个残基变 化稳定了RBD/hACE2界面上的两个病毒结合热点。SARS-CoV-2 RBD的这些结构特征增强了其与hACE2的结合亲和力。此外,研究人员还发现与SARS-CoV-2密切相关的蝙蝠冠状病毒RaTG13也使用hACE2作为其受体。在hACE2识别中,SARS-CoV-2、SARS-CoV和RaTG13的差异揭示 了SARS-CoV-2在动物和人类之间潜在的传播途径。本研究为SARS-CoV-2靶向受体识别的干预策略提供指导。
总的来说,这两项研究利用X光晶体衍射技术,揭示了SARS-CoV-2与ACE2结合的微观晶体结构,有助于科学家了解ACE2受体介导的SARS-CoV-2识别和感染细胞的过程,可以加快科学家开发治疗性药物和疫苗的进程。
18.Nat Commun:利用新的RNA成像技术开发的冠状病毒检测试剂盒
doi:10.1038/s41467-020-14932-7
西蒙弗雷泽大学的研究人员将使用他们的先进成像技术--Mango(因为它明亮的颜色)--来开发冠状病毒测试工具。他们是对加拿大卫生研究院(CIHR)最近宣布的帮助解决COVID-19的快速资助机会做出反应的一小部分加拿大研究人员之一。
SFU的博士后研究员Lena Dolgosheina和分子生物学和生物化学教授Peter Unrau开发出了Mango,可以敏感地检测RNA分子,帮助改善病毒对病毒的筛选,如冠状病毒,同时使细胞功能的基本发现成为可能。由Unrau领导的最新研究涉及到使用Mango来检测活细胞内的单个 RNA分子。
Unrau说:"我们是由分子组成的,所以当一个细胞出了问题,它就会发生在分子水平上。我们正在利用Mango系统作为催化剂,使我们不仅能够扩展基础研究问题,而且能够更快、更有效地检测冠状病毒等病原体。"
Mango系统由RNA Mango适配体组成,该适配体可以与荧光染料紧密结合。该适配体的作用类似于磁靶向并结合那些染料分子。染料一接触就会兴奋起来,发出明亮的光芒。经过修饰以包含适配体"磁铁"的RNA分子可以从细胞的其他部分中脱颖而出,这使得研究人员更容易 在显微镜下观察和研究RNA分子。
19.Cell:我国科学家从结构和功能角度揭示SARS-CoV-2利用人ACE2进入细胞机制
doi:10.1016/j.cell.2020.03.045
病毒感染始于病毒颗粒与宿主表面细胞受体的结合。因此,受体识别是病毒的细胞和组织嗜性(tropism)的一个重要决定因素。此外,病毒结合其他物种的相应受体的功能获得也是物种间传播的先决条件。有趣的是,除了HCoV-OC43和HKU1均与糖分子结合从而与细胞附 着外,其他的四个人类冠状病毒均将蛋白肽酶识别为受体。HCoV-229E与人氨基肽酶N(hAPN)结合,而MERS-CoV与人二肽基肽酶4(hDPP4或hCD26)相互作用。尽管SARS-CoV和hCoV-NL63属于不同的冠状病毒属,但是它们均与人类血管紧张素转化酶2(hACE2,即人ACE2) 相互作用以进入宿主细胞。在COVID-19疫情爆发后,中国科学家迅速确定SARS-CoV-2也利用hACE2进入细胞。
在冠状病毒中,这种进入过程是由嵌入包膜的位于病毒表面的刺突糖蛋白(S蛋白)介导的。在大多数情况下,S蛋白会被宿主蛋白酶切割为分别负责受体识别和膜融合的S1和S2亚基。 S1可以进一步分为N末端结构域(NTD)和C末端结构域(CTD),两者都可以充当受体结 合实体(比如,SARS-CoV和MERS-CoV都利用S1 CTD识别受体,因而称为受体结合结构域(RBD),然而小鼠肝炎冠状病毒利用它的S1 NTD与受体结合。在此之前,SARS-CoV-2 S蛋白中负责与hACE2相互作用的区域仍然是未知的。
在一项新的研究中,来自中国科学院、深圳市第三人民医院、山西农业大学、安徽大学、四川大学、中国科技大学和香港大学的研究人员利用免疫染色和流式细胞仪测定技术,首先鉴定出S1 CTD(SARS-CoV-2-CTD)是SARS-CoV-2中与hACE2受体相互作用的关键区域。他们 随后解析出SARS-CoV-2-CTD与hACE2结合在一起时的分辨率为2.5 ?的晶体结构,揭示了一种整体上与SARS-CoV RBD(下称SARS-RBD)相类似的受体结合模式。但是,与SARS-RBD相比,SARS-CoV-2-CTD与hACE2形成更多的原子相互作用,这与显示更高的受体结合亲和力的数 据相关。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Structural and functional basis of SARS-CoV-2 entry by using human ACE2”。
值得注意的是,一组单克隆抗体(mAb)以及针对SARS-S1/RBD的鼠多克隆抗血清无法与SARS-CoV-2 S蛋白结合,这表明SARS-CoV和SARS-CoV在抗原性上存在显著差异,并且提示着先前开发的基于SARS-RBD的候选疫苗不太可能对SARS-CoV-2预防有任何临床益处。
20.全文编译!复旦大学在Cell期刊上发文,从基因组学角度揭示SARS-CoV-2的起源和出现
doi:10.1016/j.cell.2020.03.035
新型人类冠状病毒SARS-CoV-2(之前称为2019-nCoV)的持续大流行引起了全球的极大关注。我们和中国的其他人参与了对这种病毒的初始基因组测序。在本文中,我们描述了针对SARS-CoV-2的出现,这些基因组数据揭示了什么,并讨论了我们对其起源理解上所存在的差 距。
在英国爱丁堡大学Andrew Rambaut博士的帮助下,我们于2020年1月11日(格林威治标准时间, GMT)早些时候在开放存取的virological.org网站(http://virological.org/)上发布了这种病毒的基因组序列。不久之后,中国疾控中心在公众可访问的GISAID数据库 (https://www.gisaid.org/)上类似地发布了SARS-CoV-2基因组序列(以及相关的流行病学数据)。在撰写本文时,已有近200个SARS-CoV-2基因组可公开获得,这代表了来自中国及其他地区的这种病毒的基因组多样性,并提供了可自由获取的全球资源。重要的是, SARS-CoV-2基因组序列数据的发布促进了诊断测试和感染性克隆(infectious clone)的快速开发。研发有效疫苗和抗病毒药物的竞赛正在进行中,而且针对抗病毒药物的临床试验正在逐步展开。
尽管SARS-CoV和MERS-CoV与SARS-CoV-2密切相关并且都有蝙蝠宿主,但这两种病毒之间的生物学差异却很明显。如上所述,SARS-CoV-2的传染性明显更高,从而导致与SARS-CoV和MERS-CoV完全不同的流行病学动态。在后两种病毒中,病例数的增长相对较慢,而MERS-CoV 从未完全适应人类传播:大多数病例是由于阿拉伯半岛的骆驼溢出造成的,仅零星地发生人与人之间的传播。相比之下,SARS-CoV-2在当地的显著传播最让人吃惊。确定支撑这种传播能力的病毒学特征显然是当务之急。
SARS-CoV-2似乎将不可避免地成为人类中的第五种地方性冠状病毒(其他四种为HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1),并且目前正在完全易感人群中传播。冠状病毒显然具有跨越物种界限并适应新宿主的能力,这使得预测未来会有更多的病毒出现变得很简 单,不过尚不清楚为何相比于一些其他的RNA病毒,冠状病毒具有这种能力。至关重要的是,对动物冠状病毒的监视应包括蝙蝠以外的动物,这是因为中间宿主的作用可能非常重要,从而为病毒在人类中的出现提供了更直接的途径。
鉴于野生动物中病毒的多样性以及它们的持续进化,可以说,降低未来疫情爆发风险的最简单最具成本效益的方法是尽可能限制我们对动物病原体的接触。尽管我们与动物世界的亲密关系意味着我们无法建立坚不可摧的屏障,但是针对非法野生动物贸易采取更强有力的 行动,以及将所有野生哺乳动物(也许还有禽类)从湿货市场中清除将提供一个重要的缓冲。(生物谷 Bioon.com)
2020年2月11日,世卫组织将这种疾病病重命名为2019年冠状病毒病(COVID-19)。同一天,负责分类和命名病毒的的国际病毒分类学委员会的冠状病毒研究小组在bioRxiv上发表了一篇文章,指出该研究小组已经决定,新型冠状病毒2019-nCoV是导致2002-2003年爆发严重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)的变种。因此,将这种新病原体重新命名为严重急性呼吸综合征冠状病毒2号(severe acute respiratory syndrome coronavirus 2),或SARS-CoV-2。值得注意的一点是,尽管国际病毒分类委员会冠状病毒研究小组将病毒命名为SARS-CoV-2,但该研究小组主席John Ziebuhr认为这个名字(SARS-CoV-2)和SARS(严重急性呼吸综合征,也称非典型肺炎)没有关联。不过,这种病毒的重新命名引起了不少争议。据《科学》网站报道,世界卫生组织不满意SARS-CoV-2这个名字,而且不打算采用此名称。
冠状病毒可引起多种动物的多系统感染。在此之前已有6种冠状病毒可以感染人类,它们主要引起人类的呼吸道感染:两种高度致命性的冠状病毒,即严重急性呼吸道综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV);4种可导致温和的上呼吸道疾病的冠状病毒,即HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1。
基于此次疫情给中国和全世界带来严重的危害,小编针对近期2019-nCoV/COVID-19研究取得的进展进行一番梳理,以飨读者。
1.bioRxiv:揭示SARS-CoV-2在人细胞和雪貂中引起了减弱的抗病毒反应
doi:10.1101/2020.03.24.004655
根据2020年3月24日发表在预印本服务器bioRxiv上的一项未经过同行评审的研究,导致COVID-19疫情爆发的新型冠状病毒SARS-CoV-2似乎在人细胞和雪貂中引起了减弱的抗病毒反应。这项研究的作者提出宿主对这种冠状病毒的独特转录反应可能是这种冠状病毒高病死率的原因。相关研究的论文标题为“SARS-CoV-2 launches a unique transcriptional signature from in vitro, ex vivo, and in vivo systems”。

图片来自bioRxiv, 2020, doi:10.1101/2020.03.24.004655。
美国西奈山伊坎医学院微生物学家Benjamin tenOever和他的研究团队在SARS-CoV-2出现时就已经在研究呼吸道病毒了,因此他们将早期的研究工作纳入到他们正在进行的研究中。为了比较这种冠状病毒和季节性呼吸道病毒,他们让甲型流感病毒(IAV)、呼吸道合胞病毒(RSV)或SARS-CoV-2感染肺癌细胞系,并对来自受感染细胞的RNA进行测序。他们发现正如IAV和RSV一样,SARS-CoV-2能够在这些细胞中复制,而且它表现出的转录反应在强度上与IAV相类似,但强度不如RSV。
当研究哪些基因会因病毒感染而上调时,他们发现SARS-CoV-2刺激了一组宿主基因的表达,而且相比于IAV,这种冠状病毒激活的转录程序与RSV更为相似。但是SARS-CoV-2似乎没有诱导RSV和IAV都能诱导的两个重要的抗病毒基因---编码I型和III型干扰素的基因---的表达,它们是通过发出战斗号角提醒邻近细胞存在病毒入侵者的抗病毒程序的一部分。这种冠状病毒确实增强了两种独特的细胞因子的表达,它们是先前已经证实与肺部炎症有关的分泌因子。
2.AJR:CT评分新标准可定量、准确地评估COVID-19肺炎进展
doi:10.2214/AJR.20.23078
新型冠状病毒SARS-CoV-2(之前称为2019-nCoV)导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。在一项新的研究中,来自中国芜湖市第二人民医院、山东大学、芜湖市第三人民医院和安徽医科大学第一附属医院等研究机构的研究人员报道,经更新后考虑肺叶受累和CT表现变化的CT评分新标准,可以定量、准确地评估COVID-19肺炎的进展。相关研究结果发表在American Journal of Roentgenology期刊上,论文标题为“Timely Diagnosis and Treatment Shortens the Time to Resolution of Coronavirus Disease (COVID-19) Pneumonia and Lowers the Highest and Last CT Scores From Sequential Chest CT”。
论文第一作者、芜湖市第二人民医院的Guoquan Huang总结说,“COVID-19诊断和治疗越早,疾病消退的时间越短,CT最高评分和最后一次评分越低。”
3.全文编译!流行病学研究揭示COVID在意大利伦巴第地区的早期流行趋势
文献来源: The early phase of the COVID-19 outbreak in Lombardy
根据最近发表在预印本学术平台arXiv网站上的一篇文章,来自意大利博科尼大学,米兰大学等机构的研究者们揭示了在首例病例确诊之前,意大利境内伦巴第(Lombardy)早期的COVID19流行趋势。
2020年2月20日晚,在意大利的伦巴第大区确认了首例新型冠状病毒病(COVID-19)。 该患者是一名38岁的健康男性,患有轻度肺炎,没有相关的旅行史,也没有明显接触患病人群的经历。在随后的一周中,伦巴第地区的病例数量迅速增加。对此,研究者们对伦巴第地区报告的首批5830例实验室确诊病例进行了相关分析(统计症状发生日期为2020年1月14日至2020年3月8日),包括对上述确诊病例进行的流行病学分析,背景人口统计和暴露特征分析,以及该区域内感染的传播动态等等。此外,研究者们还基于报告病例的子样本进行病毒学特征分析,从而对有症状和无症状的病例的病毒载量水平进行了初步评估。该研究为西方国家早期的COVID19传播提供了新的线索。
根据调查结果,研究者们认为:COVID19在意大利境内的流行实际上早在2020年2月20日之前就已经开始。在发现第一例COVID-19病例时,该疾病已在南部伦巴第的大部分城市中广泛传播。
根据估计,意大利伦巴第地区患者从感染到症状出现平均间隔为6.6天,介于中国湖北省(平均7.5天)和其他中国省份(平均5.1天)之间。 作者认为我国其它省份的时间间隔比伦巴第地区少1.5天的原因是伦巴第的COVID-19病例没有像在中国的那些省份那样被迅速隔离,因此继续传播感染时间更长。 在流行的指数增长阶段,作者估计其平均R0值在2.3-3.1质检。 每天的繁殖数量随时间波动很大,但在各个地理区域内却相当一致。 2月20日之后Rt值会略有下降。但是仍远高于流行阈值。
4.Ann Intern Med:在咽拭子样本呈阴性后,一些患者的痰液和粪便样本仍为SARS-CoV-2阳性
doi:10.7326/M20-0991
在一项新的研究中,来自中国首都医科大学和中国疾控中心的研究人员发现在一些患者的咽拭子样本的实时荧光聚合酶链反应(RT-PCR)测试结果为SARS-CoV-2阴性后,他们的痰液或粪便样本的RT-PCR测试结果为SARS-CoV-2阳性。咽拭子被广泛用于确定患者是否适合出院和/或是否需要继续隔离。这些发现引起了人们的关注:咽拭子阴性的患者是否真地不携带病毒,或者是否需要对其他身体部位进行采样。相关研究结果近期发表在Annals of Internal Medicine期刊上,论文标题为“SARS-CoV-2–Positive Sputum and Feces After Conversion of Pharyngeal Samples in Patients With COVID-19”。

图片来自NIAID-RML。
这些研究人员回顾性地确定了入住首都医科大学附属北京地坛医院的COVID-19患者的便利样本(convenience sample),并对这些患者的咽拭子与痰液或粪便进行了RT-PCR配对测试。在2020年1月20日至2月27日因患上COVID-19而住院的133例患者中,这些作者鉴定出22例患者的初次或随访痰液或粪便样本呈阳性,但是他们的随访咽拭子样本呈阴性;在咽拭子样本呈阴性后,痰液和粪便的RT-PCR测试结果为SARS-CoV2阳性的时间分别长达39天和13天。
5.EbioMedicine:重磅!COVID-19候选疫苗在首次同行评议研究中展现巨大希望!
doi:10.1016/j.ebiom.2020.102743
日前,一项刊登在国际杂志EbioMedicine上的研究报告中,来自匹兹堡大学等机构的科学家们通过研究公布了一项能抵御SARS-CoV-2的新型疫苗策略,SARS-CoV-2是引发COVID-19流行的一种冠状病毒,当通过指尖大小的贴片运输疫苗在小鼠机体中进行测试时,研究者发现,其所产生的针对SARS-CoV-2的特异性抗体就足以中和病毒了。
相关研究结果或为有效遏制COVID-19的传播和流行奠定坚实的基础,医学博士Andrea Gambotto表示,此前我们经历过2003年的SARS-CoV和2014年的MERS-CoV,这两种病毒与SARS-CoV-2非常相似,在研究的过程中,研究者发现,一种名为刺突蛋白(spike protein)的特殊蛋白对于有效诱导机体抵御病毒的免疫力非常重要,这样研究人员或许就知道如何有效抵御这种病毒了。
相比仅能进入临床试验的实验性mRNA疫苗而言,这种名为PittCoVacc(Pittsburgh Coronavirus Vaccine)的疫苗策略采用了一种更为成熟的方法,其能利用在实验室中制造的病毒蛋白片段来帮助机体建立免疫力,这与当前流感疫苗的开发理念是一样的。随后研究者还利用一种名为微针阵列(Microneedle Array)的新方法来运输药物从而增加其作用潜力,这种阵列是一个由400根微型针组成的指尖大小的贴片,其能将刺突蛋白片段运送到免疫反应最强的皮肤,这种贴片就好像创可贴一样,贴到皮肤上以后,其中由糖和蛋白质组成的针状结构就会溶解到皮肤中。
6.Nat Med:最新研究表明佩戴口罩确定可以降低冠状病毒传播
doi:10.1038/s41591-020-0843-2
在一项新的研究中,来自中国香港大学和美国马里兰大学的研究人员发现,医用口罩(surgical mask, 也译为外科口罩)可能有助于阻止感染者让其他人感染包括冠状病毒在内的季节性病毒,这可能有助于解决涉及临床和文化规范的激烈辩论。相关研究结果于2020年4月3日在线发表在Nature Medicine期刊上,论文标题为“Respiratory virus shedding in exhaled breath and efficacy of face masks”。论文通讯作者为香港大学医学院公共卫生学院流行病学与生物统计学部门负责人、世界卫生组织传染病流行病学与控制合作中心联合主任Benjamin J. Cowling博士。论文第一作者为香港大学的Nancy H. L. Leung博士。
在实验室实验中,根据利用马里兰大学公共卫生学院应用环境卫生学教授Don Milton博士开发的“Gesundheit II机器(Gesundheit II machine)”进行的呼吸测量结果,医用口罩可显著减少受感染患者产生的各种空气传播病毒的数量。
7.Science:利用追踪近距离接触者的移动应用程序控制冠状病毒传播
doi:10.1126/science.abb6936
在一项新的研究中,来自英国牛津大学的研究人员在Science期刊上发布的研究结果进一步加深了我们对冠状病毒SARS-CoV-2传播的了解。这一证据使得包括英国NHSX机构和挪威公共卫生研究所在内的多个国际合作伙伴能够评估在创纪录的时间内开发即时追踪接触者的移动应用程序的可行性。如果这些移动应用程序得到迅速和广泛的开发,那么它们可能有助于显著降低传播速率,并在限制逐渐放松的情况下,帮助各国安全地走出封锁。相关结果于2020年3月31日在线发表在Science期刊上,论文标题为“Quantifying SARS-CoV-2 transmission suggests epidemic control with digital contact tracing”。
论文通讯作者、牛津大学大数据研究所纳菲尔德医学系的Christophe Fraser教授说,“我们需要一种移动接触者追踪应用程序来紧急支持卫生服务,以控制冠状病毒传播、制定针对性的干预措施和并确保人们的安全。我们的分析表明,大约有一半的传播发生在感染的早期,也就是感染者未显示任何感染症状之前。我们的数学模型还强调,传统的公共卫生接触者追踪方法提供的数据不完整,无法跟上这次疫情的传播步伐。”
论文共同作者、牛津大学纳菲尔德医学系高级研究员、牛津大学约翰-拉德克利夫医院临床医生David Bonsall博士解释道,“我们在数学上建模的这种移动应用程序概念很简单,不需要追踪你所在的位置;它使用低能耗版本的蓝牙来记录所有应用程序用户最近几天有过近距离接触的人。如果你随后被感染,则这些与你接触的人会被立即匿名提醒,并且建议他们回家进行自我隔离。如果应用程序用户决定共享其他数据,那么他们可以支持卫生服务来确定疫情趋势,并针对最需要的人群采取针对性的干预措施。”
这些作者认为移动应用程序可以在疫情的任何阶段减少传播,即在疫情刚刚出现的国家或地区、在疫情高峰期,或支持安全解除移动限制或封锁。它还可能有助于减少因广泛封锁而造成的严重社会、心理和经济影响。至关重要的是,这些研究人员认为,在疫苗和抗病毒药物得到广泛应用之前,移动应用程序可以帮助减缓感染的传播。
8.Cell:重磅!体外研究表明试验用药物APN01可显著阻断SARS-CoV-2感染
doi:10.1016/j.cell.2020.04.004
在一项新的研究中,来自加拿大、瑞典、西班牙和奥地利的研究人员发现一种试验用药物可有效阻断SARS-CoV-2感染宿主所使用的细胞进入受体。这一发现有望开发出一种阻断这种新型冠状病毒早期感染的治疗方法。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Inhibition of SARS-CoV-2 infections in engineered human tissues using clinical-grade soluble human ACE2”。针对SARS-CoV-2及其在细胞水平上与宿主细胞相互作用的关键方面,以及这种病毒如何感染血管和肾脏,这项研究提供了新的见解。

图片来自Cell, 2020, doi:10.1016/j.cell.2020.04.004。
论文共同通讯作者、加拿大英属哥伦比亚大学生命科学研究所所长Josef Penninger教授说,“我们希望我们的结果对治疗这种史无前例的疫情的新型药物的开发产生影响。这项研究源于学术研究人员和公司之间的惊人合作,包括来自位于温哥华市的STEMCELL Technologies公司的Ryan Conder博士及其在胃肠道方面的研究团队、来自西班牙的Nuria Montserrat、来自多伦多市的Haibo Zhang博士和Art Slutsky博士,尤其是来自瑞典的Ali Mirazimi及其在传染生物学方面的研究团队。他们日夜不懈地工作了几个星期,旨在更好地了解这种疾病的病理和提供突破性的治疗选择。”
Slutsky博士说,“我们的新研究提供了极其需要的直接证据表明一种称为APN01(human recombinant soluble angiotensin-converting enzyme 2, 人重组可溶性血管紧张素转化酶2, 简称hrsACE2)的药物可作为一种抗病毒药物用于治疗COVID-19。欧洲生物技术公司Apeiron Biologics即将在临床试验中测试这种药物。”
在这项新研究分析的细胞培养物中,hrsACE2将SARS-CoV-2的病毒载量抑制了1000~5000倍。在由人干细胞培养出的人类血管和肾脏类器官中,这些研究人员证实这种病毒可以直接感染这些组织并在其中进行自我复制。这提供了有关这种疾病发展以及严重的COVID-19病例出现多器官衰竭和心血管损伤的重要信息。临床级hrsACE2还减少了这些体外培养出的人体组织中的SARS-CoV-2感染。
9.Science重磅!SARS-CoV-2的致命弱点或是其与SARS抗体的结合位点!
doi:10.1126/science.abb7269
Scripps研究所的科学家进行的一项研究显示,21世纪初从一名非典(SARS)幸存者身上发现的一种抗体揭示了最近这种导致COVID-19的新型冠状病毒的潜在弱点。
4月3日发表在Science杂志上的这项研究,首次以接近原子尺度的分辨率描绘了人类抗体与新型冠状病毒的相互作用。这种抗体是在SARS(严重急性呼吸系统综合症)感染时产生的,尽管SARS是由SARS-CoV病毒引起的,但它可以与新型冠状病毒SARS-CoV-2发生交叉反应。该 结构图谱揭示了抗体结合两个冠状病毒上几乎相同的位点,这表明该位点是冠状病毒家族重要的功能和易损位点。
"像这种位点保守的知识可以帮助对SARS-CoV-2疫苗和疗法基于结构的设计,而这些疗法也将防止其他可能出现在未来的冠状病毒,"这项研究的资深作者Ian Wilson说道,他是Scripps研究所计算生物学和综合结构系主任以及结构生物学的Hansen教授。
10.bioRxiv:科学家鉴别出抵御SARS-CoV-2感染的新型潜在药物靶点
doi:10.1101/2020.03.02.968388
近日,发表在预印版网站bioRxiv上的一篇研究报告中,来自加利福尼亚大学等机构的科学家们通过研究鉴别出了治疗SARS-CoV-2感染的新型潜在药物靶点;文章中,研究人员绘制出了两个关键SARS-CoV-2蛋白组成的复合体nsp10/16的原子结构,这两种蛋白能够修饰病毒 的遗传物质从而使其更像人类的RNA,这样就能促进病毒躲避宿主机体的抗病毒免疫机制并进行病毒复制。
研究者认为,如果有一种药物能抑制nsp10/16复合体的功能,那么宿主免疫系统或许就能检测到病毒并对其快速清除;研究者Godzik表示,我们首先设计出了一部分DNA来表达两种蛋白,随后对所产生的两种蛋白的结构进行分析;nsp10/nsp16蛋白复合体称之为RNA甲基转 移酶或MTase,其由于结合在一起的两种蛋白质组成,根据此前研究人员对SARS的研究,需要将这两部分结合在一起才能让蛋白复合体发挥作用。
研究者表示,他们需要多种药物来治疗SARS-CoV-2的感染,因为这种疾病会伴随人类很长一段时间,目前仅仅开发出一种药物是远远不够的,如果SARS-CoV-2对一种药物产生了耐受性,那么研究人员就需要开发出其它治疗性药物了。nsp15核酸内切酶、nsp3 ADP磷酸核糖 和nsp9复制酶,这三种蛋白质的结构对于病毒复制释放非常重要;如今研究人员绘制出了SARS-CoV-2的完整蛋白质结构体系,通过解决附加结构来扩大蛋白质结构的覆盖范围或许是后期科学家们的研究方向,第二个方向就是与潜在药物的共结晶实验,研究人员想知道冠 状病毒是如何与药物进行结合的,如果能解析清楚其中的机制,或能帮助研究者更高效地改进药物从而靶向作用SARS-CoV-2。
11.J Travel Med:ACE抑制剂和血管紧张素受体阻滞剂或会增加人群患严重COVID-19的风险
doi:10.1093/jtm/taaa041
近日,一项刊登在国际杂志Journal of Travel Medicine上的研究报告中,来自路易斯安那州立大学等机构的科学家们通过研究解释了为何某些被诊断为COVID-19的患者会出现严重的肺部并发症,相关研究结果或有望帮助开发治疗COVID-19的新型疗法。
2003年,SARS-CoV(SARSβ冠状病毒)引发了非典(严重急性呼吸综合征),如今SARS-CoV-2引发了COVID-19,SARS-CoV-2能与机体下呼吸道中的受体ACE2(血管紧张素转换酶2,angiotensin converting enzyme 2)结合从而进入到肺部,病毒性肺炎和可能致命的呼吸 衰竭会在10-14天后在易感人群中发生。
研究者Diaz表示,血管紧张素转换酶抑制剂(ACEIs)和血管紧张素受体阻滞剂(ARBs)是推荐给心血管疾病患者的常用药物,其能治疗包括心脏病、高血压、糖尿病和慢性肾脏疾病等多种人类疾病;其中许多患者均为老年人,医生通常会给其开具上述药物让患者每天服 用。
对实验性模型研究结果表明,当静脉输注ACE抑制剂后,机体呼吸系统中ACE2受体的数量会发生增加;由于利用ACEIs和ARBs治疗的患者的肺脏中ACE2受体的水平会增加,且能与冠状病毒S蛋白相互结合,因此患者会因遭遇SARS-CoV-2感染表现出严重疾病患病风险增加的状 况。
12.Nature:当COVID-19症状相对较轻时,患者较高水平地脱落病毒SARS-CoV-2
doi:10.1038/s41586-020-2196-x
在一项新的研究中,来自德国联邦国防军微生物研究所、慕尼黑施瓦宾格医院、柏林大学夏丽特医学院和慕尼黑大学医院的研究人员详细分析了来自德国慕尼黑的9名患上COVID-19呼吸道疾病且症状相对较轻的成年患者。这项研究表明冠状病毒SARS-CoV-2在这些患者的上 呼吸道中活跃复制,这表明患者在症状出现的第一周内可能较高水平地‘脱落’或者说排泄这种病毒。相关研究结果于2020年4月1日在线发表在Nature期刊上,论文标题为“Virological assessment of hospitalized patients with COVID-2019”。

图片来自Nature, 2020, doi:10.1038/s41586-020-2196-x。
论文共同通讯作者Christian Drosten及其同事们研究了9名诊断为COVID-19的中青年成年人的病毒脱落情况,这些患者因轻度上呼吸道症状在慕尼黑的一家医院接受治疗。他们分析了在临床治疗过程中从这些患者体内采集的喉部和肺部样本、痰液(即呼吸道粘液)、粪 便、血液和尿液。
这些作者发现在上呼吸道组织中SARS-CoV-2病毒复制水平较高,并且报告在症状发作的第一周内在上呼吸道中病毒脱落的水平也较高。他们都可以从这些患者体内采集的喉咙和肺部样本中分离出这种病毒的传染性形式,直到症状消失的第八天。其中的两名表现出一些早 期肺炎症状的患者持续在痰液中脱落较高水平的SARS-CoV-2直到症状消失的第十天或第十一天。在症状结束后,痰液中仍可检测到这种病毒的RNA。
血液和尿液样本中未检测到这种病毒,而且这些作者发现粪便样本中虽然存在较高浓度的病毒RNA,但是并未发现这种病毒的复制形式,这支持了它可能无法通过粪便传播的理论。但是,还需要在较大样本中进一步研究这种可能的传播途径。
13.万万没想到!研究下水道废水可以帮助对抗COVID-19疫情!
doi:10.1021/acs.est.0c01174
克兰菲尔德大学(Cranfield University)的研究人员正在研究一种新的检测方法,以检测感染了这种病毒的社区废水中的SARS-CoV-2。
基于废水的流行病学(WBE)方法可以通过收集进入下水道系统的疾病携带者的粪便和尿液中的生物标志物,为预测新型冠状病毒肺炎(COVID-19)的潜在传播提供一种有效和快速的方法。
使用基于纸张的设备的快速测试包可以在废水处理厂现场使用,以跟踪来源并确定在当地是否存在潜在的COVID-19载体。
克兰菲尔德水科学研究所传感器技术讲师Zhugen Yang博士说:"在社区或无症状感染的情况下当人们不知道他们是否被感染,通过简单的分析检测设备实时检测社区污水可以确定在一个地区有COVID-19的情况下支持快速筛查,隔离和预防。
14.Aging Dis:好消息!干细胞疗法有效对抗COVID-19肺炎
doi:10.14336/AD.2020.0228
当冠状病毒的消息出现时,Kunlin Jin博士和一组国际研究人员迅速联合起来对抗这种神秘的疾病。Jin博士说,"我们的研究表明,静脉输注临床级的人骨髓间充质干细胞是治疗COVID-19肺炎--包括老年重症肺炎患者的一种安全有效的方法。"
作为实验治疗的一部分,干细胞被静脉注射到北京的7名重症患者的血液中。研究称,三名患者被注射了安慰剂。
Jin博士说,接受检测的是北京佑安医院的病人。研究显示,检测从1月30日开始。Jin博士说,接受干细胞治疗的七名患者获得了成功,并在14天内出院。在接受安慰剂的患者中,一名死亡,一名病情严重,第三名患有急性呼吸窘迫综合征(ARDS)。
该研究小组的发现将发表在即将出版的2020年4月的《Aging and Disease》杂志上。这篇文章的标题是"Transplantation of ACE2-Mesenchymal Stem Cells Improves the Outcome of Patients with COVID-19 Pneumonia。"
15.bioRxiv:突破!合成多肽药物可以阻断SARS-CoV-2病毒与人类细胞结合
doi:10.1101/2020.03.19.999318
为了开发出治疗COVID-19的可能方法,麻省理工学院的一组化学家设计了一种候选药物,他们认为这种药物可以阻止冠状病毒进入人体细胞。这种潜在的药物是一种短的蛋白质片段,或肽段,它模仿一种在人类细胞表面发现的蛋白质。
研究人员已经证明,他们的新肽可以与冠状病毒用来进入人类细胞的病毒蛋白结合,从而有可能解除这种蛋白的武装。
"我们有我们真的想要探索的主要化合物,因为它事实上可以与病毒蛋白以一种我们预测的方式相互作用,所以它有机会抑制病毒进入宿主细胞,"领导该研究的麻省理工学院的化学副教授Brad Pentelute说道。
麻省理工学院的研究小组在3月20日发布在bioRxiv(一个在线预印本服务器)上的预印本中报告了他们的初步发现。他们已经将肽的样品寄给了计划在人体细胞中进行试验的合作者。
16.Ophthalmology:新型冠状病毒通可以通过眼泪传播?
doi:10.1016/j.ophtha.2020.03.026
虽然研究人员确定冠状病毒是通过咳嗽或打喷嚏排出的粘液和飞沫传播的,但目前还不清楚这种病毒是否通过其他体液传播,比如眼泪。最新发表的研究提供了证据,表明受感染的病人不太可能通过眼泪传播病毒,但有一个重要的警告。在这项研究中,没有一个病人患 有结膜炎,也被称为粉红眼。然而,卫生官员认为,只有1%到3%的冠状病毒感染者会出现粉红色眼睛。该研究的作者得出结论,他们的发现,加上感染患者中粉红色眼睛的发病率较低,表明通过眼泪传播病毒的风险较低。他们的研究发表在《眼科学》(Ophthalmology)杂 志网络版上,该杂志是美国眼科学会(American Academy of Ophthalmology)的期刊。

图片来源:https://cn.bing.com。
为了进行这项研究,新加坡国立大学医院的临床医学学士Ivan Seah和他的同事收集了17名COVID-19患者的眼泪样本,从他们出现症状到大约20天后恢复。无论是病毒培养还是逆转录聚合酶链反应(RT-PCR)都没有在患者的眼泪中检测到病毒。
在同一时期,Seah博士还从鼻子后部和喉咙处取样。虽然病人的眼泪里没有病毒,但他们的鼻子和喉咙里却充满了病毒。Seah博士说,他希望他们的工作有助于指导更多的研究,防止病毒通过更重要的途径传播,如飞沫和粪便-口腔传播。
17.重磅!两篇Nature揭示SARS-CoV-2结合ACE2受体的晶体结构
doi:10.1038/s41586-020-2180-5; doi:10.1038/s41586-020-2179-y
一种新型高致病性冠状病毒(SARS-CoV-2)自2019年12月以来肆掠全球,应对这一疫情的关键是了解病毒的受体识别机制,调节其感染性、发病机制和宿主范围。而在分子和原子水平了解SARS-CoV-2如何感染细胞有利于科学家们更快开发出更有效地预防或者治疗性药物。
3月30日,Nature杂志在线发表了两项最新研究,揭示了SARS-CoV-2识别和结合人ACE2的机制及形成的复合物的晶体结构,两项研究分别为清华大学王新泉课题组和张林琦课题组合作发表的"Structure of the SARS-CoV-2 spike receptor-binding domain bound to the ACE2 receptor"以及明尼苏达大学李放教授课题组发表的"Structural basis of receptor recognition by SARS-CoV-2"。
为了在原子水平上更好地理解感染的初始步骤,我们王新泉课题组和张林琦课题组以2.45 A的分辨率确定了与细胞受体ACE2结合的SARS-CoV-2 刺突蛋白受体结合域(spike receptor binding domain,RBD)的晶体结构。SARS-CoV-2 RBD和ACE2的整体结合模式与SARS-CoV RBD几乎相同,后者也利用ACE2作为细胞受体。研究人员在SARS-CoV-2 RBD中结构分析发现了对ACE2结合至关重要的残基,其中大部分要么高度保守,要么与SARS-CoV RBD中的残基具有类似的侧链性质。研究人员发现虽然SARS-CoV-2不会在SARS和SARS相关的冠状病毒中聚 集,但这种结构和序列上的相似性有力地证明了SARS-CoV-2和SARS-CoV RBDs之间的趋同进化可以改善它们与ACE2的结合。研究人员还分析了以RBD为靶点的两种SARS-CoV抗体的表位,为今后交叉反应性抗体的鉴定提供了思路。
在另一项研究中,李放教授课题组确定了与hACE2配合物中SARS-CoV-2受体结合域(RBD)的晶体结构(利用一种可以促进结晶的工程化RBD)。研究人员发现与SARS-CoV RBD相比,在SARS-CoV-2 RBD中,hACE2的结合具有更紧密的构象;此外,SARS-CoV-2 RBD中的几个残基变 化稳定了RBD/hACE2界面上的两个病毒结合热点。SARS-CoV-2 RBD的这些结构特征增强了其与hACE2的结合亲和力。此外,研究人员还发现与SARS-CoV-2密切相关的蝙蝠冠状病毒RaTG13也使用hACE2作为其受体。在hACE2识别中,SARS-CoV-2、SARS-CoV和RaTG13的差异揭示 了SARS-CoV-2在动物和人类之间潜在的传播途径。本研究为SARS-CoV-2靶向受体识别的干预策略提供指导。
总的来说,这两项研究利用X光晶体衍射技术,揭示了SARS-CoV-2与ACE2结合的微观晶体结构,有助于科学家了解ACE2受体介导的SARS-CoV-2识别和感染细胞的过程,可以加快科学家开发治疗性药物和疫苗的进程。
18.Nat Commun:利用新的RNA成像技术开发的冠状病毒检测试剂盒
doi:10.1038/s41467-020-14932-7
西蒙弗雷泽大学的研究人员将使用他们的先进成像技术--Mango(因为它明亮的颜色)--来开发冠状病毒测试工具。他们是对加拿大卫生研究院(CIHR)最近宣布的帮助解决COVID-19的快速资助机会做出反应的一小部分加拿大研究人员之一。
SFU的博士后研究员Lena Dolgosheina和分子生物学和生物化学教授Peter Unrau开发出了Mango,可以敏感地检测RNA分子,帮助改善病毒对病毒的筛选,如冠状病毒,同时使细胞功能的基本发现成为可能。由Unrau领导的最新研究涉及到使用Mango来检测活细胞内的单个 RNA分子。
Unrau说:"我们是由分子组成的,所以当一个细胞出了问题,它就会发生在分子水平上。我们正在利用Mango系统作为催化剂,使我们不仅能够扩展基础研究问题,而且能够更快、更有效地检测冠状病毒等病原体。"
Mango系统由RNA Mango适配体组成,该适配体可以与荧光染料紧密结合。该适配体的作用类似于磁靶向并结合那些染料分子。染料一接触就会兴奋起来,发出明亮的光芒。经过修饰以包含适配体"磁铁"的RNA分子可以从细胞的其他部分中脱颖而出,这使得研究人员更容易 在显微镜下观察和研究RNA分子。
19.Cell:我国科学家从结构和功能角度揭示SARS-CoV-2利用人ACE2进入细胞机制
doi:10.1016/j.cell.2020.03.045
病毒感染始于病毒颗粒与宿主表面细胞受体的结合。因此,受体识别是病毒的细胞和组织嗜性(tropism)的一个重要决定因素。此外,病毒结合其他物种的相应受体的功能获得也是物种间传播的先决条件。有趣的是,除了HCoV-OC43和HKU1均与糖分子结合从而与细胞附 着外,其他的四个人类冠状病毒均将蛋白肽酶识别为受体。HCoV-229E与人氨基肽酶N(hAPN)结合,而MERS-CoV与人二肽基肽酶4(hDPP4或hCD26)相互作用。尽管SARS-CoV和hCoV-NL63属于不同的冠状病毒属,但是它们均与人类血管紧张素转化酶2(hACE2,即人ACE2) 相互作用以进入宿主细胞。在COVID-19疫情爆发后,中国科学家迅速确定SARS-CoV-2也利用hACE2进入细胞。
在冠状病毒中,这种进入过程是由嵌入包膜的位于病毒表面的刺突糖蛋白(S蛋白)介导的。在大多数情况下,S蛋白会被宿主蛋白酶切割为分别负责受体识别和膜融合的S1和S2亚基。 S1可以进一步分为N末端结构域(NTD)和C末端结构域(CTD),两者都可以充当受体结 合实体(比如,SARS-CoV和MERS-CoV都利用S1 CTD识别受体,因而称为受体结合结构域(RBD),然而小鼠肝炎冠状病毒利用它的S1 NTD与受体结合。在此之前,SARS-CoV-2 S蛋白中负责与hACE2相互作用的区域仍然是未知的。
在一项新的研究中,来自中国科学院、深圳市第三人民医院、山西农业大学、安徽大学、四川大学、中国科技大学和香港大学的研究人员利用免疫染色和流式细胞仪测定技术,首先鉴定出S1 CTD(SARS-CoV-2-CTD)是SARS-CoV-2中与hACE2受体相互作用的关键区域。他们 随后解析出SARS-CoV-2-CTD与hACE2结合在一起时的分辨率为2.5 ?的晶体结构,揭示了一种整体上与SARS-CoV RBD(下称SARS-RBD)相类似的受体结合模式。但是,与SARS-RBD相比,SARS-CoV-2-CTD与hACE2形成更多的原子相互作用,这与显示更高的受体结合亲和力的数 据相关。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Structural and functional basis of SARS-CoV-2 entry by using human ACE2”。
值得注意的是,一组单克隆抗体(mAb)以及针对SARS-S1/RBD的鼠多克隆抗血清无法与SARS-CoV-2 S蛋白结合,这表明SARS-CoV和SARS-CoV在抗原性上存在显著差异,并且提示着先前开发的基于SARS-RBD的候选疫苗不太可能对SARS-CoV-2预防有任何临床益处。
20.全文编译!复旦大学在Cell期刊上发文,从基因组学角度揭示SARS-CoV-2的起源和出现
doi:10.1016/j.cell.2020.03.035
新型人类冠状病毒SARS-CoV-2(之前称为2019-nCoV)的持续大流行引起了全球的极大关注。我们和中国的其他人参与了对这种病毒的初始基因组测序。在本文中,我们描述了针对SARS-CoV-2的出现,这些基因组数据揭示了什么,并讨论了我们对其起源理解上所存在的差 距。
在英国爱丁堡大学Andrew Rambaut博士的帮助下,我们于2020年1月11日(格林威治标准时间, GMT)早些时候在开放存取的virological.org网站(http://virological.org/)上发布了这种病毒的基因组序列。不久之后,中国疾控中心在公众可访问的GISAID数据库 (https://www.gisaid.org/)上类似地发布了SARS-CoV-2基因组序列(以及相关的流行病学数据)。在撰写本文时,已有近200个SARS-CoV-2基因组可公开获得,这代表了来自中国及其他地区的这种病毒的基因组多样性,并提供了可自由获取的全球资源。重要的是, SARS-CoV-2基因组序列数据的发布促进了诊断测试和感染性克隆(infectious clone)的快速开发。研发有效疫苗和抗病毒药物的竞赛正在进行中,而且针对抗病毒药物的临床试验正在逐步展开。
尽管SARS-CoV和MERS-CoV与SARS-CoV-2密切相关并且都有蝙蝠宿主,但这两种病毒之间的生物学差异却很明显。如上所述,SARS-CoV-2的传染性明显更高,从而导致与SARS-CoV和MERS-CoV完全不同的流行病学动态。在后两种病毒中,病例数的增长相对较慢,而MERS-CoV 从未完全适应人类传播:大多数病例是由于阿拉伯半岛的骆驼溢出造成的,仅零星地发生人与人之间的传播。相比之下,SARS-CoV-2在当地的显著传播最让人吃惊。确定支撑这种传播能力的病毒学特征显然是当务之急。
SARS-CoV-2似乎将不可避免地成为人类中的第五种地方性冠状病毒(其他四种为HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1),并且目前正在完全易感人群中传播。冠状病毒显然具有跨越物种界限并适应新宿主的能力,这使得预测未来会有更多的病毒出现变得很简 单,不过尚不清楚为何相比于一些其他的RNA病毒,冠状病毒具有这种能力。至关重要的是,对动物冠状病毒的监视应包括蝙蝠以外的动物,这是因为中间宿主的作用可能非常重要,从而为病毒在人类中的出现提供了更直接的途径。
鉴于野生动物中病毒的多样性以及它们的持续进化,可以说,降低未来疫情爆发风险的最简单最具成本效益的方法是尽可能限制我们对动物病原体的接触。尽管我们与动物世界的亲密关系意味着我们无法建立坚不可摧的屏障,但是针对非法野生动物贸易采取更强有力的 行动,以及将所有野生哺乳动物(也许还有禽类)从湿货市场中清除将提供一个重要的缓冲。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


