厦大Nature:基因不稳定导致肠道干细胞坏死诱发肠道炎症
来源:本站原创 2020-04-04 09:28
2020年4月4日讯 /生物谷BIOON /——炎症性肠病(infammatory bowel disease,IBD)的病因包含遗传和环境之间的多因素相互作用导致。近日来自厦门大学细胞应激生物学国家重点实验室、生命科学学院莫玮教授课题组和韩家淮院士课题组合作在Nature杂志上发文揭示了肠道干细胞中基因组不稳定性引发干细胞坏死,导致自发性的肠道炎症的机制,改
2020年4月日4讯 /生物谷BIOON /——炎症性肠病(infammatory bowel disease,IBD)的病因包含遗传和环境之间的多因素相互作用导致。近日来自厦门大学细胞应激生物学国家重点实验室、生命科学学院莫玮教授课题组和韩家淮院士课题组合作在Nature杂志上发文揭示了肠道干细胞中基因组不稳定性引发干细胞坏死,导致自发性的肠道炎症的机制,该文章题为"Gut stem cell necroptosis by genome instability triggers bowel inflammation",研究人员发现了一种组蛋白甲基转移酶SETDB1的缺失,会介导赖氨酸9处组蛋白H3的三甲基化,从而参与IBD的发病机制。
图片来源:Nature
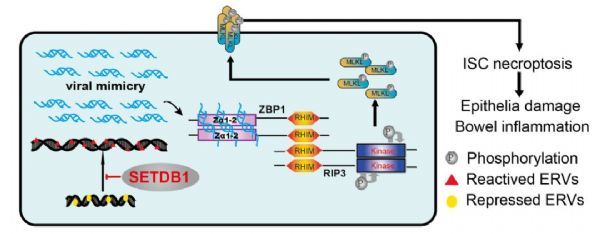
研究人员发现,IBD患者的SETDB1水平下降,而肠道干细胞中SETDB1水平下降的小鼠会发生自发性末端回肠炎和结肠炎。SETDB1保护了基因组的稳定性,肠干细胞中SETDB1的缺失释放了对内源性逆转录病毒的抑制(在人类中,长时间重复的类似逆转录病毒的元素约占基因组的8%)。
研究人员发现内源性逆转录病毒引起的过度病毒拟态触发了z-DNA结合蛋白1 (ZBP1)依赖性的坏死,不可逆转地破坏了上皮屏障的稳态,最终促进了肠道炎症。在IBD患者中均可见到基因组不稳定、内源性逆转录病毒反应、ZBP1上调和坏死。
研究人员还发现使用药物抑制RIP3对setdb1缺陷小鼠有治疗效果,这提示靶向肠干细胞坏死可能是治疗严重IBD的一种方法。(生物谷Bioon.com)
参考资料:
Wang, R., Li, H., Wu, J. et al. Gut stem cell necroptosis by genome instability triggers bowel inflammation. Nature (2020). https://doi.org/10.1038/s41586-020-2127-x
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->