北京大学钟超团队发现PD-1信号通过调节LTi细胞功能促进肠道稳态
来源:生物世界 2022-07-07 20:24
PD-1/PD-L1 抑制剂目前已被 FDA 批准应用于包括恶性黑色素瘤、非小细胞肺癌、肝癌、胃癌、头颈癌等二十余种癌症的治疗,较传统治疗取得较好效果。
PD-1/PD-L1 抑制剂目前已被 FDA 批准应用于包括恶性黑色素瘤、非小细胞肺癌、肝癌、胃癌、头颈癌等二十余种癌症的治疗,较传统治疗取得较好效果。然而,PD-1/PD-L1 阻断,往往伴随免疫相关副作用(immune-related adverse events,irAEs),严重者导致免疫治疗中断。
肠炎作为 PD-1/PD-L1 抑制剂治疗过程中的常见 irAEs,其发生机制至今尚不清楚。因此,深入探讨 PD-1 信号对肠道稳态的调控作用,有利于对 PD-1 抑制剂肿瘤治疗过程中副反应的防护。
2022年7月4日,北京大学钟超课题组在 Nature 子刊 Nature Metabolism 在线发表了题为:
该研究发现,PD-1 信号通过限制淋巴组织诱导细胞(Lymphoid tissue inducer,简称LTi)活化过程中脂肪酸氧化促进其免疫效应功能,从而维持肠道稳态,缓解肠道炎症。

首先,研究者发现 PD-1 基因(PDCD1)缺失会导致小鼠肠道菌群紊乱、肠炎易感,重复了肿瘤免疫治疗中 PD-1 抑制剂引起肠炎发生的临床现象。LTi 是富集于哺乳动物肠道的一群天然免疫细胞,通过分泌效应细胞因子 IL-22 对维持肠道稳态具有重要作用。
研究团队发现 PD-1 分子在结肠 LTi 细胞上高水平表达,然而,其信号是否对 LTi 的功能存在调控作用仍未见报道。利用 LTi 细胞 PDCD1 缺失的条件性敲除小鼠,研究团队证明 PD-1 信号通过促进 LTi 细胞分泌 IL-22,对维持肠道稳态、减缓肠炎发生具有重要作用。
机制上,研究团队利用单细胞测序(scRNA-seq)、细胞能量代谢检测等技术,发现LTi细胞活化过程中会发生脂合成及糖代谢增强的代谢重编程,而 PD-1 信号缺失导致活化 LTi 细胞脂肪酸氧化(FAO)水平异常增高,进而抑制其 IL-22 的表达。据此,研究团队利用 Etomoxir 等 FAO 抑制剂或通过构建 LTi 细胞 FAO 限速酶 Cpt1 的条件性敲除小鼠,均有效恢复了 PD-1 信号缺失 LTi 中的 IL-22 表达。
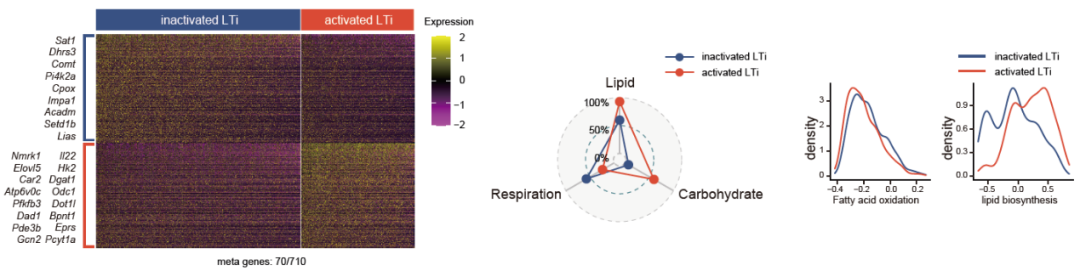
单细胞测序分析LTi细胞活化过程的代谢重塑
总而言之,该研究揭示了 PD-1 信号调控肠道 LTi 细胞活化过程中的代谢重编程,从而促进其发挥免疫效应功能,维持肠道稳态。同时,该研究也为 PD-1 抑制剂治疗过程中出现的肠炎副反应提供了一种可能的解释,为针对性治疗提供了参考策略。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


