Nature子刊:梁毅/刘聪合作揭示渐冻症致病蛋白质SOD1构象转化分子机制
来源:生物世界 2022-06-23 15:40
该研究首次在原子水平上揭示了 SOD1 由生理型向病理型结构转变的机制,启示不同的病理突变体在调节 SOD1 构象转化中可能发挥着不同的作用,并使得发展新的基于 SOD1 纤维结构的 ALS 治疗药物
武汉大学梁毅教授团队和中国科学院上海有机所交叉中心刘聪研究员团队合作,在 Nature Communications 期刊发表了题为:Cryo-EM structure of an amyloid fibril formed by full-length human SOD1 reveals its conformational conversion 的研究论文。
该研究率先解析了铜锌超氧化物歧化酶(SOD1)纤维的高分辨率冷冻电镜结构,揭示了渐冻症(ALS)致病蛋白质 SOD1 构象转化分子机制,为发展新的基于 SOD1 纤维结构的 ALS 治疗药物奠定了基础。
肌萎缩侧索硬化症(Amyotrophic lateral sclerosis,ALS)又称渐冻症,是一种进行性的、致命的神经退行性疾病,其主要症状表现为运动皮层、脑干以及脊髓中的上、下运动神经元进行性的退化,它们的退化伴随而来的是肌无力、肌肉萎缩导致的瘫痪,以及最终因为呼吸衰竭而导致的死亡。SOD1 和 TAR DNA 结合蛋白43(TDP-43)在中枢神经系统的运动神经元形成纤维样聚集体是 ALS 的重要病理特征之一。
SOD1 主要位于细胞质中,也存在于细胞核和线粒体膜间隙中,是真核细胞抵抗活性氧(ROS)的抗氧化应激酶系中的重要成员,SOD1 是最早被鉴定出与家族遗传型 ALS 相关的致病基因。随着年龄的增大,细胞中特别是 SOD1 半衰期较长的运动神经元细胞中,SOD1 受到损伤的风险增大,极易发生病变,造成 ALS 等相关神经退行性疾病。
在野生型朊蛋白及其病理突变体 E196K 淀粉样纤维冷冻电镜结构及功能前期工作(2020年6月8日和2021年9月9日分别发表于 Nat. Struct. Mol. Biol. 2020, 27, 598-602)和 Sci. Adv. 2021, 7, eabg9676)中,梁毅与刘聪团队合作解析了全长野生型朊病毒蛋白纤维和全长 E196K 纤维的结构,首次在原子水平上揭示了朊蛋白由细胞型朊蛋白(PrPC)向病理型朊病毒蛋白(PrPSc)结构转变的机制,揭示了朊病毒蛋白病理聚集多态性的分子机制。SOD1 是一种类朊病毒蛋白,然而非常稳定的天然 SOD1 蛋白到底是怎么转化为具有致病结构的 SOD1 的仍是困扰科学界的谜题。
“冷冻电镜(Cryo-EM)技术为蛋白质错误折叠与疾病带来革命性的进展,解析全长 SOD1 纤维的高分辨率结构将为理解 ALS 的发病机制起到极大的推动作用。”论文作者指出。
但迄今为止,由于 SOD1 纤维的不溶性和异质性,仍无高分辨率的全长 SOD1 纤维的结构,极大地限制了基于 SOD1 纤维结构的 ALS 治疗药物的研发。
梁毅介绍,为了阐释 SOD1 由生理型向病理型转变的结构基础,在这项研究中,研究人员制备了高度均一的全长人 SOD1 淀粉样纤维,发现这些纤维具有显著的细胞毒性,能够诱导细胞内的线粒体功能紊乱,并运用冷冻电镜结合三维重构技术在原子水平上解析了全长 SOD1 纤维的高分辨率结构(2.95 Å),发现 SOD1 纤维由单股原纤维以左手螺旋的方式缠绕而成,纤维宽度为12.3 nm,纤维核心直径是11 nm,半个螺旋周期为73.1 nm。纤维核心的疏水氨基酸侧链向内折叠形成5个疏水空腔,起到了稳定淀粉样纤维结构的作用。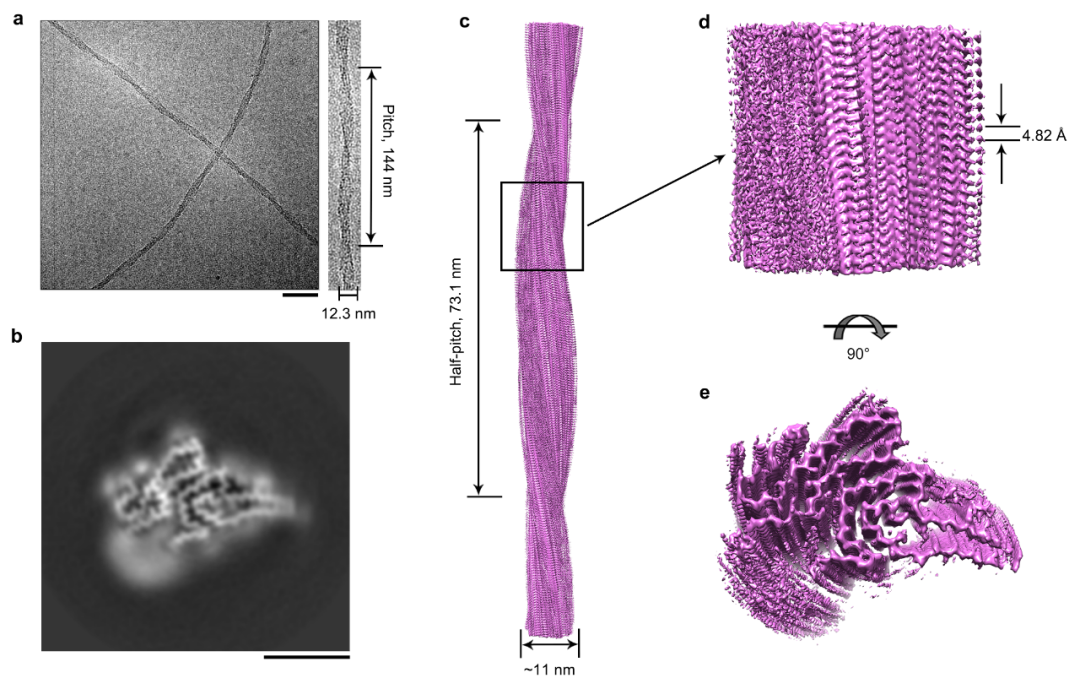 图1:全长人SOD1纤维的冷冻电镜结构
图1:全长人SOD1纤维的冷冻电镜结构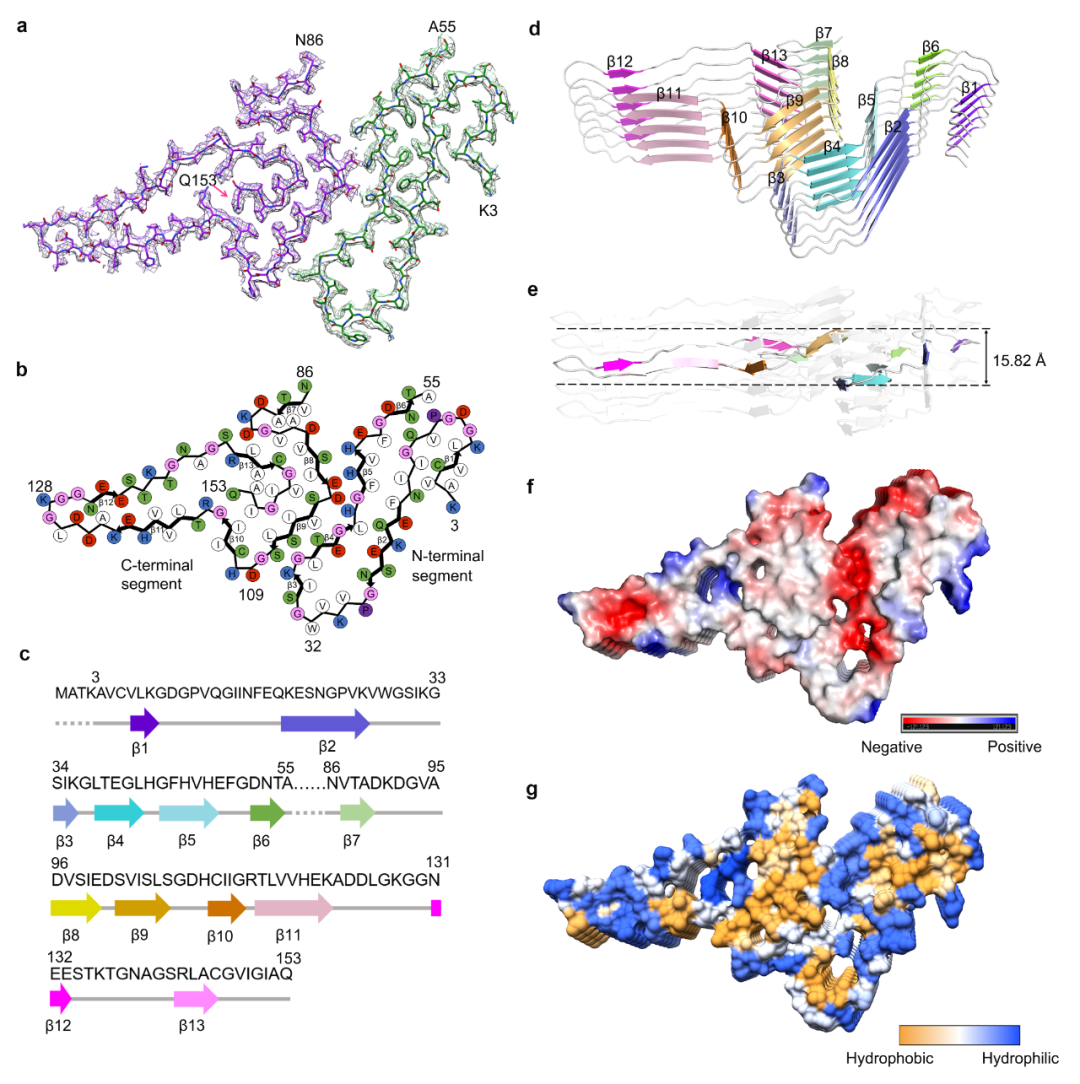 图2:全长人SOD1纤维的原子结构模型
图2:全长人SOD1纤维的原子结构模型
进一步研究发现,SOD1 纤维核心由其 N 端的3-55区域和 C 端的86-153区域组成,而且这两个区域主要通过 Lys36 和 Asp109 之间、His43 和 Asp101 之间以及 His46 和 Glu100 之间形成的3对盐桥紧密结合在一起。
对于这样新奇的结构,研究人员对于其病理学意义进行了探索,发现在 SOD1 纤维结构中形成盐桥的五个关键氨基酸残基 His43、His46、Glu100、Asp101 和 Asp109 都是与 ALS 相关联的病理突变位点。
通过比较脱辅基 SOD1 二聚体结构,研究人员提出,在 SOD1 错误折叠过程中,脱辅基 SOD1 亚基的一个α-螺旋和由8个β-折叠组成的β-桶状结构转变成 SOD1 纤维的13个β-折叠结构。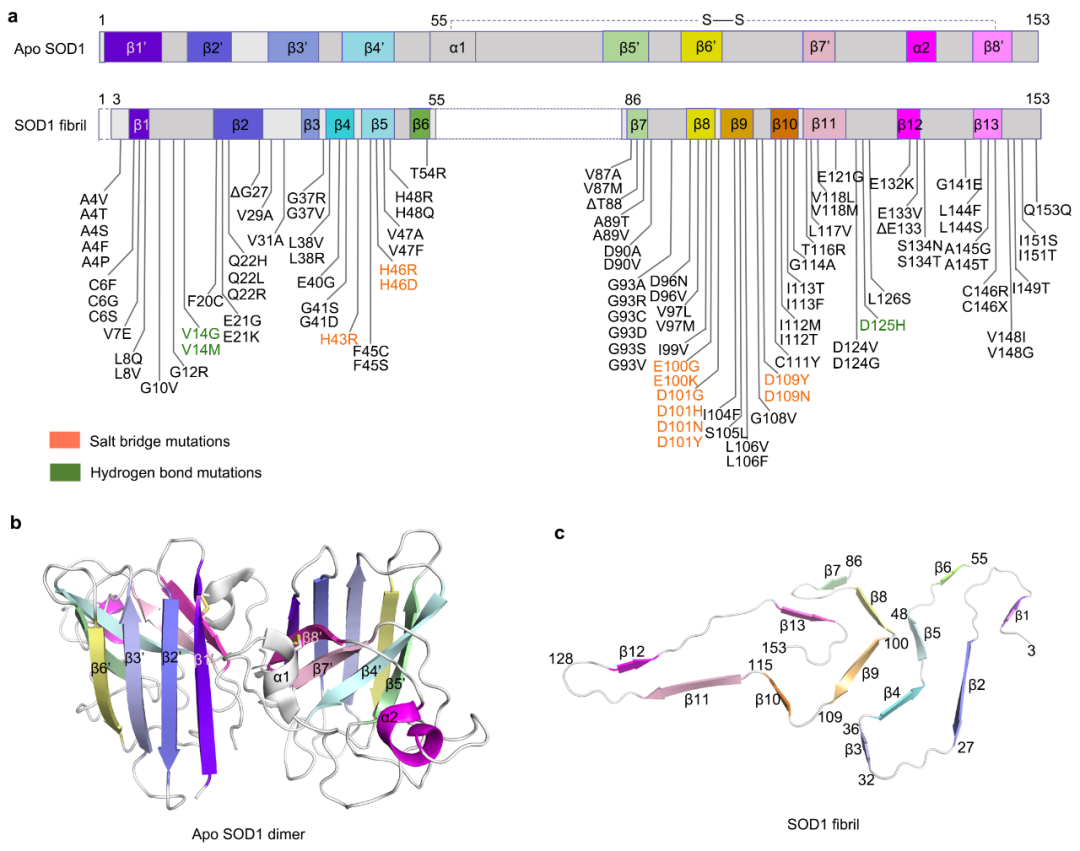
图3:脱辅基人SOD1二聚体和SOD1纤维结构比较
该研究首次在原子水平上揭示了 SOD1 由生理型向病理型结构转变的机制,启示不同的病理突变体在调节 SOD1 构象转化中可能发挥着不同的作用,并使得发展新的基于 SOD1 纤维结构的 ALS 治疗药物成为可能,为 SOD1 聚集体结构与致病功能的深入研究奠定了分子基础。
武汉大学生命科学学院梁毅教授和中国科学院上海有机所交叉中心刘聪研究员为该论文的共同通讯作者;武汉大学生命科学学院博士后王利强、中国科学院上海有机所交叉中心博士生马烨阳和武汉大学生命科学学院博士生袁菡烨为共同第一作者;华中农业大学生命科学技术学院殷平教授、中国科学院上海有机所交叉中心博士生赵焜和武汉大学土木建筑工程学院王正直副教授等参与了该论文的研究工作。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


