Cell子刊:杨玲团队揭示肥胖导致非酒精性脂肪肝病进展的新机制
来源:生物世界 2024-05-11 11:16
本研究的发现提供了肥胖导致下丘脑细胞功能缺陷以及下丘脑-肝脏内质网应激通讯在NAFLD进展中的病理生理作用的第一个证据和机制。
肥胖会改变控制肝脏免疫代谢稳态的下丘脑激素水平,而下丘脑功能紊乱会导致非酒精性脂肪肝病(NAFLD)。但肥胖对下丘脑稳态的具体影响目前尚不清楚。
2024年5月7日,爱荷华大学杨玲团队在 Cell Metabolism 期刊发表了题为:Obesity disrupts the pituitary-hepatic UPR communication leading to NAFLD progression 的研究论文。
该研究表明,肥胖会破坏垂体-肝脏未折叠蛋白反应(UPR)通讯,导致非酒精性脂肪肝病(NAFLD)进展。

在这里,我们发现肥胖小鼠和人类的下丘脑中存在着不明显的未折叠蛋白反应(UPR)和升高的炎症标志物。此外,我们发现肥胖会引发下丘脑炎症,导致下丘脑IRE1α-XBP1 UPR分支受损,这一分支对于保护下丘脑内分泌功能和防止NAFLD进展至关重要。令人惊讶的是,下丘脑IRE1α缺失会导致甲状腺功能减退,并抑制肝脏中由THRB介导的Xbp1激活。相反,激活肝脏中的THRB-XBP1轴可以改善下丘脑UPR缺陷小鼠的NAFLD。我们的研究提供了肥胖导致的下丘脑细胞缺陷的首个证据和NAFLD进展中下丘脑-肝脏UPR通讯的病理生理作用。
垂体是控制全身激素、炎症、代谢和能量稳态的中枢内分泌器官,在肥胖中,所有这些都会被破坏,而肥胖是非酒精性脂肪肝病(NAFLD)的主要风险因素。
值得注意的是,下丘脑功能减退、生长激素缺乏和甲状腺功能减退患者中非酒精性脂肪性肝病(NAFLD)的患病率较高。众所周知,垂体激素的分泌受下丘脑神经内分泌输入信号的控制,肥胖相关的下丘脑细胞功能障碍导致肝脏糖脂代谢缺陷。然而,肥胖对垂体的直接影响目前仍知之甚少。垂体有自己的自主调控程序,并根据发育和生理挑战进行动态重编程。目前,肥胖背景下的垂体细胞可塑性尚不清楚,并且NAFLD进展中垂体依赖性机制的直接证据有限。
高达70%的垂体质量由专职分泌细胞组成,这些分泌细胞需要完整的内质网(ER)功能来支持大量分泌激素的需求。内质网稳态的紊乱引起内质网应激(ER Stress),激活未折叠蛋白反(UPR)以恢复正常的内质网功能。不能启动这种适应反应以减轻内质网应激会导致其他内分泌细胞异常,例如胰岛β细胞的胰岛素分泌受损。
垂体激素产生的动力学与营养状态密切相关,肥胖是一种适应不良的营养调节状态,可能通过内质网(ER)直接影响垂体功能。然而,肥胖是否以及在多大程度上损害垂体的未折叠蛋白反应(UPR),以及其直接功能意义尚不清楚。
在肝脏中,未能激活UPR的适应性以恢复ER稳态是NAFLD中脂肪变性、胰岛素抵抗和炎症发病的一个主要因素。虽然损害保护性肝脏UPR的机制尚不清楚,但通过化学或分子伴侣减轻内质网应激可改善肥胖小鼠和人类的代谢控制和胰岛素敏感性。
研究表明,肝脏UPR感知内分泌输入,从而调节肝脏细胞和代谢程序。例如,在NAFLD的情况下,胰高血糖素和肾上腺素信号通过分解代谢激活肝脏适应性UPR可改善被破坏的内质网功能。然而,异常垂体激素输出是否以及在多大程度上促进了有缺陷的肝脏UPR诱导的NAFLD进展,这一点在很大程度上尚不清楚。
生物体通过协调细胞、组织和器官之间的应激反应来适应和应对环境挑战。然而,UPR在整个生物体的器官/组织之间传递压力的调节机制尚不完全清楚,特别是在肥胖相关病理的背景下。在这项研究中,研究团队提供了内分泌介导的垂体-肝脏UPR在NAFLD背景下的相互作用的第一个见解。
具体来说,该研究发现,肥胖小鼠和人类的下丘脑存在受抑制的未折叠蛋白反应(UPR)和升高的炎症标志物。该研究还发现肥胖会引发下丘脑炎症,导致下丘脑IRE1α-XBP1 UPR分支受损,这对保护下丘脑内分泌功能和阻止NAFLD进展至关重要。
值得注意的是,下丘脑IRE1敲除会导致甲状腺功能减退,并抑制肝脏中由THRB介导的Xbp1激活。相反,激活肝脏中的THRB-XBP1轴改善了下丘脑UPR缺陷小鼠的NAFLD。
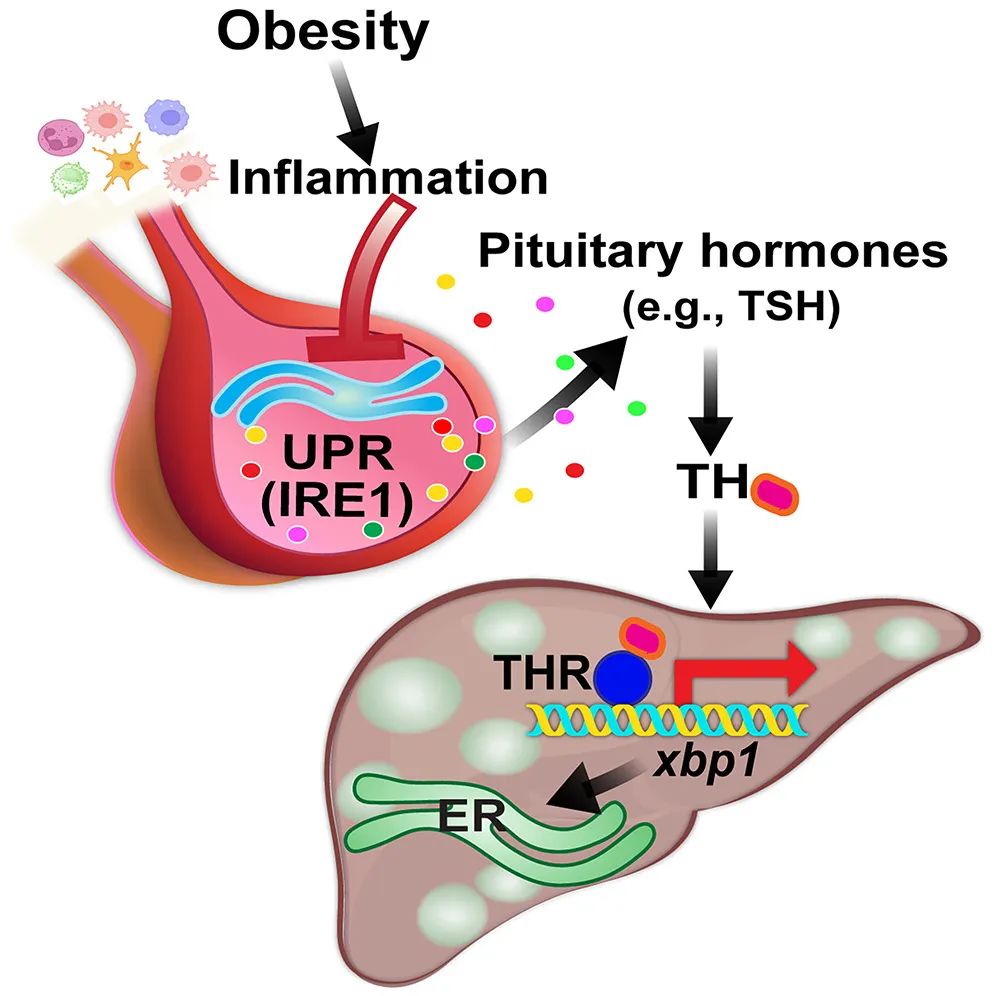
这些发现提供了肥胖导致下丘脑细胞功能缺陷以及下丘脑-肝脏内质网应激通讯在NAFLD进展中的病理生理作用的第一个证据和机制。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


