15价肺炎疫苗!默沙东Vaxneuvance获欧盟CHMP建议批准:用于6周龄-18岁以下人群!
来源:生物谷原创 2022-09-22 17:02
今年6月,Vaxneuvance获得美国FDA批准,成为近十年来第一种获批的儿科肺炎球菌结合疫苗,将帮助儿童群体免受IPD影响。
图片来源:摄图网
2022年09月22日讯 /生物谷BIOON/ --默沙东(Merck & Co)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一份积极审查意见,建议批准Vaxneuvance(15价肺炎球菌结合疫苗,V114):用于6周龄至18岁以下的婴儿、儿童、青少年群体,进行主动免疫接种,以预防由15种血清型肺炎链球菌引起的侵袭性疾病、肺炎和急性中耳炎。在欧盟,Vaxneuvance先前已被批准用于18岁及以上成年人群。现在,CHMP的意见将递交至欧盟委员会(EC)审查,后者预计将在今年年底做出最终审查决定。
Vaxneuvance是一款15价疫苗,由来自15种血清型(1、3、4、5、6A、6B、7F、9V、14、18C、19A、19F、22F、23F、33F)肺炎球菌多糖与CRM197载体蛋白结合而成,包括22F和33F血清型,这2种血清型通常与全球范围内的IPD有关。
在美国监管方面,Vaxneuvance于2021年7月获得FDA批准,用于18岁及以上成人群体,进行主动免疫接种,预防由上述15种肺炎链球菌血清型引起的侵袭性肺炎球菌病(IPD)。2022年6月,Vaxneuvance获得FDA批准扩大适应症:用于6周龄至17岁的儿童群体。随着这项扩大适应症,Vaxneuvance是近十年来美国第一种获批的儿童肺炎球菌结合疫苗,将帮助儿童群体免受IPD的影响。此前,美国FDA已授予Vaxneuvance突破性药物资格(BTD),用于6周至18岁以下儿科人群、18岁及以上成年人群,预防由疫苗血清型引起的IPD。
图片来源:摄图网
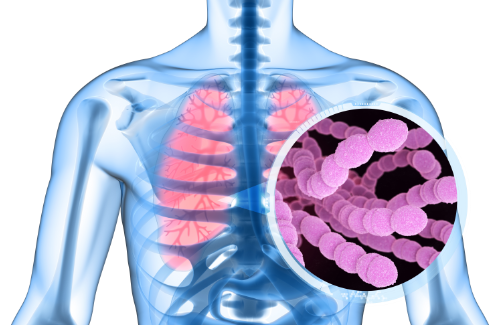
肺炎球菌病是一种由肺炎链球菌引起的感染。这种细菌的不同菌株称为血清型。当肺炎链球菌入侵身体通常不存在细菌的部位时,就会发生侵袭性肺炎球菌病(IPD)。尽管有大约100种不同的血清型,但儿童IPD的致病血清型较少。血清型3、22F、33F是导致儿童IPD病例的前5种血清型中的3种。IPD可导致住院或死亡。IPD的一些例子包括菌血症(血液感染)和脑膜炎(脑脊髓膜感染),这会导致长期的神经并发症。2岁以下的儿童尤其容易感染IPD。
在美国和欧盟,针对儿科人群适应症,FDA的批准和CHMP的积极审查意见,分别基于7项、8项随机、双盲临床研究的数据。这些研究评估了Vaxneuvance在婴儿、儿童、青少年中的安全性、耐受性和免疫原性。来自关键性研究的临床数据表明,根据血清型特异性免疫球蛋白G(IgG)几何平均浓度(GMC)测定结果,针对13种共有血清型,Vaxneuvance在四剂儿科方案接种后引发的免疫反应不低于目前可用的13价肺炎球菌结合疫苗(PCV13)。此外,针对重要致病性共有血清型3和Vaxneuvance特有的2种血清型22F和33F,Vaxneuvance在四剂儿科方案接种后引发的免疫反应优于PCV13。
来自临床项目的数据也支持Vaxneuvance与其他常用常规儿科疫苗同时使用,以及在各种临床环境中使用,例如,在启动婴儿PCV13疫苗接种计划后将Vaxneuvance作为可互换疫苗使用,或在未接种肺炎球菌疫苗或之前接受另一种PCV不完整接种方案的较大儿童人群中将Vaxneuvance用于疫苗补种(catch-up)。此外,数据支持在特殊人群中使用Vaxneuvance,例如早产儿和感染HIV或患有镰状细胞病(SCD)的儿童。(生物谷Bioon.com)
原文出处:Merck Receives Positive CHMP Opinion for VAXNEUVANCE™ (Pneumococcal 15-valent Conjugate Vaccine) in Infants and Children
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


