赛诺菲新型SGLT-1/2双效抑制剂sotagliflozin在欧盟进入正式审查
2018年03月31日讯 /生物谷BIOON/ --法国制药巨头赛诺菲(Sanofi)近日宣布,欧洲药品管理局(EMA)已受理sotagliflozin(索格列净)的上市许可申请(MAA)。此次MAA,申请批准sotagliflozin作为胰岛素疗法的一种口服补充疗法,用于改善1型糖尿病(T1D)成人患者的血糖控制。sotagliflozin是一种钠-葡萄糖协同转运蛋白-1和钠-葡萄糖协同转运蛋白
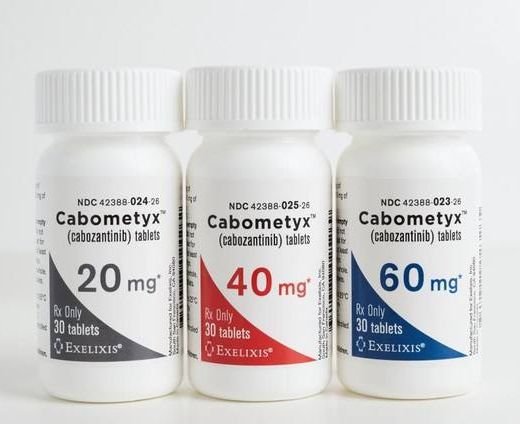
益普生靶向抗癌药Cabometyx二线治疗晚期肝细胞癌(HCC)在欧盟进入正式审查
2018年03月30日/生物谷BIOON/-法国制药公司益普生(ipsen)近日宣布,欧洲药品管理局(EMA)已受理口服靶向抗癌药Cabometyx(cabozantinib)治疗晚期肝细胞癌(HCC)的额外适应症申请。此次提交,是基于全球性III期临床研究CELESTIAL的积极数据。该研究是一项随机、双盲、对照研究,在全球19个国家超过100个临床中心开展,研究中共入组了773例既往接受过多吉
拜耳“广谱“抗癌药larotrectinib在美进入实质审查,可治疗各类TRK融合肿瘤
小编推荐会议:2018新药研发东方论坛2018年03月27日/生物谷BIOON/--德国制药巨头拜耳(Bayer)与合作伙伴Loxo Oncology近日联合宣布,双方已完成向美国食品和药物管理局(FDA)滚动提交靶向药物larotrectinib的新药申请(NDA)。此次滚动提交于2017年12月启动,NDA的目的是寻求批准larotrectinib用于存在神经营养酪氨酸激酶(NTRK)基因融合
英国Shire公司新型便秘药物prucalopride在美国进入正式审查
2018年03月07日讯 /生物谷BIOON/ --英国制药公司Shire近日宣布美国食品和药物管理局(FDA)已受理实验性药物prucalopride(SHP555)的新药申请(NDA),该药是一种选择性、高亲和力的5-羟色胺4(5-HT4)受体激动剂,目前正被评估作为一种潜在的每日一次药物,用于慢性特发性便秘(CIC)成人患者的治疗。FDA预计将在2018年12月21日做出审查决定。如果获批,
Shire公司抗癌药Calaspargase Pegol (Cal-PEG)在美国进入正式审查
2018年03月10日讯 /生物谷BIOON/ --英国制药公司Shire是罕见疾病领域的全球生物技术领导者。近日,该公司宣布美国食品和药物管理局(FDA)已受理实验性抗癌药Calaspargase Pegol(Cal-PEG,SHP663)的生物制品许可申请(BLA)。目前,该药正评估作为多药化疗方案的一部分,用于急性淋巴细胞白血病(ALL)的治疗。FDA已指定该BLA的处方药用户收费法(PDU
总局发布眼科光学相干断层扫描仪注册技术审查指导原则的通告
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了《眼科光学相干断层扫描仪注册技术审查指导原则》,现予发布。特此通告。附件:眼科光学相干断层扫描仪注册技术审查指导原则附件眼科光学相干断层扫描仪注册技术审查指导原则本指导原则旨在指导注册申请人对眼科光学相干断层扫描仪(Optical Coherence Tomography,简称OCT)注册
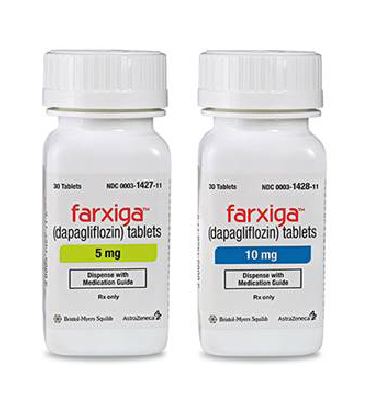
阿斯利康新型降糖药Forxiga(达格列净)治疗1型糖尿病在欧盟进入正式审查
2018年03月06日讯 /生物谷BIOON/ --英国制药巨头阿斯利康(AstraZeneca)近日宣布,欧洲药品管理局(EMA)已受理新型降糖药Farxiga(中文品牌名:安达唐,通用名:dapagliflozin,达格列净)的上市许可变更申请(MAV),该药是一种选择性钠-葡萄糖协同转运蛋白-2抑制剂(SGLT2i),此次MAV寻求批准Forxiga作为胰岛素疗法的一种口服辅助治
总局发布超声软组织切割止血系统注册技术审查指导原则的通告
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了《超声软组织切割止血系统注册技术审查指导原则》,现予发布。特此通告。附件:超声软组织切割止血系统注册技术审查指导原则本指导原则旨在给出系统的、具有指导意义的指南性文件,用于指导注册申请人规范产品的研究开发和注册申报,同时也用于指导监管部门对超声软组织切割止血系统申请注册材料的技术审评。本指
国家食品药品监督管理总局发布《人表皮生长因子受体(EGFR)突变基因检测试剂(PCR法)注册技术审查指导原则》
小编推荐会议:2018先进体外诊断行业峰会为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了《人表皮生长因子受体(EGFR)突变基因检测试剂(PCR法)注册技术审查指导原则》《幽门螺杆菌抗原/抗体检测试剂注册技术审查指导原则》《抗人球蛋白检测试剂注册技术审查指导原则》《肠道病毒核酸检测试剂注册技术审查指导原则》,现予发布。特此通告。附件1
总局发布人表皮生长因子受体(EGFR)突变基因检测试剂等4项注册技术审查指导原则的通告
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了《人表皮生长因子受体(EGFR)突变基因检测试剂(PCR法)注册技术审查指导原则》《幽门螺杆菌抗原/抗体检测试剂注册技术审查指导原则》《抗人球蛋白检测试剂注册技术审查指导原则》《肠道病毒核酸检测试剂注册技术审查指导原则》,现予发布。特此通告。附件:1.人表皮生长因子受体(EGFR)突变基因