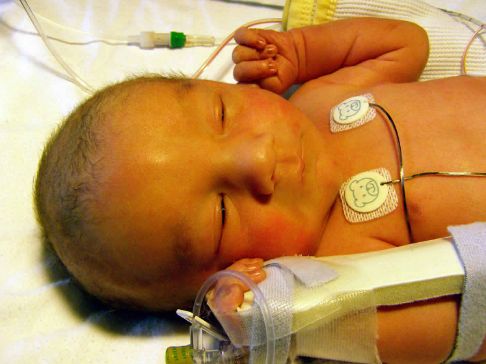
口服ASBT抑制剂maralixibat获美国FDA优先审查:治疗ALGS患者胆汁淤积性瘙痒!
maralixibat是一种口服顶端钠依赖性胆汁酸转运体(ASBT)抑制剂,导致更多胆汁酸从粪便中排除,减少胆汁酸介导的肝损伤和并发症。
胆汁淤积症突破性药物!强效回肠胆汁酸转运体抑制剂odevixibat在美国和欧盟申请上市!
odevixibat有潜力成为第一个治疗进行性家族性肝内胆汁淤积症(PFIC)的药物。
GSK回肠胆汁酸转运体抑制剂linerixibat治疗胆汁郁积性瘙痒疗效显著!
linerixibat有潜力成为60年来针对原发性胆汁性胆管炎(PBC)胆汁郁积性瘙痒的首个新疗法。
胆汁淤积症突破性药物!强效回肠胆汁酸转运体抑制剂odevixibat III期成功:达到欧美监管终点!
odevixibat有潜力成为第一个治疗进行性家族性肝内胆汁淤积症(PFIC)的药物。
Science:揭示底物和抑制剂对多药转运蛋白P-glycoprotein的变构调节机制
2019年6月9日讯/生物谷BIOON/---在一项新的研究中,来自美国范德堡大学和弗吉尼亚大学的研究人员发现了一种蛋白泵如何区分它将细胞中排出的化学物和阻止它发挥作用的抑制剂。相关研究结果近期发表在Science期刊上,论文标题为“Mechanism of allosteric modulation of P-glycoprotein by transport substrates and in
美国FDA授予Albireo新型回肠胆汁转运体抑制剂A4250胆道闭锁孤儿药资格
2019年1月24日讯 /生物谷BIOON/ --Albireo Pharma是一家临床阶段的制药公司,专注于开发新型胆汁酸调节剂用于罕见儿科肝脏疾病的治疗。近日,该公司宣布,美国食品和药物管理局(FDA)已授予其先导药物A4250治疗胆道闭锁(biliary atresia)的孤儿药资格。胆道闭锁是一种罕见的、威胁生命的肝脏疾病,目前尚没有获批的治疗药物。在美国和欧盟,A4250目前已被授予多种
欧盟授予Albireo回肠胆汁转运体抑制剂A4250治疗胆道闭锁的孤儿药资格
2018年12月27日讯 /生物谷BIOON/ --Albireo Pharma是一家临床阶段的制药公司,专注于开发新型胆汁酸调节剂用于罕见儿科肝脏疾病的治疗。近日,该公司宣布,欧洲药品管理局(EMA)已授予其先导药物A4250治疗胆道闭锁的孤儿药资格。胆道闭锁是一种罕见的、威胁生命的肝脏疾病,目前尚没有获批的治疗药物。在美国和欧盟,A4250之前已被授予治疗进行性家族性肝内胆汁淤积症(PFIC)
美国FDA授予Albireo首创胆汁转运蛋白抑制剂A4250罕见儿科病资格
2018年6月13日讯 /生物谷BIOON/ --Albireo Pharma是一家临床阶段的制药公司,专注于开发新型胆汁酸调节剂用于罕见儿科肝脏疾病的治疗。近日,该公司宣布,美国食品和药物管理局(FDA)已授予其先导药物A4250治疗进行性家族性肝内胆汁淤积症(PFIC)的罕见儿科疾病资格认定。此前,A4250在2012年还被美国FDA和欧盟EMA授予了孤儿药资格,在2016年被EMA授予了优先
全球首例 卫材胆汁酸转运抑制剂便秘药物GOOFICE在日本上市
日前,日本制药名企卫材公司旗下胃肠疾病子公司EA药业和Mochida制药股份有限公司宣布,全球首款胆汁酸转运抑制剂于2018年4月19日正式在日本上市。该药物商品名为GOOFICE(通用名elobixibat hydrate),剂型为片剂,药物含量为5mg/片,药品的开发编号AJG533。EA药业是通过向Albireo AB(瑞典)获得了该药物的许可。GOOFICE片剂是一