Cancer Cell:揭示花生四烯酸和γ干扰素协同诱导肿瘤细胞铁死亡机制
在一项新的研究中,来自美国密歇根大学罗杰尔癌症中心的研究人员发现一种细胞因子和一种脂肪酸可以协同发挥作用,触发一种以前由合成分子研究确定的细胞死亡。他们开展细胞培养物体外实验和小鼠体内实验,了解到一种称为γ干扰素的T细胞细胞因子的释放与一种称为花生四烯酸的脂肪酸一起如何通过靶向ACSL4酶而导致一种叫做铁死亡(ferroptosis)的细胞死亡。
Nature Chemistry:细胞内原位合成人工聚合物实现肿瘤精准治疗
细胞内化学环境具有高度复杂性并且细胞对外部刺激极为敏感,因此利用化学手段在活细胞内实现非天然分子结构转化,特别是人工大分子合成一直以来都较为困难,但科研人员对这一领域的探索却从未停止。可以试想如果将人工大分子引入细胞内,他们是否会与天然大分子发生相互作用,是否会影响细胞行为,是否会改变细胞原有的功能,是否能杀死肿瘤细胞实现肿瘤治疗?更
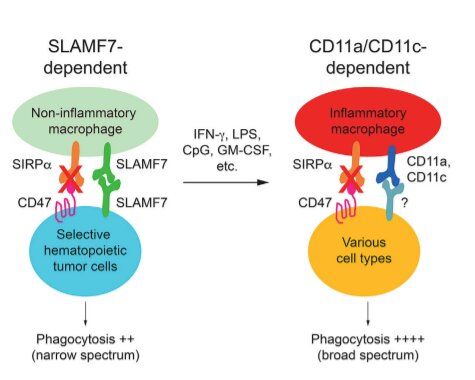
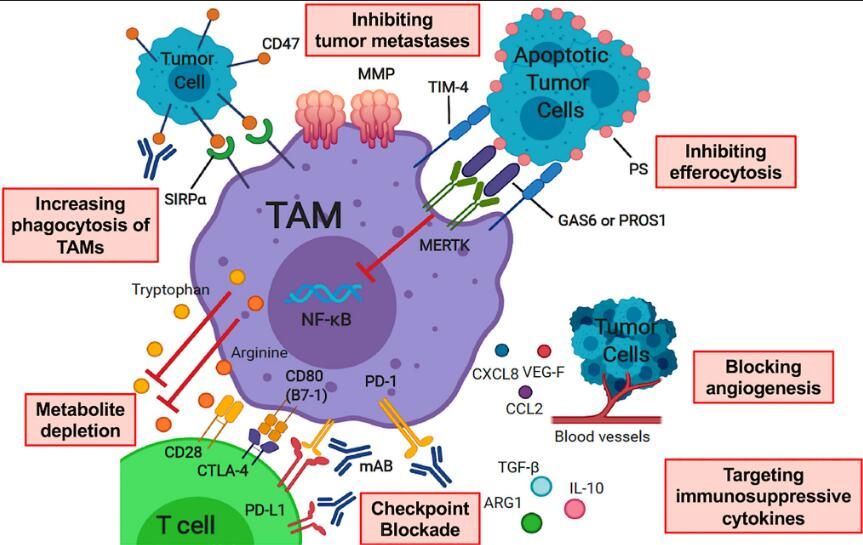
Cell子刊:揭示增强巨噬细胞杀死癌细胞的能力
在一项新的研究中,来自加拿大蒙特利尔大学和蒙特利尔临床研究所等研究机构的研究人员利用位于巨噬细胞表面上的两种分子---CD11a和CD11c---唤醒免疫系统摧毁癌症的本能,这是治疗癌症的一条有希望的途径。相关研究结果近期发表在Cell Reports期刊上。
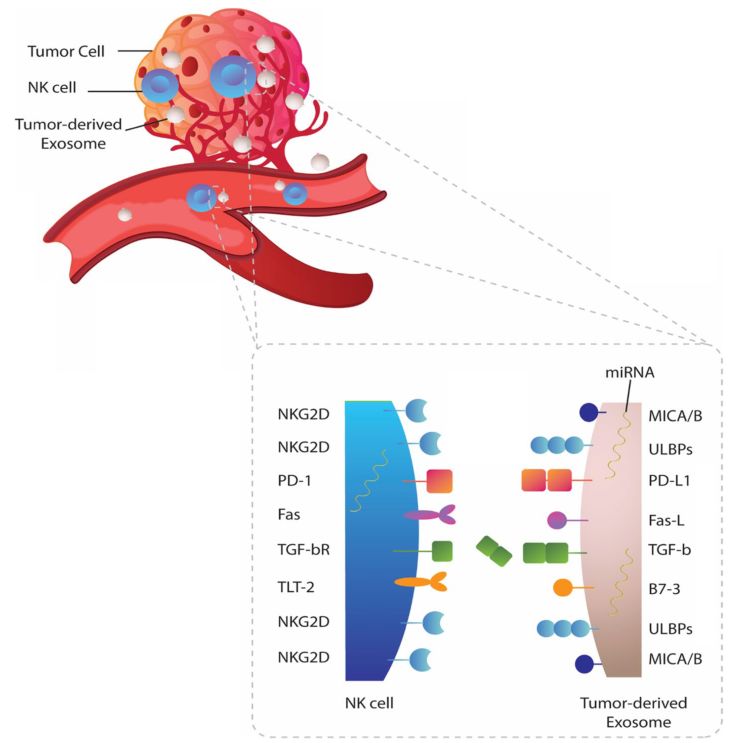
科学家揭示了肿瘤免疫治疗中肿瘤外泌体对NK细胞的影响
肿瘤来源的外泌体(TDEs)在癌症生物学的多个方面发挥着重要作用,有很多研究结论明显显示,TDES还可以通过负面影响抗肿瘤免疫来促进肿瘤生长。
Science子刊:人正交IL-2/IL-2Rβ系统可增强CAR-T细胞的增殖和抗肿瘤效果
在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学院和斯坦福大学医学院的研究人员设计出一对人正交IL-2(orthogonal IL-2, ortho-hIL-2)和人正交IL-2Rβ(ortho-hIL-2Rβ)对,含有人类特异性突变。ortho-hIL-2对表达ortho-hIL-2Rβ的细胞具有选择性,对野生型T细胞没有明显的信号传导作用。ortho
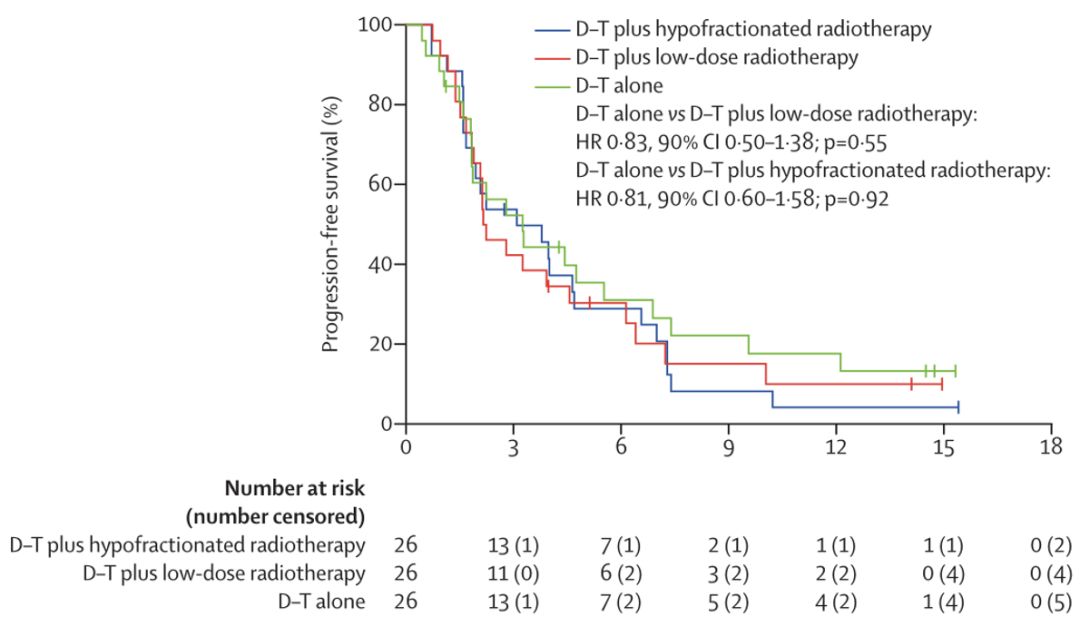
《柳叶刀·肿瘤学》:对PD-1/PD-L1抑制剂耐药的非小细胞肺癌患者或需另谋出路
凭借超高的发病率与致死率,肺癌成为对人群健康和生命威胁最大的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占比80%以上。目前,单独使用PD-1抑制剂或PD-L1抑制剂,以及二者分别与化疗配合的治疗方案,已成功跻身于NSCLC的一线治疗行列[1-3],但大部分患者要么对该方案无反应,要么在治疗期间仍会发生进展。好在靶向免疫检查点的工作机
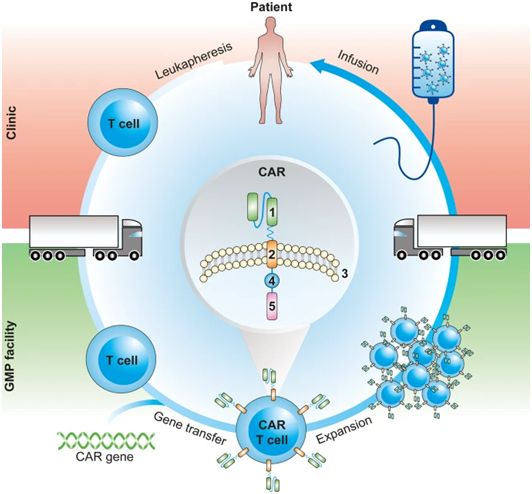
摘去肿瘤细胞的“糖衣”,CAR-T即成为“炮弹”
通过基因工程技术将T细胞激活,并装上定位导航到肿瘤的装置-肿瘤嵌合抗原受体(Chimeric Antigen Receptor, CAR),可以将T细胞这个普通“武器”改造成“超级武器”,即为CAR-T细胞。CAR-T是治疗B细胞恶性肿瘤的有效疗法,但在实体瘤中疗效有限。这些限制性的因素包括:肿瘤部位T细胞的迁移和浸润不足、抑制信号的持续存在、肿瘤限制性抗原
JEM:揭示人类机体肺部巨噬细胞发育的分子机理
来自瑞典卡罗琳学院等机构的科学家们通过研究揭示了机体肺部巨噬细胞是如何发育的,相关研究结果或有望帮助减少机体的器官损伤,对于后期开发治疗肺部疾病的新型疗法至关重要。
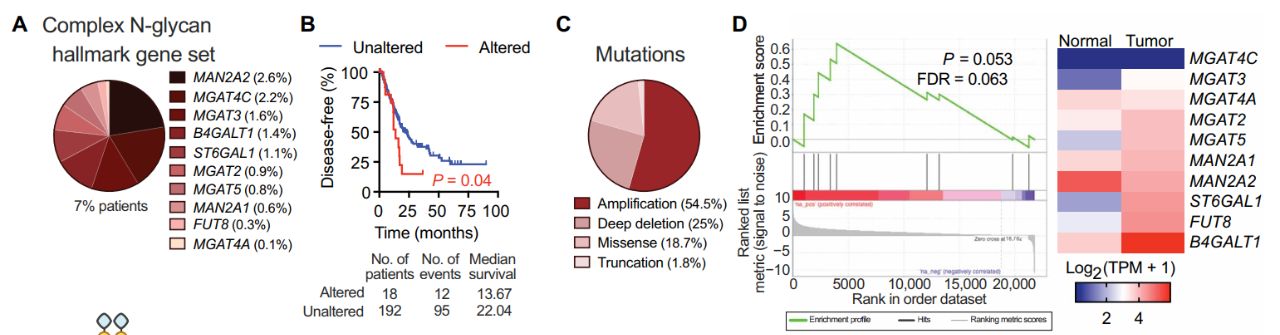
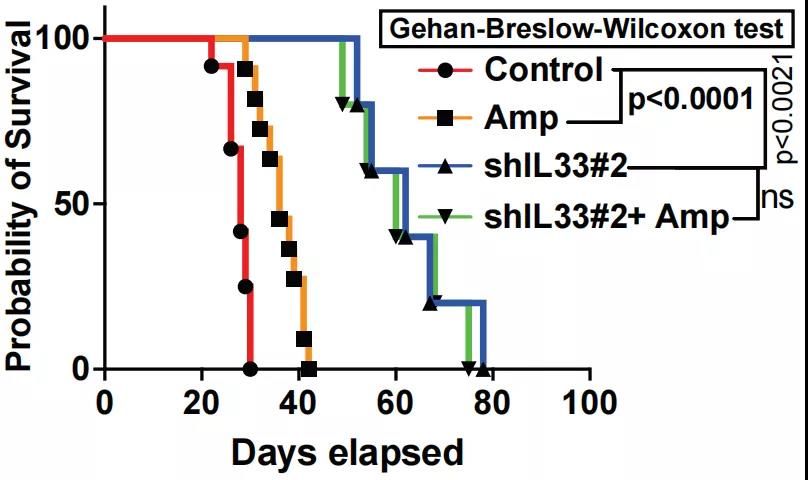
《细胞》子刊:科学家发现,肿瘤中的真菌会刺激胰腺癌细胞分泌IL-33,招募并激活2型先天性淋巴细胞,促进肿瘤进展
说起“癌王”,大家都会不约而同地想到胰腺癌,这种总体5年生存率将将达到两位数的癌症对于医生、患者和基础研究人员都是极大的挑战。胰腺癌具有非常独特的肿瘤免疫谱,一部分肿瘤中有40-60%都是免疫细胞,但可气的是,它们基本都是免疫抑制细胞,比如肿瘤相关巨噬细胞、调节性T细胞、CD4+ 2型辅助T细胞(Th2)和骨髓来源的抑制细胞,它们狼狈
Science子刊:一种正交IL-2/IL-2Rβ系统促进CAR-T细胞的持久存在并增强肿瘤清除效果
在一项新的研究中,来自美国Synthekine公司的研究人员报告了一种能够特异性地在体内控制CAR-T细胞的增殖和激活的正交IL-2受体/配体系统,在这种系统中,一种正交人IL-2(STK-009)选择性地与CAR-T细胞表面上表达的正交人IL-2Rβ(hoRb)配对。STK-009在存在和不存在肿瘤抗原的情况下让表达hoRb的CAR-T细胞增殖,并维持干细胞记忆T细胞和效应T细胞的存在。