Cell子刊:揭示增强巨噬细胞杀死癌细胞的能力
来源:本站原创 2022-01-21 07:15
在一项新的研究中,来自加拿大蒙特利尔大学和蒙特利尔临床研究所等研究机构的研究人员利用位于巨噬细胞表面上的两种分子---CD11a和CD11c---唤醒免疫系统摧毁癌症的本能,这是治疗癌症的一条有希望的途径。相关研究结果近期发表在Cell Reports期刊上。
2022年1月21日讯/生物谷BIOON/---阻断抑制性检查点SIRPα-CD47可以促进巨噬细胞对癌细胞的吞噬,是抗癌治疗中一条很有前途的途径。有效的吞噬作用严格地取决于促吞噬受体--- Fc受体(FcR)、整合素CD11b或SLAMF7---与癌细胞表面上的配体的共同参与。
在一项新的研究中,来自加拿大蒙特利尔大学和蒙特利尔临床研究所等研究机构的研究人员利用位于巨噬细胞表面上的两种分子---CD11a和CD11c---唤醒免疫系统摧毁癌症的本能,这是治疗癌症的一条有希望的途径。相关研究结果近期发表在Cell Reports期刊上,论文标题为“Inflammatory macrophages exploit unconventional pro-phagocytic integrins for phagocytosis and anti-tumor immunity”。
几年来,免疫学和个性化医疗为医生和患者带来了抗击癌症的新希望。这项新的研究揭开了一种创新的治疗癌症的方式,与蓬勃发展的精准医学领域相一致。这些作者研究了是否可以利用更多的促吞噬受体来扩大吞噬的范围。炎症刺激物,包括多种细胞因子和TLR(Toll-like receptor)配体,增强了吞噬效率,完全缓解了吞噬作用对FcR、CD11b和SLAMF7的需求。这些作用是由非典型促吞噬整合素CD11a和CD11c介导的,它们与CD18一起作用,启动肌动蛋白极化,导致吞噬作用。一些炎症刺激物甚至在没有SIRPα-CD47阻断的情况下也能使吞噬作用发生。在临床研究中,富含巨噬细胞的肿瘤中较高的CD11c表达与生存率的提高相关。因此,炎性巨噬细胞利用非典型促吞噬整合素来提高吞噬能力和抗肿瘤免疫力。
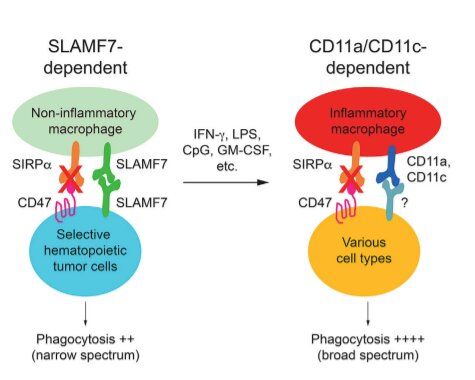
图片来自Cell Reports, 2021, doi:10.1016/j.celrep.2021.110111。
这些先进的疗法主要靶向免疫系统中称为T细胞的免疫细胞,它们的作用一方面是保护身体不受有害的病毒、细菌和寄生虫等外来物的侵害,另一方面也是为了对付癌细胞。
在“身体卫士”中也有称为巨噬细胞的免疫细胞,这些免疫细胞的主要作用是通过吞食来消灭有害物。科学家们和制药公司对靶向巨噬细胞用于治疗目的越来越感兴趣。
在这项新的研究中,论文共同通讯作者、蒙特利尔大学的André Veillette博士及其团队发现巨噬细胞特别擅长摧毁某些类型的癌细胞。更重要的是,他们能够极大地刺激巨噬细胞的胃口。特别是,他们发现了位于巨噬细胞表面上的两种分子(CD11a和CD11c),这两种分子经激活后可以增加巨噬细胞摧毁肿瘤细胞的本能。在动物模型和实验室的人类细胞培养物中,受到刺激的巨噬细胞变成了癌细胞的超级吞噬者。
论文共同第一作者Zhenghai Tang说,“释放巨噬细胞破坏力的能力是一项重要的发现,它为个性化医疗中一些真正令人兴奋的新可能性铺平了道路。” 论文共同第一作者Dominique Davidson补充说,“我们帮助身体更好地保护自己。”
这种利用CD11a和CD11c帮助身体更好地对抗癌症的新方法是Veillette团队正在进行的研究工作的产物。Veillette团队在过去30年里一直在研究调控免疫系统运作的机制。2017年,在发表于Nature期刊上的一项研究中,该团队阐明了SLAMF7分子,它也对巨噬细胞的破坏力产生作用(Nature, 2017, doi:10.1038/nature22076)。
Veillette说,“我们对免疫系统的运作了解得越多,我们就越能找到有效的、毒性较小的治疗方案来对抗疾病。像巨噬细胞这样的免疫细胞不仅在当前的免疫学研究中获得了极大的关注,而且也在制药业中也是如此,因为这确实是治疗许多致命疾病的未来。”
他补充说,“就我们而言,下一步将是确定CD11a和CD11c分子在多大程度上可以作为生物标志物来识别最有可能对这种类型的治疗产生反应的患者。”(生物谷 Bioon.com)
参考资料:
Zhenghai Tang et al. Inflammatory macrophages exploit unconventional pro-phagocytic integrins for phagocytosis and anti-tumor immunity. Cell Reports, 2021, doi:10.1016/j.celrep.2021.110111.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


