《柳叶刀·肿瘤学》:对PD-1/PD-L1抑制剂耐药的非小细胞肺癌患者或需另谋出路
来源:奇点糕 2022-03-11 17:35
凭借超高的发病率与致死率,肺癌成为对人群健康和生命威胁最大的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占比80%以上。目前,单独使用PD-1抑制剂或PD-L1抑制剂,以及二者分别与化疗配合的治疗方案,已成功跻身于NSCLC的一线治疗行列[1-3],但大部分患者要么对该方案无反应,要么在治疗期间仍会发生进展。好在靶向免疫检查点的工作机
凭借超高的发病率与致死率,肺癌成为对人群健康和生命威胁最大的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占比80%以上。
目前,单独使用PD-1抑制剂或PD-L1抑制剂,以及二者分别与化疗配合的治疗方案,已成功跻身于NSCLC的一线治疗行列[1-3],但大部分患者要么对该方案无反应,要么在治疗期间仍会发生进展。
好在靶向免疫检查点的工作机制多样,联合使用似有希望。在临床前模型中,PD-1/PD-L1抑制剂和CTLA-4抑制剂联合使用(durvalumab + tremelimumab)显示出协同作用,并已被批准为转移性NSCLC的一线治疗方案[5-6]。然而,这种联合治疗的前瞻性数据太少,其临床效益也被打上了大大的问号。
近期,美国Dana-Farber癌症研究所免疫肿瘤学中心的F Stephen Hodi教授携团队在《柳叶刀·肿瘤学》上发表重要研究成果[7],填补了放疗联合PD-L1抑制剂和CTLA-4抑制剂在临床中的空白。
他们指出,对既往PD-1/PD-L1抑制剂治疗无应答的NSCLC患者来说,即使联合了放疗,也没有提高患者对PD-L1抑制剂和CTLA-4抑制剂联合使用的反应。
放疗单独使用或与化疗联用是局部晚期、不能手术的NSCLC的标准治疗方法,有时候还能联合免疫治疗使转移性NSCLC患者获得治疗效益[8]。
此前,已有报道指出,大分割放疗(8 Gy/段)和低剂量放疗(<1 Gy/段)都具有良好的免疫效果[9-11],比如促进树突状细胞成熟、T细胞归巢激活,以及巨噬细胞极化等,但这些放疗方案尚未在接受PD-L1抑制剂联合CTLA-4抑制剂的患者中进行前瞻性试验。
故此,F Stephen Hodi团队分别评估了PD-L1抑制剂联合CTLA-4抑制剂,以及将双免疫检查点抑制剂与低剂量放疗或大分割放疗联用,在既往PD-1/PD-L1抑制剂治疗转移性NSCLC患者中的潜在益处。
这个非盲、多中心、随机的2期临床研究由美国国家癌症研究所(NCI)实验治疗临床试验网络在美国18个地点(癌症中心和医院)开展。参与者为组织学或细胞学证实的转移性非小细胞肺癌患者,年龄至少为18岁,表现状态为美国东部肿瘤协作组(ECOG)评分标准中的0或1,预期寿命超过6个月,并且有证据表明,在先前的全身PD-1/PD-L1靶向治疗期间存在临床疾病进展。
在2017年8月24日至2019年3月29日期间,共计纳入90例参与者,Hodi团队将所有患者随机分配成三组,治疗方案分别为:
双免疫组:每4周静脉注射一次PD-L1抑制剂durvalumab(每次1500 mg)和CTLA-4抑制剂tremelimumab(每次75 mg),durvalumab注射最多持续13个周期,tremelimumab最多持续4个周期;
双免疫联合低剂量放疗组:在durvalumab与tremelimumab双免疫治疗的前4个周期,每天提供两次0.5 Gy的低剂量放疗,重复2天;
双免疫联合大分割放疗组:首次注射durvalumab与tremelimumab后一周,仅在治疗的第一个周期内,每隔一天给予24 Gy的大分割放疗,每次8 Gy。
最终,在排除放弃参与或因脑转移等因素不适合纳入研究的患者后,共有78例患者接受了指定的治疗方案,每组26例。研究治疗持续到1年或直至发生进展,主要终点是总缓解率,次要终点包括无进展生存期等。
总的来说研究结果令人失望,双免疫联合低剂量放疗(7.7%,0.0-16.3;p=0.64)或大分割放疗组(11.5%,1.2-21.8;p=0.99)的总体应答率与双免疫组(11.5%,90% CI 1.2-21.8)之间并无显着差异。
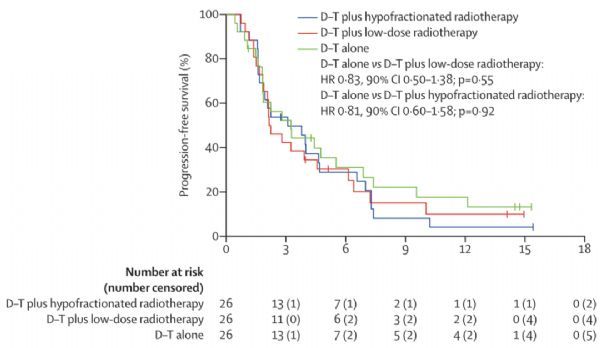
对各组中无进展生存患者(18个月)的比例进行统计,发现双免疫组、联合低剂量放疗组与大分割放疗组的比例分别为81%、85%和92%,但遗憾的是,各组无进展生存期之间亦无显着差异(双免疫组的中位数为3.3个月;低剂量放疗组的中位数为4.6个月;大分割放疗组的中位数为4个月)。
此外,总体生存率的结果也不尽如人意,各组之间仍然没有显着差异。
Hodi团队对每个治疗周期的治疗相关毒性都进行了评估,治疗停止后90天内每30天评估一次,并且根据不良事件的通用术语标准4.0版对毒性进行了分级。
结果显示,78例患者中有59例(76%)发生了可能与治疗相关的不良事件,最常见的3级或3级以上不良事件分别是呼吸困难(双免疫组2例,低剂量放疗组3例,大分割放疗组3例)和低钠血症(双免疫组1例,低剂量放疗组2例,大分割放疗组3例)。
进一步分析发现,双免疫组发生了1例(4%)与治疗相关的严重不良事件(黄斑丘疹);低剂量放疗组发生了5例(19%)与治疗相关的严重不良事件,包括腹痛、腹泻、呼吸困难、低血钾和呼吸衰竭等;大分割放疗组发生了4例(15%)与治疗相关的严重不良事件(肾上腺功能不全、结肠炎、腹泻和低钠血症)。
总的来说,这个随机临床2期试验是迄今为止首个研究CTLA-4抑制剂联合PD-L1抑制剂与放疗联用的前瞻性成果,评估了放疗在既往PD-1/PD-L1靶向治疗有进展的NSCLC患者中仅作为系统免疫激活剂的效用。
尽管没有取得临床效益上的突破,但研究人员获得了PD-L1抑制剂与CTLA-4抑制剂联合使用治疗PD-1/PD-L1耐药患者的安全性数据,并通过中位随访12.4个月,发现治疗后发生进展性疾病的患者数量减少,同时,对治疗发生反应的患者数量增加。因此,Hodi团队确定了PD-L1抑制剂与CTLA-4抑制剂联合使用对表现出应答的部分患者具有重大临床意义。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。