三款1类新药拟纳入突破性治疗药物品种
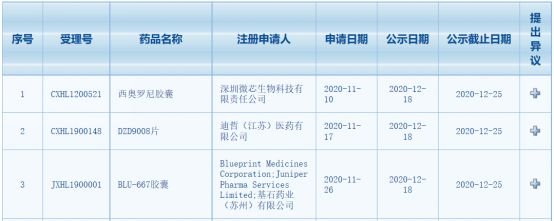
近日,中国国家药监局药品审评中心(CDE)最新公示,三款新药拟纳入突破性治疗品种,并进入为其一周的公示期。这三款新药分别是:Blueprint Medicines/基石药业RET抑制剂BLU-667胶囊(pralsetinib,普拉替尼),微芯生物多靶点多通路选择性激酶抑制剂西奥罗尼胶囊,迪哲医药EGFR抑制剂DZD9008片。(截图来源:CDE官网)其中,
CDE拟突破性疗法认证:荣昌生物ADC单抗,治疗HER2+尿路上皮癌
12月17日,荣昌生物纬迪西妥单抗(注射用重组人源化抗HER2单抗-MMAE偶联剂)被CDE拟授予突破性疗法资格(受理号:CXSL1400087),用于既往经过化疗失败后疾病进展的HER2过表达局部晚期或转移性尿路上皮癌患者(包括膀胱、输尿管、肾盂及尿道来源)。一项在43例既往经过化疗失败后疾病进展的HER2+ (IHC3+或2+)局部晚期或mUC患者中开展
科济生物靶向BCMA的CAR-T疗法拟纳入突破性治疗品种
日前,据国家药监局CDE公示信息,科济生物CT053全人抗BCMA自体CAR-T细胞注射液拟纳入突破性治疗品种,拟定适应症为复发难治多发性骨髓瘤(R/R MM)。据了解,CT053是由科济生物自主研发的创新疗法,采用全人抗体靶向B细胞成熟抗原(BCMA)的嵌合抗原受体(CAR)修饰的T细胞,主要目标适应症为R/R MM。BCMA则是一种极其重要的
CDE公示3个拟纳入突破性治疗药物,来自诺华、科济生物、Calliditas制药
中国国家药监局药品审评中心(CDE)网站公示了3个拟纳入突破性治疗品种的药物,分别为科济生物旗下CT053全人抗BCMA自体CAR T细胞注射液、Calliditas制药的Nefecon(布地奈德)缓释胶囊以及诺华的TQJ230注射液。昨日(11月30日),中国国家药监局药品审评中心(CDE)网站公示了3个拟纳入突破性治疗品种的药物,分别为科济生
恒瑞医药卡瑞利珠单抗又一上市申请拟纳入优先审评
恒瑞医药发布公告称,其子公司苏州盛迪亚生物医药有限公司的注射用卡瑞利珠单抗申报生产,拟联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗,该药品注册申请已获国家药监局受理,并纳入拟优先审评审批程序。药品名称:注射用卡瑞利珠单抗剂型:注射剂规格:200mg/瓶注册分类:治疗用生物制品1类申报阶段:生产申请人:苏州盛迪亚生物医药有限公司拟优先
医保局发布区域点数法总额预算和按病种分值付费试点城市名单
11月4日,国家医保局官网发布《国家医疗保障局办公室关于印发区域点数法总额预算和按病种分值付费试点城市名单的通知》。按照《区域点数法总额预算和按病种分值付费试点工作方案》(医保办发〔2020〕45号)要求,根据各省(区、市)医疗保障局自愿申报的情况,确定了区域点数法总额预算和按病种分值付费试点城市名单。据统计,共有27个省的70个市纳入本次试点。
泽璟制药肝癌1类新药上市申请拟纳入优先审评
10月12日,中国国家药监局药品审评中心(CDE)网站最新公示,泽璟制药1类新药甲苯磺酸多纳非尼片上市申请拟纳入优先审评,本次申请的拟定适应症为——用于治疗晚期(无法手术或转移性)肝细胞癌。这不仅意味着多纳非尼有望在中国加速获批,也意味着泽璟制药将有望迎来首款获批上市的药品。多纳非尼是泽璟制药开发的口服多靶点、多激酶抑制剂类小分子抗肿瘤药物,属于1类新药。临
5款新药拟纳入优先审评 来自贝达药业、阿斯利康、拜耳等
10月12日,中国国家药监局药品审评中心(CDE)网站公示,5款新药上市申请拟纳入优先审评(详见下表)。这些产品分别是贝达药业1类新药埃克替尼,阿斯利康(AstraZeneca)EGFR-TKI奥希替尼,泽璟制药肝癌新药多纳非尼,拜耳(Bayer)抗血栓产品利伐沙班,赛诺菲(Sanofi)"双靶点"抗体度普利尤单抗(dupilumab)。拟纳入优
百济神州「迪妥昔单抗」和「泽布替尼」拟纳入优先审评
9月29日,中国国家药监局(NMPA)药品审评中心(CDE)公示,百济神州2款新药拟纳入优先审评。其中一款为迪妥昔单抗注射液,正在开发用于治疗多种神经母细胞瘤。根据公开信息,这是今年初百济神州从EUSA Pharma引进的单克隆抗体QARZIBA(dinutuximab beta),它可以与神经母细胞瘤细胞过度表达的特定靶标GD2.iii结合。另一款为BTK
爱美津制药罕见病用药拟纳入优先审评
9月14日,中国国家药监局药品审评中心(CDE)网站最新显示,由爱美津制药按4类仿制药提交的麦格司他胶囊上市申请拟纳入优先审评,拟定适应症(或功能主治)为:用于成人及儿童C型尼曼匹克病患者的进行性神经症状的治疗。麦格司他(miglustat)是一种葡糖神经酰胺合成酶抑制剂,它能够降低葡萄糖脑苷脂水平,从而缓解患者症状。葡糖神经酰胺合成酶是大多数鞘糖脂类合成的