针对新冠病毒SARS-CoV-2/COVID-19,Nature期刊研究进展一览(第5期)
来源:本站原创 2020-11-30 23:22
2020年11月30日讯/生物谷BIOON/---自2019年12月8日以来,中国湖北省武汉市报告了几例病因不明的肺炎。大多数患者在当地的华南海鲜批发市场工作或附近居住。在这种肺炎的早期阶段,严重的急性呼吸道感染症状出现了,一些患者迅速发展为急性呼吸窘迫综合征 (acute respiratory distress syndrome, ARDS)、急性呼吸衰
2020年11月30日讯/生物谷BIOON/---自2019年12月8日以来,中国湖北省武汉市报告了几例病因不明的肺炎。大多数患者在当地的华南海鲜批发市场工作或附近居住。在这种肺炎的早期阶段,严重的急性呼吸道感染症状出现了,一些患者迅速发展为急性呼吸窘迫综合征 (acute respiratory distress syndrome, ARDS)、急性呼吸衰竭和其他的严重并发症。2020年1月7日,中国疾病预防控制中心(China CDC)从患者的咽拭子样本中鉴定出一种新型冠状病毒,最初被世界卫生组织(WHO)命名为2019-nCoV。大多数2019-nCoV肺炎患者的 症状较轻,预后良好。到目前为止,一些患者已经出现严重的肺炎,肺水肿,ARDS或多器官功能衰竭和死亡。
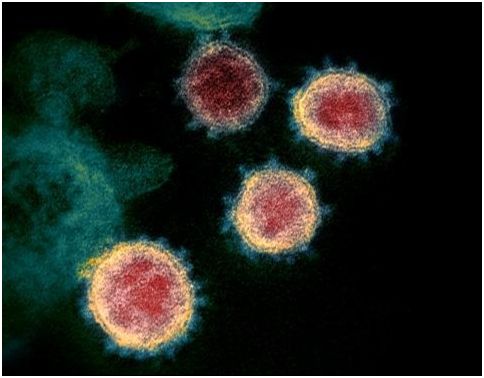
2020年2月11日,世卫组织将这种疾病病重命名为2019年冠状病毒病(COVID-19)。同一天,负责分类和命名病毒的的国际病毒分类学委员会的冠状病毒研究小组在bioRxiv上发表了一篇文章,指出该研究小组已经决定,新型冠状病毒2019-nCoV是导致2002-2003年爆发严 重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)的变种。因此,将这种新病原体重新命名为严重急性呼吸综合征冠状病毒2号(severe acute respiratory syndrome coronavirus 2),或SARS-CoV-2。值得注意的一点是,尽管国际病毒分类委员会冠状病毒研究小组将 病毒命名为SARS-CoV-2,但该研究小组主席John Ziebuhr认为这个名字(SARS-CoV-2)和SARS(严重急性呼吸综合征,也称非典型肺炎)没有关联。不过,这种病毒的重新命名引起了不少争议。据《科学》网站报道,世界卫生组织不满意SARS-CoV-2这个名字,而且不打 算采用此名称。
冠状病毒可引起多种动物的多系统感染。在此之前已有6种冠状病毒可以感染人类,它们主要引起人类的呼吸道感染:两种高度致命性的冠状病毒,即严重急性呼吸道综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV);4种可导致温 和的上呼吸道疾病的冠状病毒,即HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1。
基于此次疫情给中国和全世界带来严重的危害,小编针对Nature期刊上发表的2019-nCoV/COVID-19研究进行一番梳理,以飨读者。
1.Nature:构建出SARS-CoV-2感染的人远端肺类器官模型
doi:10.1038/s41586-020-3014-1
在一项新的研究中,来自美国斯坦福大学医学院等研究机构的研究人员以成人肺泡上皮细胞II型(AT2)或KRT5+基底细胞为来源,培育出长期不含饲养细胞的化学限定性远端肺祖细胞培养物:远端肺类器官(organoid)。相关研究结果于2020年11月25日在线发表在Nature期刊上,论文标题为“Progenitor identification and SARS-CoV-2 infection in human distal lung organoids”。
AT2细胞类器官表现出AT1转分化潜能,而基底细胞类器官产生的管腔内排列有分化的棒状细胞(club cell)和纤毛细胞。对基底细胞类器官的KRT5+基底细胞进行单细胞分析揭示了一个独特的ITGA6+ITGB4+有丝分裂细胞群体,它们的增殖可进一步产生一个TNFRSF12Ahi细胞亚群,这个细胞亚群含有大约10%的KRT5+基底细胞,簇集在终末细支气管内,并表现出丰富的克隆性类器官(clonogenic organoid)生长活性。构建出的远端肺类器官具有顶端朝外的极性,这将ACE2展示在暴露的外表面上,从而促进SARS-CoV-2感染AT2细胞和基底细胞培养物,并鉴定出棒状细胞是一个新的可被这种病毒感染的目标群体。对人远端肺进行长期不含饲养细胞的类器官培养,并结合单细胞分析,确定了未预想到的基底细胞功能异质性,并建立了一种简便的人远端肺感染(包括与COVID-19相关的肺炎)的体外类器官模型。
2.Nature:构建出一种计算机模型,可以准确预测新冠肺炎在美国10个大型城市的传播情况
doi:10.1038/s41586-020-2923-3
在一项新的研究中,来自美国斯坦福大学和西北大学的研究人员构建出一种计算机模型,并利用这种模型通过分析驱动感染风险的三个因素---人们在一天中去了哪里,停留了多长时间,以及有多少其他人在同一时间访问同一地点---准确预测了今年春天COVID-19在美国10个主要城市的传播情况。相关研究结果于2020年11月10日在线发表在Nature期刊上,论文标题为“Mobility network models of COVID-19 explain inequities and inform reopening”。
这项研究合并了人口统计学数据、流行病学估计和匿名手机位置信息,似乎证实了大多数COVID-19传播发生在“超级传染源(superspreader)”场所,比如全方位服务的餐馆、健身中心和咖啡馆,在那里,人们长时间地呆在狭小的空间里。这些研究人员说,他们的模型可以作为官员们的工具,通过揭示新感染和销售损失之间的权衡,帮助他们在重新开始营业(比如在20%或50%的营业能力下)时尽量减少COVID-19的传播。
论文共同作者、坦福大学人文与科学学院社会学教授David Grusky说,这种预测能力特别有价值,这是因为它针对少数族裔和低收入人群不成比例的感染率背后的因素提供了有用的新见解。他说,“在过去,这些差异被认为是由已存在的医疗状况和不平等的医疗服务驱动的,而我们的模型表明,人群流动模式也有助于推动这些不成比例的风险。”
3.Nature:利用K18-hACE2小鼠评估COVID-19发病机制
doi:10.1038/s41586-020-2943-z
在2003-2004年SARS流行期间,由于受感染的小鼠只产生了轻微的疾病,美国爱荷华大学的研究人员和其他人构建出表达hACE2的转基因小鼠(即K18-hACE2小鼠)。K18-hACE2小鼠在细胞角蛋白18编码基因的启动子的驱动下表达hACE2,而且主要是在上皮细胞中表达。受到SARS-CoV感染的K18-hACE2小鼠患上不好处理的脑炎和轻度肺炎。SARS-CoV-2和SARS-CoV都使用hACE2,但在患者的疾病表现中显示出差异。SARS-CoV-2感染上呼吸道的程度比SARS-CoV更大。SARS-CoV-2已经与嗅觉丧失、味觉丧失、血栓形成和肺血管内皮损伤、心脏和神经系统疾病以及儿童和青少年中的多系统炎症等临床表现相关。基于这些观察,爱荷华大学的研究人员推断SARS-CoV-2感染的K18-hACE2小鼠也可能显示出发病机制的差异。
在一项新的研究中,爱荷华大学的Paul B. McCray Jr和Stanley Perlman及其同事们展示了K18-hACE2小鼠对COVID-19疾病的研究和治疗的效用。他们发现SARS-CoV-2感染K18-hACE2小鼠会引起剂量依赖性的致死性呼吸道疾病,其特征类似于严重的人类COVID-19,包括弥漫性肺泡损伤、炎症细胞浸润、组织损伤、肺血管损伤和死亡,其中,有一部分小鼠会因出现脑部感染而死亡。相关研究结果近期发表在Nature期刊上,论文标题为“COVID-19 treatments and pathogenesis including anosmia in K18-hACE2 mice”。
SARS-CoV-2感染的K18-hACE2小鼠重现了许多在COVID-19患者中观察到的发现,因而提供了一个有用的模型来研究发病机制和评估干预措施。
4.Nature:新研究指出超过170万纽约人感染新冠病毒,而且这种病毒早在2月底就已存在于纽约
doi:10.1038/s41586-020-2912-6
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。在一项新的对今年2月初至7月采集的1万多份血浆样本进行的回顾性监测研究中,来自美国西奈山伊坎医学院的研究人员报告,SARS-CoV-2早在今年3月1日纽约市首例COVID-19病例被证实之前就已经存在于该市。他们的研究发现,超过170万纽约人---约占全市人口的20%--已经感染了这种病毒,而且这种病毒的感染死亡率接近1%,比流感的死亡率高10倍。相关研究结果于2020年11月3日在线发表在Nature期刊上,论文标题为“Repeated cross-sectional sero-monitoring of SARS-CoV-2 in New York City”。

在3月8日结束的一周内,纽约市感染病例急剧增加,随后在3月15日结束的一周内,COVID-19死亡病例大幅增加。纽约州于3月22日实施了一项待在家中的命令,此后纽约市的每日病例数开始趋于稳定,然后在4月和5月出现下降。论文共同通讯作者、西奈山伊坎医学院病理学副教授Emilia Mia Sordillo博士说,在3月初当地流行病开始出现时,几乎没有检测能力,但是,“我们如今知道许多无症状病例和轻度到中度的病例可能没有被发现。在这项新的研究中,我们旨在了解普通人群和寻求紧急护理的人的感染动态。”
5.Nature:65岁以下人群的COVID-19死亡人数更可能衡量一个国家的新冠病毒传播率
doi:10.1038/s41586-020-2918-0
在一项新的研究中,来自英国剑桥大学和法国巴斯德研究所等研究机构的研究人员发现鉴于不同国家的老年人口中报告的COVID-19死亡率存在很大差异,简单地比较不同国家的死亡总数可能会对SARS-CoV-2(一种导致COVID-19疾病的冠状病毒)的基本传播水平产生误导。相关研究结果于2020年11月2日在线发表在Nature期刊上,论文标题为“Age-specific mortality and immunity patterns of SARS-CoV-2”。
这项研究强调了欧洲养老院发生的大规模COVID-19疫情,以及一些亚洲和南美国家可能出现的失踪死亡事件,如何扭曲了老年群体的COVID-19死亡数据,使得对这一流行病规模的国家间比较不准确。这些作者表示,报告65岁以下人群死于COVID-19的情况可能要可靠得多,因此可以更清楚地了解这种病毒的基本传播情况,并能更好地进行国家间比较---这对指导政府试图控制COVID-19的策略至关重要。
6.Nature:通过构建肺部类器官和结肠类器官鉴定出新冠病毒抑制剂
doi:10.1038/s41586-020-2901-9
人们迫切需要利用人类疾病相关的细胞构建新的模型,来研究SARS-CoV-2生物学特性和促进药物筛选。鉴于SARS-CoV-2主要感染呼吸道,在一项新的研究中,来自美国威尔康奈尔医学院、芝加哥大学、哥伦比亚大学和中国上海交通大学等研究机构的研究人员利用人多能性干细胞(human pluripotent stem cell, hPSC)开发出一种肺部类器官(lung organoid)模型(下称hPSC-LO)。相关研究结果近期发表在Nature期刊上,论文标题为“Identification of SARS-CoV-2 Inhibitors using Lung and Colonic Organoids”。
hPSC-LO,特别是肺泡II型样细胞,可被SARS-CoV-2感染,并在SARS-CoV-2感染后表现出强劲的趋化因子表达,这与COVID-19患者中观察到的情况相似。这些患者中近25%的人也有胃肠道症状,这与更糟糕的COVID-19临床结果相关。与此同时,作为对hPSC-LO的补充,这些研究人员也利用hPSC构建出结肠类器官(hPSC-CO)来探究结肠细胞对SARS-CoV-2感染的反应。他们发现,多种结肠细胞类型,特别是肠上皮细胞(enterocyte),表达ACE2,并且可被SARS-CoV-2感染。
利用hPSC-LO,这些研究人员对美国食品药品管理局(FDA)批准的药物进行了高通量筛选,并鉴定出SARS-CoV-2的细胞进入抑制剂,包括伊马替尼(imatinib)、霉酚酸(mycophenolic acid, MPA)和盐酸阿的平(quinacrine dihydrochloride, QNHC)。这些药物在生理相关水平下的处理显著抑制了SARS-CoV-2对hPSC-LO和hPSC-CO的感染。
7.Nature:刺突蛋白突变D614G改变了新冠病毒的适应性
doi:10.1038/s41586-020-2895-3
在一项新的研究中,来自美国德克萨斯大学的研究人员通过基因改造让SARS-CoV-2毒株USA-WA1/2020携带D614G突变,并描述了它的影响。他们发现D614G通过提高这种毒株的感染力,增强了它在人肺上皮细胞和原代人气道组织中的复制。相关研究结果近期发表在Nature期刊上,论文标题为“Spike mutation D614G alters SARS-CoV-2 fitness”。

感染了G614变体的仓鼠在鼻腔洗液和气管中而不是在肺部中产生了较高的传染性病毒滴度,这就证实了之前的临床证据发现:D614G突变增加了COVID-19患者上呼吸道的病毒载量,并可能增加传播。
来自受到D614变体感染的仓鼠的血清对G614病毒变体的中和滴度适度高于对D614病毒变体的中和滴度,这表明(i)这种突变可能不会降低临床试验中疫苗对COVID-19的保护能力,(ii)应针对传播中的G614病毒变体进行治疗性抗体检测。结合临床发现,这项研究强调了这种突变在病毒传播、疫苗疗效和抗体治疗中的重要性。
8.Nature:一种新型筛查算法或能将COVID-19的检测成本降低20倍!
doi:10.1038/s41586-020-2885-5
近日,一项刊登在国际杂志Nature上的研究报告中,来自爱丁堡大学等机构的科学家们通过研究开发了一种新型的数学算法,其对大规模群体进行COVID-19筛查的成本要比单独进行检测便宜20倍左右。研究者表示,应用这种新算法或能一次性对多个样本进行检测,从而就减少了所需的检测总数,并能降低人群进行COVID-19筛查的成本。
研究者表示,这种新方法或能使早期发现疾病爆发变得更加容易,而且初步研究结果也表明,当大多数人COVID-19检测结果呈现阴性时,该方法在识别阳性病例上或许会更加有效;研究者表示,这种名为超立方算法(hypercube algorithm)的新方法目前正在非洲进行首次测试。研究人员从单个棉拭子中提取少量样本,随后混合进行测试,他们表示,即使在混合了99个阴性样本后,他们也能检测到其中掺入的单个阳性样本。
如果最初的测试结果强调混合的样本中包含阳性样本的话,那么研究者就能利用新算法来设计后续的一系列实验,这样就能帮助研究者从混合样本中找到单一的阳性拭子,从而就能快速识别出感染COVID-19的个体。如果初次测试结果表明混合样本中并没有阳性样本,则研究者就不需要进行后续的测试了。研究者表示,这种新算法最适合进行一般人群的常规筛查,而并非针对单一患者,同时还能帮助明显降低人群的检测成本。
9.Nature:详细绘制新冠病毒中和抗体的结合位点,有助开发新的治疗策略
doi:10.1038/s41586-020-2852-1
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。在一项新的研究中,来自美国加州理工学院等研究机构的研究人员描述了针对这种病毒的多种抗体的特征,并鉴定出那些最有效地中和这种病毒的抗体。抗体是人体为应对感染而产生的蛋白。最终,他们希望像这项研究中描述的强效抗体可以作为治疗或预防COVID-19的药物。相关研究结果于2020年10月12日在线发表在Nature期刊上,论文标题为“SARS-CoV-2 neutralizing antibody structures inform therapeutic strategies”。论文通讯作者为加州理工学院生物学与生物工程系的Pamela Björkman教授。论文第一作者为加州理工学院生物学与生物工程系博士后研究员Christopher Barnes。
一个人可以产生数百或数千种不同的抗体变体来对抗包括病毒在内的任何病原体或外来物,这会导致个人和人群中的抗体具有广泛的多样性。有些抗体比其他抗体更能阻止病毒入侵。想一想一个拳击手与对手交手的众多方式:打脸的一拳比打腿的一拳更有可能击倒对手。当一种抗体有效地使得病毒无法感染细胞---可以说是把它击倒了--这种抗体就是所谓的“中和抗体”。
10.Nature:新冠候选疫苗BNT162b1可引发强劲的人体抗体反应和TH1 T细胞反应
doi:10.1038/s41586-020-2814-7
最近,来自美国辉瑞公司的研究人员报道了一项正在进行的安慰剂对照、观察者单盲(observer-blinded)的1/2期2019年冠状病毒病(COVID-19)疫苗(称为BNT162b1)临床试验的安全性、耐受性和抗体反应数据(Nature, 2020, doi:10.1038/s41586-020-2639-4)。该临床试验涉及45名年龄在18岁至55岁之间的健康成年人。其中的一半人被随机选择注射低、中、高剂量的BNT162b1,而另一半人注射 “假疫苗”安慰剂。它的临床结果表明这种候选疫苗在参与者中引起了强大的免疫反应,而且剂量越大,免疫反应越强。注射第二剂“加强”疫苗也会增强免疫系统的反应。
在一项新的研究中,这些研究人员在18~55岁的健康成年人中开展了第二项非随机的开放标签的BNT162b1疫苗1/2期临床试验,评估了这些参与者接种BNT162b1疫苗后的抗体反应和T细胞反应。相关研究结果于2020年9月30日在线发表在Nature期刊上,论文标题为“COVID-19 vaccine BNT162b1 elicits human antibody and TH1 T-cell responses”。
两剂1至50μg的BNT162b1引起了强劲的CD4+ T细胞反应、CD8+ T细胞反应和强烈的抗体反应,结合RBD的IgG抗体浓度明显高于COVID-19患者恢复期血清样本盘(convalescent sample panel)中的抗体浓度。第43天时的血清SARS-CoV-2中和几何平均滴度为COVID-19患者恢复期血清样本盘的0.7倍(1μg)至3.5倍(50μg)。
免疫血清广泛地中和了具有不同SARS-CoV-2刺突蛋白变体的假病毒。大多数参与者具有偏向于1型辅助性T细胞(TH1)的T细胞免疫反应,而且他们的RBD特异性的CD8+ T细胞和CD4+T细胞发生扩增。很大比例的RBD特异性CD8+ T细胞和CD4+ T细胞产生干扰素γ(IFN-γ)。
11.Nature:震惊!重症新冠肺炎的主要遗传风险因素竟来自尼安德特人
doi:10.1038/s41586-020-2818-3
在一项新的研究中,德国马克斯-普朗克进化人类学研究所的Hugo Zeberg和Svante Paabo研究了一组与感染冠状病毒SARS-CoV-2的患者住院和呼吸衰竭的风险较高有关的基因,发现一些人从尼安德特人祖先(Neanderthal ancestor)那里遗传的基因可能会增加他们罹患重症COVID-19的可能性。相关研究结果于2020年9月30日在线发表在Nature期刊上,论文标题为“The major genetic risk factor for severe COVID-19 is inherited from Neanderthals”。
这两名研究人员确定这些基因属于一个基因组合,或者说单倍型(haplotype),很可能来自尼安德特人。这种单倍型在欧洲约有16%的人口和南亚一半的人口中发现,而在非洲和东亚则不存在。(生物谷 Bioon.com)

SARS-CoV-2(之前称为2019-nCoV)的透射电镜图,图片来自NIAID RML。
2020年2月11日,世卫组织将这种疾病病重命名为2019年冠状病毒病(COVID-19)。同一天,负责分类和命名病毒的的国际病毒分类学委员会的冠状病毒研究小组在bioRxiv上发表了一篇文章,指出该研究小组已经决定,新型冠状病毒2019-nCoV是导致2002-2003年爆发严 重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)的变种。因此,将这种新病原体重新命名为严重急性呼吸综合征冠状病毒2号(severe acute respiratory syndrome coronavirus 2),或SARS-CoV-2。值得注意的一点是,尽管国际病毒分类委员会冠状病毒研究小组将 病毒命名为SARS-CoV-2,但该研究小组主席John Ziebuhr认为这个名字(SARS-CoV-2)和SARS(严重急性呼吸综合征,也称非典型肺炎)没有关联。不过,这种病毒的重新命名引起了不少争议。据《科学》网站报道,世界卫生组织不满意SARS-CoV-2这个名字,而且不打 算采用此名称。
冠状病毒可引起多种动物的多系统感染。在此之前已有6种冠状病毒可以感染人类,它们主要引起人类的呼吸道感染:两种高度致命性的冠状病毒,即严重急性呼吸道综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV);4种可导致温 和的上呼吸道疾病的冠状病毒,即HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1。
基于此次疫情给中国和全世界带来严重的危害,小编针对Nature期刊上发表的2019-nCoV/COVID-19研究进行一番梳理,以飨读者。
1.Nature:构建出SARS-CoV-2感染的人远端肺类器官模型
doi:10.1038/s41586-020-3014-1
在一项新的研究中,来自美国斯坦福大学医学院等研究机构的研究人员以成人肺泡上皮细胞II型(AT2)或KRT5+基底细胞为来源,培育出长期不含饲养细胞的化学限定性远端肺祖细胞培养物:远端肺类器官(organoid)。相关研究结果于2020年11月25日在线发表在Nature期刊上,论文标题为“Progenitor identification and SARS-CoV-2 infection in human distal lung organoids”。

图片来自Pixabay/CC0 Public Domain。
AT2细胞类器官表现出AT1转分化潜能,而基底细胞类器官产生的管腔内排列有分化的棒状细胞(club cell)和纤毛细胞。对基底细胞类器官的KRT5+基底细胞进行单细胞分析揭示了一个独特的ITGA6+ITGB4+有丝分裂细胞群体,它们的增殖可进一步产生一个TNFRSF12Ahi细胞亚群,这个细胞亚群含有大约10%的KRT5+基底细胞,簇集在终末细支气管内,并表现出丰富的克隆性类器官(clonogenic organoid)生长活性。构建出的远端肺类器官具有顶端朝外的极性,这将ACE2展示在暴露的外表面上,从而促进SARS-CoV-2感染AT2细胞和基底细胞培养物,并鉴定出棒状细胞是一个新的可被这种病毒感染的目标群体。对人远端肺进行长期不含饲养细胞的类器官培养,并结合单细胞分析,确定了未预想到的基底细胞功能异质性,并建立了一种简便的人远端肺感染(包括与COVID-19相关的肺炎)的体外类器官模型。
2.Nature:构建出一种计算机模型,可以准确预测新冠肺炎在美国10个大型城市的传播情况
doi:10.1038/s41586-020-2923-3
在一项新的研究中,来自美国斯坦福大学和西北大学的研究人员构建出一种计算机模型,并利用这种模型通过分析驱动感染风险的三个因素---人们在一天中去了哪里,停留了多长时间,以及有多少其他人在同一时间访问同一地点---准确预测了今年春天COVID-19在美国10个主要城市的传播情况。相关研究结果于2020年11月10日在线发表在Nature期刊上,论文标题为“Mobility network models of COVID-19 explain inequities and inform reopening”。
这项研究合并了人口统计学数据、流行病学估计和匿名手机位置信息,似乎证实了大多数COVID-19传播发生在“超级传染源(superspreader)”场所,比如全方位服务的餐馆、健身中心和咖啡馆,在那里,人们长时间地呆在狭小的空间里。这些研究人员说,他们的模型可以作为官员们的工具,通过揭示新感染和销售损失之间的权衡,帮助他们在重新开始营业(比如在20%或50%的营业能力下)时尽量减少COVID-19的传播。
论文共同作者、坦福大学人文与科学学院社会学教授David Grusky说,这种预测能力特别有价值,这是因为它针对少数族裔和低收入人群不成比例的感染率背后的因素提供了有用的新见解。他说,“在过去,这些差异被认为是由已存在的医疗状况和不平等的医疗服务驱动的,而我们的模型表明,人群流动模式也有助于推动这些不成比例的风险。”
3.Nature:利用K18-hACE2小鼠评估COVID-19发病机制
doi:10.1038/s41586-020-2943-z
在2003-2004年SARS流行期间,由于受感染的小鼠只产生了轻微的疾病,美国爱荷华大学的研究人员和其他人构建出表达hACE2的转基因小鼠(即K18-hACE2小鼠)。K18-hACE2小鼠在细胞角蛋白18编码基因的启动子的驱动下表达hACE2,而且主要是在上皮细胞中表达。受到SARS-CoV感染的K18-hACE2小鼠患上不好处理的脑炎和轻度肺炎。SARS-CoV-2和SARS-CoV都使用hACE2,但在患者的疾病表现中显示出差异。SARS-CoV-2感染上呼吸道的程度比SARS-CoV更大。SARS-CoV-2已经与嗅觉丧失、味觉丧失、血栓形成和肺血管内皮损伤、心脏和神经系统疾病以及儿童和青少年中的多系统炎症等临床表现相关。基于这些观察,爱荷华大学的研究人员推断SARS-CoV-2感染的K18-hACE2小鼠也可能显示出发病机制的差异。
在一项新的研究中,爱荷华大学的Paul B. McCray Jr和Stanley Perlman及其同事们展示了K18-hACE2小鼠对COVID-19疾病的研究和治疗的效用。他们发现SARS-CoV-2感染K18-hACE2小鼠会引起剂量依赖性的致死性呼吸道疾病,其特征类似于严重的人类COVID-19,包括弥漫性肺泡损伤、炎症细胞浸润、组织损伤、肺血管损伤和死亡,其中,有一部分小鼠会因出现脑部感染而死亡。相关研究结果近期发表在Nature期刊上,论文标题为“COVID-19 treatments and pathogenesis including anosmia in K18-hACE2 mice”。
SARS-CoV-2感染的K18-hACE2小鼠重现了许多在COVID-19患者中观察到的发现,因而提供了一个有用的模型来研究发病机制和评估干预措施。
4.Nature:新研究指出超过170万纽约人感染新冠病毒,而且这种病毒早在2月底就已存在于纽约
doi:10.1038/s41586-020-2912-6
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。在一项新的对今年2月初至7月采集的1万多份血浆样本进行的回顾性监测研究中,来自美国西奈山伊坎医学院的研究人员报告,SARS-CoV-2早在今年3月1日纽约市首例COVID-19病例被证实之前就已经存在于该市。他们的研究发现,超过170万纽约人---约占全市人口的20%--已经感染了这种病毒,而且这种病毒的感染死亡率接近1%,比流感的死亡率高10倍。相关研究结果于2020年11月3日在线发表在Nature期刊上,论文标题为“Repeated cross-sectional sero-monitoring of SARS-CoV-2 in New York City”。

图片来源:https://cn.bing.com。
在3月8日结束的一周内,纽约市感染病例急剧增加,随后在3月15日结束的一周内,COVID-19死亡病例大幅增加。纽约州于3月22日实施了一项待在家中的命令,此后纽约市的每日病例数开始趋于稳定,然后在4月和5月出现下降。论文共同通讯作者、西奈山伊坎医学院病理学副教授Emilia Mia Sordillo博士说,在3月初当地流行病开始出现时,几乎没有检测能力,但是,“我们如今知道许多无症状病例和轻度到中度的病例可能没有被发现。在这项新的研究中,我们旨在了解普通人群和寻求紧急护理的人的感染动态。”
5.Nature:65岁以下人群的COVID-19死亡人数更可能衡量一个国家的新冠病毒传播率
doi:10.1038/s41586-020-2918-0
在一项新的研究中,来自英国剑桥大学和法国巴斯德研究所等研究机构的研究人员发现鉴于不同国家的老年人口中报告的COVID-19死亡率存在很大差异,简单地比较不同国家的死亡总数可能会对SARS-CoV-2(一种导致COVID-19疾病的冠状病毒)的基本传播水平产生误导。相关研究结果于2020年11月2日在线发表在Nature期刊上,论文标题为“Age-specific mortality and immunity patterns of SARS-CoV-2”。
这项研究强调了欧洲养老院发生的大规模COVID-19疫情,以及一些亚洲和南美国家可能出现的失踪死亡事件,如何扭曲了老年群体的COVID-19死亡数据,使得对这一流行病规模的国家间比较不准确。这些作者表示,报告65岁以下人群死于COVID-19的情况可能要可靠得多,因此可以更清楚地了解这种病毒的基本传播情况,并能更好地进行国家间比较---这对指导政府试图控制COVID-19的策略至关重要。
6.Nature:通过构建肺部类器官和结肠类器官鉴定出新冠病毒抑制剂
doi:10.1038/s41586-020-2901-9
人们迫切需要利用人类疾病相关的细胞构建新的模型,来研究SARS-CoV-2生物学特性和促进药物筛选。鉴于SARS-CoV-2主要感染呼吸道,在一项新的研究中,来自美国威尔康奈尔医学院、芝加哥大学、哥伦比亚大学和中国上海交通大学等研究机构的研究人员利用人多能性干细胞(human pluripotent stem cell, hPSC)开发出一种肺部类器官(lung organoid)模型(下称hPSC-LO)。相关研究结果近期发表在Nature期刊上,论文标题为“Identification of SARS-CoV-2 Inhibitors using Lung and Colonic Organoids”。
hPSC-LO,特别是肺泡II型样细胞,可被SARS-CoV-2感染,并在SARS-CoV-2感染后表现出强劲的趋化因子表达,这与COVID-19患者中观察到的情况相似。这些患者中近25%的人也有胃肠道症状,这与更糟糕的COVID-19临床结果相关。与此同时,作为对hPSC-LO的补充,这些研究人员也利用hPSC构建出结肠类器官(hPSC-CO)来探究结肠细胞对SARS-CoV-2感染的反应。他们发现,多种结肠细胞类型,特别是肠上皮细胞(enterocyte),表达ACE2,并且可被SARS-CoV-2感染。
利用hPSC-LO,这些研究人员对美国食品药品管理局(FDA)批准的药物进行了高通量筛选,并鉴定出SARS-CoV-2的细胞进入抑制剂,包括伊马替尼(imatinib)、霉酚酸(mycophenolic acid, MPA)和盐酸阿的平(quinacrine dihydrochloride, QNHC)。这些药物在生理相关水平下的处理显著抑制了SARS-CoV-2对hPSC-LO和hPSC-CO的感染。
7.Nature:刺突蛋白突变D614G改变了新冠病毒的适应性
doi:10.1038/s41586-020-2895-3
在一项新的研究中,来自美国德克萨斯大学的研究人员通过基因改造让SARS-CoV-2毒株USA-WA1/2020携带D614G突变,并描述了它的影响。他们发现D614G通过提高这种毒株的感染力,增强了它在人肺上皮细胞和原代人气道组织中的复制。相关研究结果近期发表在Nature期刊上,论文标题为“Spike mutation D614G alters SARS-CoV-2 fitness”。

图片来自Nature, 2020, doi:10.1038/s41586-020-2895-3。
感染了G614变体的仓鼠在鼻腔洗液和气管中而不是在肺部中产生了较高的传染性病毒滴度,这就证实了之前的临床证据发现:D614G突变增加了COVID-19患者上呼吸道的病毒载量,并可能增加传播。
来自受到D614变体感染的仓鼠的血清对G614病毒变体的中和滴度适度高于对D614病毒变体的中和滴度,这表明(i)这种突变可能不会降低临床试验中疫苗对COVID-19的保护能力,(ii)应针对传播中的G614病毒变体进行治疗性抗体检测。结合临床发现,这项研究强调了这种突变在病毒传播、疫苗疗效和抗体治疗中的重要性。
8.Nature:一种新型筛查算法或能将COVID-19的检测成本降低20倍!
doi:10.1038/s41586-020-2885-5
近日,一项刊登在国际杂志Nature上的研究报告中,来自爱丁堡大学等机构的科学家们通过研究开发了一种新型的数学算法,其对大规模群体进行COVID-19筛查的成本要比单独进行检测便宜20倍左右。研究者表示,应用这种新算法或能一次性对多个样本进行检测,从而就减少了所需的检测总数,并能降低人群进行COVID-19筛查的成本。
研究者表示,这种新方法或能使早期发现疾病爆发变得更加容易,而且初步研究结果也表明,当大多数人COVID-19检测结果呈现阴性时,该方法在识别阳性病例上或许会更加有效;研究者表示,这种名为超立方算法(hypercube algorithm)的新方法目前正在非洲进行首次测试。研究人员从单个棉拭子中提取少量样本,随后混合进行测试,他们表示,即使在混合了99个阴性样本后,他们也能检测到其中掺入的单个阳性样本。
如果最初的测试结果强调混合的样本中包含阳性样本的话,那么研究者就能利用新算法来设计后续的一系列实验,这样就能帮助研究者从混合样本中找到单一的阳性拭子,从而就能快速识别出感染COVID-19的个体。如果初次测试结果表明混合样本中并没有阳性样本,则研究者就不需要进行后续的测试了。研究者表示,这种新算法最适合进行一般人群的常规筛查,而并非针对单一患者,同时还能帮助明显降低人群的检测成本。
9.Nature:详细绘制新冠病毒中和抗体的结合位点,有助开发新的治疗策略
doi:10.1038/s41586-020-2852-1
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。在一项新的研究中,来自美国加州理工学院等研究机构的研究人员描述了针对这种病毒的多种抗体的特征,并鉴定出那些最有效地中和这种病毒的抗体。抗体是人体为应对感染而产生的蛋白。最终,他们希望像这项研究中描述的强效抗体可以作为治疗或预防COVID-19的药物。相关研究结果于2020年10月12日在线发表在Nature期刊上,论文标题为“SARS-CoV-2 neutralizing antibody structures inform therapeutic strategies”。论文通讯作者为加州理工学院生物学与生物工程系的Pamela Björkman教授。论文第一作者为加州理工学院生物学与生物工程系博士后研究员Christopher Barnes。
一个人可以产生数百或数千种不同的抗体变体来对抗包括病毒在内的任何病原体或外来物,这会导致个人和人群中的抗体具有广泛的多样性。有些抗体比其他抗体更能阻止病毒入侵。想一想一个拳击手与对手交手的众多方式:打脸的一拳比打腿的一拳更有可能击倒对手。当一种抗体有效地使得病毒无法感染细胞---可以说是把它击倒了--这种抗体就是所谓的“中和抗体”。
10.Nature:新冠候选疫苗BNT162b1可引发强劲的人体抗体反应和TH1 T细胞反应
doi:10.1038/s41586-020-2814-7
最近,来自美国辉瑞公司的研究人员报道了一项正在进行的安慰剂对照、观察者单盲(observer-blinded)的1/2期2019年冠状病毒病(COVID-19)疫苗(称为BNT162b1)临床试验的安全性、耐受性和抗体反应数据(Nature, 2020, doi:10.1038/s41586-020-2639-4)。该临床试验涉及45名年龄在18岁至55岁之间的健康成年人。其中的一半人被随机选择注射低、中、高剂量的BNT162b1,而另一半人注射 “假疫苗”安慰剂。它的临床结果表明这种候选疫苗在参与者中引起了强大的免疫反应,而且剂量越大,免疫反应越强。注射第二剂“加强”疫苗也会增强免疫系统的反应。
在一项新的研究中,这些研究人员在18~55岁的健康成年人中开展了第二项非随机的开放标签的BNT162b1疫苗1/2期临床试验,评估了这些参与者接种BNT162b1疫苗后的抗体反应和T细胞反应。相关研究结果于2020年9月30日在线发表在Nature期刊上,论文标题为“COVID-19 vaccine BNT162b1 elicits human antibody and TH1 T-cell responses”。

图片来源:CC0 Public Domain。
两剂1至50μg的BNT162b1引起了强劲的CD4+ T细胞反应、CD8+ T细胞反应和强烈的抗体反应,结合RBD的IgG抗体浓度明显高于COVID-19患者恢复期血清样本盘(convalescent sample panel)中的抗体浓度。第43天时的血清SARS-CoV-2中和几何平均滴度为COVID-19患者恢复期血清样本盘的0.7倍(1μg)至3.5倍(50μg)。
免疫血清广泛地中和了具有不同SARS-CoV-2刺突蛋白变体的假病毒。大多数参与者具有偏向于1型辅助性T细胞(TH1)的T细胞免疫反应,而且他们的RBD特异性的CD8+ T细胞和CD4+T细胞发生扩增。很大比例的RBD特异性CD8+ T细胞和CD4+ T细胞产生干扰素γ(IFN-γ)。
11.Nature:震惊!重症新冠肺炎的主要遗传风险因素竟来自尼安德特人
doi:10.1038/s41586-020-2818-3
在一项新的研究中,德国马克斯-普朗克进化人类学研究所的Hugo Zeberg和Svante Paabo研究了一组与感染冠状病毒SARS-CoV-2的患者住院和呼吸衰竭的风险较高有关的基因,发现一些人从尼安德特人祖先(Neanderthal ancestor)那里遗传的基因可能会增加他们罹患重症COVID-19的可能性。相关研究结果于2020年9月30日在线发表在Nature期刊上,论文标题为“The major genetic risk factor for severe COVID-19 is inherited from Neanderthals”。
这两名研究人员确定这些基因属于一个基因组合,或者说单倍型(haplotype),很可能来自尼安德特人。这种单倍型在欧洲约有16%的人口和南亚一半的人口中发现,而在非洲和东亚则不存在。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


