鼻息肉(CRSwNP)新药!GSK抗炎药Nucala(美泊利单抗)第4个适应症获美国FDA受理!
来源:本站原创 2020-12-10 17:04
Nucala是全球首个IL-5靶向疗法,已获批3种嗜酸性粒细胞疾病适应症。

2020年12月10日讯 /生物谷BIOON/ ---葛兰素史克(GSK)近日宣布,美国食品和药物管理局(FDA)已受理抗炎药Nucala(mepolizumab,美泊利单抗)的一份补充生物制品许可申请(sBLA),用于治疗慢性鼻-鼻窦炎伴鼻息肉(CRSwNP)患者。
如果获得批准,Nucala将成为美国第一个获批用于治疗CRSwNP的抗IL-5生物制剂,也是唯一获批用于4种嗜酸性粒细胞驱动疾病的疗法。之前,Nucala已获批3种适应症:(1)治疗重度嗜酸性粒细胞性哮喘(SAE)患者;(2)治疗嗜酸粒细胞性肉芽肿性多血管炎(EGPA)患者;(3)治疗嗜酸性粒细胞增多综合征(HES)患者。
CRSwNP是一种主要由2型炎症引起的上呼吸道慢性疾病,特征是阻塞鼻窦和鼻道的息肉。目前的治疗选择是鼻内皮质类固醇、系统性皮质类固醇和手术,所有这些方案治疗后疗效都不理想和/或复发率高。患者可能会出现严重的鼻阻塞、呼吸困难、鼻涕、嗅觉和味觉下降或丧失、面部疼痛或压迫。CRSwNP的持续症状会对患者健康相关生活质量产生显著不利影响,包括生产力和日常生活活动降低、无法享受食物、睡眠不足和疲劳。
目前,CRSwNP治疗方面,赛诺菲/再生元抗炎药Dupixent(dupilumab,IL-4/IL-13靶向单抗)分别于2019年6月和10月获美国和欧盟批准,成为首个治疗CRSwNP的生物制剂。今年8月和12月,诺华/罗氏Xolair(中文品牌名:茁乐,通用名:omalizumab,奥马珠单抗)获得欧盟和美国批准一个新的适应症:作为鼻内皮质类固醇(INC)的附加(add-on)疗法,用于治疗采用INC不能充分控制病情的严重CRSwNP成人患者(≥18岁),该批准使Xolair成为首个专门靶向和阻断免疫球蛋白E(IgE)治疗鼻息肉的生物制剂。
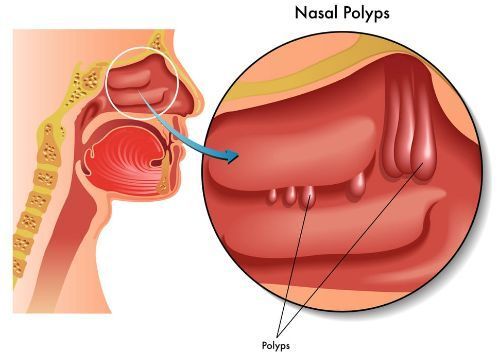
鼻息肉(图片来源:myhealthandwellnessinfo.com)
如果获得批准,Nucala将与Dupixent和Xolair展开竞争。Nucala的监管申请文件,基于关键III期SYNAPSE研究的阳性结果。这是首次一种抗IL-5生物制剂在治疗CRSwNP方面报告阳性III期数据,增加了Nucala拥有有效数据的嗜酸性粒细胞驱动疾病范围。
特别值得一提的是,SYNAPSE研究入组的患者全部有过手术史(大约三分之一的患者有过3次以上的手术)、并且由于严重的症状和增大的息肉而需要进一步手术,该研究是第一项评估生物制剂在这类严重患者人群中治疗益处的临床研究。
SYNAPSE是一项为期52周的随机、双盲、平行组III期研究,入组了400多例反复性严重双侧鼻息肉成人患者,评估了Nucala与安慰剂分别联合标准护理(SoC)的疗效和安全性。研究中,这些患者被随机分配,接受Nucala(100mg液体制剂)或安慰剂,同时接受SoC。Nucala和安慰剂均采用预充式注射器进行皮下注射,每4周一次,治疗52周。严重双侧鼻息肉患者被定义为平均鼻塞视觉模拟量表(VAS)症状评分>5分、内镜评分至少为5分(最高评分为8分)、每个鼻腔最低评分为2分。患者必须在过去的10年中至少有一次鼻息肉手术史,尽管按照标准护理进行治疗,但仍有反复性鼻息肉,并且目前需要鼻息肉手术。
结果显示,该研究达到了2个共同主要终点:与SoC+安慰剂组相比,SoC+Nucala治疗组在第52周时鼻息肉的体积(p<0.001)和第49-52周鼻塞(p<0.001)均有统计学上的显著改善:(1)鼻内窥镜下鼻息肉总分与基线的中位数变化差异为-0.73(95%CI:-1.11,-0.34);(2)鼻塞视觉模拟量表(VAS)评分与基线的中位数变化差异为-3.14(95%CI:-4.09,-2.18)。关键次要终点方面:52周期间进行第一次实际鼻腔手术时间也具有统计学显著差异;与SoC+安慰剂组相比,SoC+Nucala治疗组进行第一次实际鼻腔手术时间推迟了57%(p=0.003;95%CI:0.43[0.25,0.76])。研究中的安全性结果与Nucala已知的安全特征一致。
Nucala于2015年底首次被批准用于治疗重度嗜酸性粒细胞哮喘(SEA),是全球上市的首个靶向IL-5的生物疗法。Nucala的活性药物成分mepolizumab是一种特异性靶向白细胞介素5(IL-5)的单克隆抗体。IL-5是一种细胞因子,能够调节嗜酸性粒细胞(一种白细胞)的生长、活化、存活,并能够为嗜酸性粒细胞从骨髓迁移至肺部及其他器官提供重要的信号。Nucala与人IL-5结合,阻断IL-5与嗜酸性粒细胞表面受体的结合。以这种方式抑制IL-5对受体的结合作用,能够降低血液、组织、痰液中的嗜酸性粒细胞水平,这反过来又能够降低嗜酸性粒细胞所介导的炎症。
基于上述作用机制,Nucala正被开发用于多种由嗜酸性粒细胞引起的炎症所致的疾病。该药已在21个临床试验、超过3000例患者、横跨多种嗜酸性粒细胞适应症进行了评估。
截止目前,Nucala已获美国、欧洲以及其他20个其他市场批准,作为一种附加维持疗法治疗重度嗜酸性粒细胞性哮喘(SAE)成人患者。在美国和欧盟以及其他几个市场,Nucala还被批准用于治疗6-17岁重度嗜酸性粒细胞性哮喘(SAE)儿科患者。此外,在美国、日本、加拿大等多个市场,Nucala也已被批准作为作为一种附加维持疗法治疗嗜酸粒细胞性肉芽肿性多血管炎(EGPA)成人患者。今年9月,美国FDA批准Nucala用于治疗嗜酸性粒细胞增多综合征(HES)。除了CRSwNP外,GSK目前也正在评估Nucala治疗慢性阻塞性肺病(COPD)的潜力。(生物谷Bioon.com)
原文出处:FDA accepts GSK’s filing of Nucala (mepolizumab) for use in chronic rhinosinusitis with nasal polyps
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


