Nature子刊:利用免疫正交直向同源物有望提高CRISPR-Cas9基因组编辑效率
来源:本站原创 2019-08-22 20:47
2019年8月22日讯/生物谷BIOON/---近年来,进入临床试验的蛋白治疗剂的数量急剧增加。这类治疗剂的一个重要限制是它们可能是宿主适应性免疫系统的靶标。业已存在的免疫力和治疗诱导的免疫应答都能够潜在地降低治疗效果。鉴于CRISPR-Cas9的功效和高通量能力,它引发了基因组编辑领域的变革。一项利用CRISPR-Cas9介导的基因组编辑的临床试验于今年年初开始,并且还将有更多的临床试验。然而,
2019年8月22日讯/生物谷BIOON/---近年来,进入临床试验的蛋白治疗剂的数量急剧增加。这类治疗剂的一个重要限制是它们可能是宿主适应性免疫系统的靶标。业已存在的免疫力和治疗诱导的免疫应答都能够潜在地降低治疗效果。
鉴于CRISPR-Cas9的功效和高通量能力,它引发了基因组编辑领域的变革。一项利用CRISPR-Cas9介导的基因组编辑的临床试验于今年年初开始,并且还将有更多的临床试验。然而,人们仍然关注Cas9蛋白在人体中的潜在免疫原性,特别是腺相关病毒(AAV)载体介导的Cas9递送在体内的应用。最近,几个独立的研究团队报道了人体对Cas9蛋白的免疫力早已存在。幸运的是,科学家们在自然界中发现了来自不同细菌物种的几种Cas9变体(Cas9的直向同源物)。
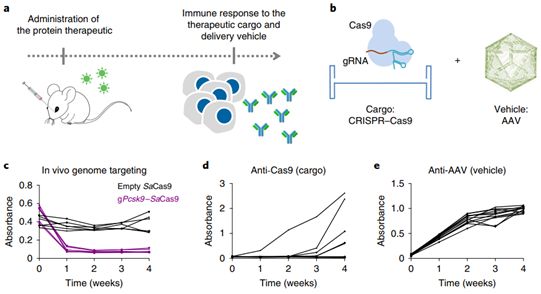
考虑到这些因素,Moreno及其同事们在一项新的研究中,通过预测Cas9变体和AAV各自的氨基酸序列对主要组织相容性复合物I型(MHCI)和II型(MHCII)的结合能力来分析它们的免疫正交性(immune-orthogonality)。通过使用Cas9和AAV的免疫正交直向同源物(immune-orthogonal ortholog),它们在预先接受Cas9蛋白免疫的动物中实现了高效的基因组编辑。有趣的是,预先免疫仅导致编辑效率的部分降低,这表明抗Cas9适应性免疫应答在体内的影响是有限的。
然而,这项研究的一个重要限制是使用与人类相比具有有限MHC谱系的近交小鼠。这些研究人员承认,鉴于不同AAV衣壳之间的高度保守性和人群中众多MHC免疫基因的存在,使用免疫正交直向同源物可能是降低人类抗衣壳免疫原性的一个较差的解决方案。Cas9在体内的使用可能存在类似的限制。然而,细菌中Cas9的进化具有较长的历史,并且每个月从不同的细菌菌株中分离出新的Cas9变体。降低对Cas9产生适应性免疫应答的风险的另一种可能的解决方案是通过mRNA或蛋白递送实现Cas9核酸酶的瞬时表达。
自然界中存在的Cas9蛋白的免疫正交性似乎提供了一种解决方案来潜在地降低预先存在的和治疗后产生的免疫应答对基因组编辑功效的影响。如果在具有更大MHC谱的动物模型中得到证实,那么这种方法可以允许利用基因组编辑对体细胞进行修饰和在体内校正人类的基因突变。(生物谷 Bioon.com)
参考资料:
1.Ana M. Moreno et al. Immune-orthogonal orthologues of AAV capsids and of Cas9 circumvent the immune response to the administration of gene therapy. Nature Biomedical Engineering, 2019, doi:10.1038/s41551-019-0431-2.
2.Giuseppe Ronzitti. Immune-orthogonal orthologs: The solution for genome editing?. Science Translational Medicine, 2019, doi:10.1126/scitranslmed.aay7701.
鉴于CRISPR-Cas9的功效和高通量能力,它引发了基因组编辑领域的变革。一项利用CRISPR-Cas9介导的基因组编辑的临床试验于今年年初开始,并且还将有更多的临床试验。然而,人们仍然关注Cas9蛋白在人体中的潜在免疫原性,特别是腺相关病毒(AAV)载体介导的Cas9递送在体内的应用。最近,几个独立的研究团队报道了人体对Cas9蛋白的免疫力早已存在。幸运的是,科学家们在自然界中发现了来自不同细菌物种的几种Cas9变体(Cas9的直向同源物)。

图片来自Nature Biomedical Engineering, 2019, doi:10.1038/s41551-019-0431-2。
考虑到这些因素,Moreno及其同事们在一项新的研究中,通过预测Cas9变体和AAV各自的氨基酸序列对主要组织相容性复合物I型(MHCI)和II型(MHCII)的结合能力来分析它们的免疫正交性(immune-orthogonality)。通过使用Cas9和AAV的免疫正交直向同源物(immune-orthogonal ortholog),它们在预先接受Cas9蛋白免疫的动物中实现了高效的基因组编辑。有趣的是,预先免疫仅导致编辑效率的部分降低,这表明抗Cas9适应性免疫应答在体内的影响是有限的。
然而,这项研究的一个重要限制是使用与人类相比具有有限MHC谱系的近交小鼠。这些研究人员承认,鉴于不同AAV衣壳之间的高度保守性和人群中众多MHC免疫基因的存在,使用免疫正交直向同源物可能是降低人类抗衣壳免疫原性的一个较差的解决方案。Cas9在体内的使用可能存在类似的限制。然而,细菌中Cas9的进化具有较长的历史,并且每个月从不同的细菌菌株中分离出新的Cas9变体。降低对Cas9产生适应性免疫应答的风险的另一种可能的解决方案是通过mRNA或蛋白递送实现Cas9核酸酶的瞬时表达。
自然界中存在的Cas9蛋白的免疫正交性似乎提供了一种解决方案来潜在地降低预先存在的和治疗后产生的免疫应答对基因组编辑功效的影响。如果在具有更大MHC谱的动物模型中得到证实,那么这种方法可以允许利用基因组编辑对体细胞进行修饰和在体内校正人类的基因突变。(生物谷 Bioon.com)
参考资料:
1.Ana M. Moreno et al. Immune-orthogonal orthologues of AAV capsids and of Cas9 circumvent the immune response to the administration of gene therapy. Nature Biomedical Engineering, 2019, doi:10.1038/s41551-019-0431-2.
2.Giuseppe Ronzitti. Immune-orthogonal orthologs: The solution for genome editing?. Science Translational Medicine, 2019, doi:10.1126/scitranslmed.aay7701.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


