全球血友病基因疗法!valrox遭美国FDA拒绝批准,单次输注3年后年出血率减少96%!
来源:本站原创 2020-08-20 15:30
valrox正在接受欧盟的加速审批,有潜力成为全球第一个血友病基因疗法。
2020年08月20日讯 /生物谷BIOON/ --BioMarin是一家全球性的生物技术公司,专注于开发治疗严重且危及生命的罕见和超罕见遗传疾病的创新疗法。近日,该公司宣布,美国食品和药物管理局(FDA)已针对其基因疗法valoctocogene roxaparvovec(valrox,BMN270)治疗重度A型血友病成人患者的生物制品许可申请(BLA)发布了一份完整回应函(CRL)。值得一提的是,valrox是美国FDA受理的首个血友病基因疗法,但CRL意味着BLA审查周期已经完成,并且该BLA以目前的形式不能获得批准。
此前,BioMarin与FDA就支持BLA所需数据的范围达成了一致意见。现在,FDA对该公司正在进行的270-301研究(III期)中的两年数据提出了新的建议,将年化出血率(ABR)为主要终点,以提供持久效果的实质证据。该机构在CRL中第一次通知公司这一建议,但在开发或审查期间的任何时候都没有提出这一建议。该机构建议该公司完成这项III期,并提交所有研究参与者的两年随访安全性和有效性数据。FDA的结论是,270-201研究(I/II期)和III期研究之间的差异限制了其依靠I/II期研究来支持疗效持久性的能力。III期研究于2019年11月完成患者入组,最后一例患者将于2021年11月完成2年随访。
BioMarin计划在未来几周与FDA会面,就支持批准的下一步达成一致意见。BioMarin董事长兼首席执行官Jean-Jacques Bienaimé表示:“我们仍然致力于血友病社区,并引领A型血友病有史以来的第一个基因疗法。我们感到惊讶和失望的是,FDA首次在CRL中提出了新的期望。我们对valrox基因疗法及其重新定义A型血友病患者治疗模式的潜力充满信心。”
目前,valrox治疗重度A型血友病成人患者的营销授权申请(MAA)正在接受欧洲药品管理局(EMA)的加速评估,这也是在欧洲进入审查的针对任何类型血友病基因治疗的第一份上市申请。
如果获得批准,valrox将成为全球第一种治疗任何类型血友病的基因疗法。此前,valrox已被FDA授予突破性药物资格(BTD)、被EMA授予优先药物资格(PRIME)、被FDA和EMA授予了孤儿药资格(ODD)。
A型血友病也被称为因子VIII(FIII)缺乏或经典血友病,是一种由凝血因子VIII缺失或缺陷引起的X连锁遗传病,患者会反复发生持续或自发性出血,特别是在关节、肌肉或内脏器官中,长期可导致残疾。目前,重度A型血友病的护理标准是每周2-3次静脉输注凝血因子VIII的预防性治疗方案。
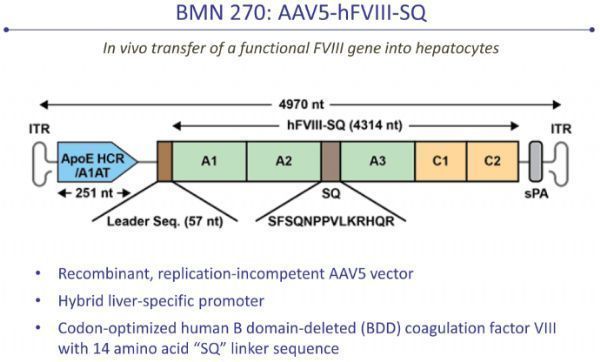
valrox是一种基于腺相关病毒(AAV)的基因疗法,开发用于A型血友病的治疗。该疗法通过向患者体内递送凝血因子VIII功能基因,恢复VIII的产生,从而消除或减少静脉VIII输注需求。如果获批,valrox将标志着A型血友病治疗的一个重大里程碑,这种开创性的疗法,有潜力使患者实现“一劳永逸”的治疗效果。
valrox的监管申请,基于III期研究的中期分析(使用拟商业化工艺生产的valrox对受试者进行了治疗)和来自I/II期研究的三年数据。
2019年5月底,BioMarin公司宣布,valrox治疗重度A型血友病达到了美国和欧盟监管审查的预先规定的临床标准。截至2019年5月28日,在III期GENEr8-1研究的20-patient队列中,有8例患者在第23-26周时达到凝血因子VIII活性水平≥40国际单位/分升(IU/dL)的预先规定标准。
2019年7月,在第27届国际血栓与止血学会(ISTH)2019年大会上,BioMarin公司公布了正在进行的I/II期研究6e13 vg/kg剂量队列的最新数据。
结果显示,单次给药valrox后,出血率控制和因子VIII使用减少在第三年继续维持。在研究开始前,患者平均年出血率(ABR)为16.3次、中位ABR为16.5次;三年后,平均ABR降至0.6次,中位ABR为0。这意味着,患者的平均ABR降低了96%,目标关节出血100%消除。在三年内,患者平均年化因子VIII使用率也降低了96%,所有患者继续保持无需因子VIII预防性治疗。患者因子VIII水平在三年内维持足以达到显著的止血效果。因子VIII的表达已经进入一个平稳期,下降的速度已经大大减缓,这可能实现持久的、长期的表达。(生物谷Bioon.com)
原文出处:BioMarin Receives Complete Response Letter (CRL) from FDA for Valoctocogene Roxaparvovec Gene Therapy for Severe Hemophilia A
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



