刷新当前科学认知!揭示那些科学家们获得的“首次”研究发现!
来源:本站原创 2020-08-21 13:09
本文中,小编整理了多篇研究成果,揭示那些科学家们获得的“首次”研究发现!与大家一起学习!图片来源:Forschungszentrum Juelich/Katrin Amunts【1】Science:首次构建出人脑细胞结构数字图谱—Julich-Braindoi:10.1126/science.abb4588ulich-Brain是第一个人脑三维图谱的名称,它
本文中,小编整理了多篇研究成果,揭示那些科学家们获得的“首次”研究发现!与大家一起学习!
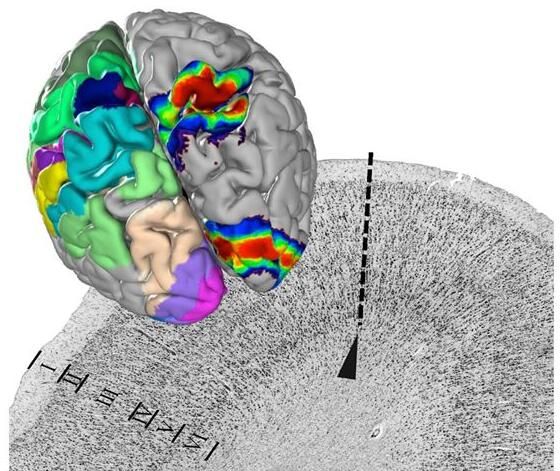
图片来源:Forschungszentrum Juelich/Katrin Amunts
【1】Science:首次构建出人脑细胞结构数字图谱—Julich-Brain
doi:10.1126/science.abb4588
ulich-Brain是第一个人脑三维图谱的名称,它以微观分辨率反映了大脑结构的变化。该图谱有近250个结构不同的区域,每个区域都是基于对10个大脑的分析。24000多张极薄的大脑切片由专家们进行数字化处理、三维组装和绘制图谱。作为欧洲人脑计划(European Human Brain Project)的EBRAINS研究基础设施的一部分,该图谱作为一个接口,以空间精确的方式连接关于大脑的信息。由Katrin Amunts博士领导的一个研究小组在Science期刊上发表了这个新型大脑图谱。
在显微镜下,可以看到人脑的结构并不统一,而是被划分为清晰可辨的区域。这些区域在神经细胞的分布和密度以及功能上都有所不同。借助于Julich-Brain,这个研究小组如今提出了最全面的大脑细胞结构数字图谱,并通过EBRAINS研究基础设施向全世界提供。研究者表示,一方面,这个数字大脑图谱将有助于更准确地解读神经影像学研究的结果,比如对患者的神经影像学研究。另一方面,它正在成为大脑'谷歌地球'的基础--这是因为细胞水平是连接关于大脑非常不同方面的数据的最佳接口。
【2】Cell:重磅!首次发现大脑中存在少量辅助性T细胞,并揭示它们在大脑发育中的新作用
doi:10.1016/j.cell.2020.06.026
大脑中是否能发现白细胞一直存在争议,它们可能发挥什么作用在此之前完全是个谜。在一项新的开创性研究中,来自比利时VIB大脑与疾病研究中心、鲁汶大学和英国巴布拉汉研究所的研究人员描述了在小鼠和人类大脑中发现的一个专门的大脑驻留免疫细胞群体,并发现白细胞的存在对小鼠大脑的正常发育至关重要,相关研究结果发表在Cell期刊上。
就像一个高度设防的总部,我们的大脑通过血脑屏障享有特殊的保护,不受身体其他部位循环的东西影响。这个高度选择性的边界确保了从血液到大脑的通道受到严格的控制。血脑屏障也将大脑与我们身体的免疫系统分隔开来,这就是为什么大脑也有它自己的称为小胶质细胞的驻留免疫细胞,它们可触发炎症和组织修复。小胶质细胞在胚胎发育过程中到达大脑,之后,它们会自我更新。
然而,作为我们免疫系统的一部分,白细胞已经被发现在不同的脑部疾病中发挥作用,包括多发性硬化症、阿尔茨海默病和帕金森病或中风。白细胞是否也能在健康的大脑中找到,以及它们在那里可能发挥何种作用,一直是人们激烈争论的主题。由Liston教授领导的一个跨学科研究团队开始寻找答案。
【3】Cell:科学家首次利用DNA条形码成功绘制出大脑的连接图谱
doi:10.1016/j.cell.2020.05.029
近日,一项刊登在国际杂志Cell上的研究报告中,来自冷泉港实验室等机构的科学家们通过研究成功利用DNA测序技术有效绘制出了大脑不同区域之间的远程连接图谱,相比传统基于显微镜的方法而言,这种新方法能够明显降低绘制大脑广泛连接图谱的成本。
研究者Longwen Huang博士表示,神经科学家们需要解剖学图谱来理解大脑中的信息如何从一个区域流向另一个区域,绘制大脑不同部位的细胞连接图谱(即大脑连接组,connectome)就能帮助揭示神经系统如何加工信息,以及错误的连线如何诱发精神性疾病等其它疾病,绘制这些图谱既昂贵又费时,需要科学家们大量的努力,而这对于很多研究团队而言也是遥不可及的。
【4】Science:重大进展!首次发现组蛋白H3-H4四聚体是一种铜还原酶
doi:10.1126/science.aba8740
在一项新的研究中,来自美国加州大学洛杉矶分校的研究人员发现组蛋白H3-H4四聚体是一种铜还原酶,相关研究结果发表在Science期刊上,在这篇论文中,他们描述了他们开展的两项实验,实验结果显示组蛋白H3-H4四聚体参与了细胞内部铜的还原。组蛋白是存在于真核细胞内部的蛋白。之前的研究已表明,它们的主要功能是将DNA结构排列成核小体。它们的作用是充当DNA螺旋缠绕的线轴,使之能够适应细胞核内部。在这项新的研究中,这些研究人员发现组蛋白还有另一个功能:将铜离子从有毒的形式还原成一种可以安全存在于细胞内的形式。
这些研究人员在开始他们的研究时指出,几十年前,其他的科学家们就已发现,在细胞内部两种组蛋白相遇的地方,成对的组氨酸和半胱氨酸氨基酸可能与金属离子结合。这提示着组蛋白可能在让人体安全使用铜方面发挥了作用。为了测试这个想法,他们设置并进行了两个都涉及酵母细胞的实验。第一个实验涉及他们在之前的研究中提出的区域内让组蛋白的氨基酸序列发生突变。他们发现,具有突变组蛋白的细胞具有较低水平的Cu(I)离子,这是铜的安全形式。他们认为,这是组蛋白在这种还原过程中发挥作用的证据。在第二个实验中,他们在试管中测试了组蛋白H3-H4四聚体,发现它们确实能将Cu(II)还原成Cu(I)。
【5】Science:新研究首次确定麻疹病毒的起源,从而为探究COVID-19起源提供信息
doi:10.1126/science.aba9411
在一项新的研究中,来自德国、比利时、美国和法国的研究人员解决了麻疹首次出现的时间这个有争议的问题,发现它可能与大城市的崛起有关。他们对来自1912年的一种麻疹病毒毒株的基因组进行了测序,并反向评估了这种病毒可能在人类群体中出现的时间,并将它确定在公元前6世纪左右,相关研究结果发表在Science期刊上。
研究者表示,从在环境中迅速降解的麻疹病毒等RNA病毒中获取基因组数据仍然极具挑战性。Ariane Düx、Sébastian Calvignac-Spencer及其同事们对这种麻疹基因组的测序是一项巨大的成就。要准确地确定病毒和细菌等病原体何时何地跳跃到人类中是非常困难的。有时这些跳跃发生了,它们就会消失。但有时它们会站稳脚跟并在全球范围内传播。对于任何一种特定的病原体来说,跳跃的时间一定发生在两个时间点之间:它从亲缘关系最近的已知亲属中分离出来的时间和我们观察人类中的这种病原体并追溯到共同祖先的谱系的时间。
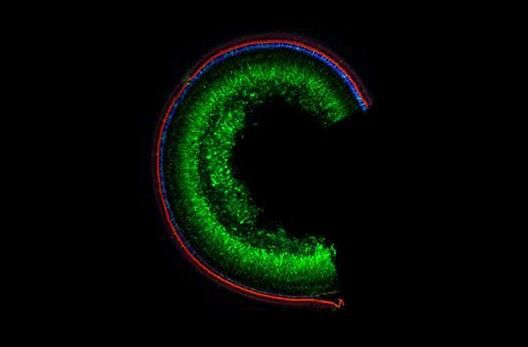
图片来源:Science Translational Medicine, 2020, doi:10.1126/scitranslmed.aay9101
【6】Science子刊:世界上首次!在体内利用碱基编辑器让隐性遗传性耳聋小鼠恢复部分听力
doi:10.1126/scitranslmed.aay9101
当Wei Hsi Yeh还是一名年轻的本科生时,她的一位男性好友在一个月的时间里,从正常听力变成了全聋。他当时29岁。没有人知道他为什么会失去听力,医生至今也不知道。Yeh上个月刚从美国哈佛大学获得化学博士学位,她的好友失去听力让她感到沮丧和恐惧。她的研究生生涯致力于解决听力丧失背后的巨大遗传之谜。在美国,每8个12岁或以上的人中,就有1个双耳听力丧失。虽然助听器和人工耳蜗等技术可以放大声音,但是它们无法纠正这个问题。但是,鉴于遗传异常导致了一半的听力丧失病例,基因编辑或许可以做到这一点。两年前,Yeh和美国布罗德研究所成员David R. Liu教授首次在小鼠模型中修复一种显性突变并阻止听力丧失。但是,Liu说,“大多数遗传疾病不是由显性突变引起的,而是由隐性突变引起的,包括大多数遗传性听力丧失。
如今,在一项新的研究中,Liu、Yeh和来自哈佛大学、布罗德研究所和霍华德休斯医学研究所的研究人员取得了另一个“第一”:他们恢复了因TMC1隐性突变而全聋的小鼠的部分听力,这是利用基因组编辑修复隐性致病突变的第一个成功例子。相关研究结果发表在Science Translational Medicine期刊上。显性致病突变,指的是仅破坏了人体两个基因拷贝中的一个拷贝的突变而使得在某些方面更容易被攻击。敲除不好的基因拷贝,好的基因拷贝就可以来拯救。Liu 说,“但是,对于隐性疾病来说,你不能这样做。根据定义,隐性等位基因意味着你有两个不好的基因拷贝。因此,你不能仅破坏不好的拷贝。你必须修复一个或两个不好的拷贝。”
【7】Nature:重磅!科学家首次揭示人类机体制造甘油三酯的分子机理!
doi:10.1038/s41586-020-2280-2
医生经常会提醒病人,机体甘油三酯(一种主要的膳食脂肪)水平较高会增加心脏病、糖尿病、肥胖和脂肪肝的风险,因此研究人员非常感兴趣寻找新方法来有效调节机体血液中的甘油三酯水平,从而控制这种可能危及机体生命的常见疾病。近日,一项刊登在国际杂志Nature上的研究报告中,来自贝勒医学院等机构的科学家们通过研究揭示了二酰甘油 O-酰基转移酶-1(DGAT1)的3D结构和作用方式,这种酶类能帮助合成甘油三酯,对于人类膳食脂肪的吸收和储存非常重要;DGAT1同时也被认为是治疗肥胖和其它代谢性疾病的重要靶点,因此详细理解DGAT1的结构或有望帮助研究人员开发治疗多种人类疾病的新型疗法。
研究者Ming Zhou指出,DGAT1是科学家们非常感兴趣的酶类,因为其能帮助合成甘油三酯,其是机体硬脂肪的主要成分,而硬脂肪通常存在于腹部或腰部中段,同时甘油三酯也是运输胆固醇颗粒的一部分,胆固醇包括有益胆固醇(高密度脂蛋白)和有害胆固醇(低密度脂蛋白),因此,学会如何调节DGAT1酶类或能帮助调节机体的脂肪合成并潜在管理其它可能的疾病。
【8】Nature:推翻此前理论!最新研究首次揭示细菌细胞壁的精细化结构 有望彻底解决抗生素耐药性问题!
doi:10.1038/s41586-020-2236-6
近日,一项刊登在国际杂志Nature上的研究报告中,来自谢菲尔德大学等机构的科学家们通过研究揭示了细菌细胞壁结构的首张高分辨率图像,相关研究结果对于阐明抗生素耐药性产生的分子机制至关重要。文章中,研究者揭示了金黄色葡萄球菌细菌外膜的新型重要结构,相关研究结果对于理解细菌生长及抗生素的作用机制都很关键,同时其也推翻了此前关于细菌外膜结构的相关理论;研究者所获得的图像能帮助他们深入理解细菌细胞壁的组成,并未开发新型抗生素来抵御抗生素耐药性提供帮助。
研究者Laia Pasquina Lemonche博士表示,很多抗生素能通过抑制细菌细胞壁的产生来发挥作用,细胞壁是细菌周围一层坚固但能渗透的外膜结构,其对于细菌生存至关重要;目前我们并不是非常清楚诸如青霉素等抗生素如何杀灭细菌,但这并不奇怪,因为到目前为止,研究人员对细菌细胞壁的实际结构并不是非常清楚,而本文研究为研究人员更好地理解抗生素的作用机制提供了新的线索和基础,并为后期开发新方法来抵御抗生素耐药性提供了新思路。
【9】Nature:重磅!科学家首次绘制出全球最大的人类蛋白质互作组图谱—HuRI!
doi:10.1038/s41586-020-2188-x
人体由数十亿个细胞组成,每个细胞都能通过其分子部分之间无数的相互作用而形成和维持,但哪些相互作用能维持机体健康?,哪些相互作用出错时会引发疾病?人类基因组计划为我们提供了一份细胞“部件列表”,只有当我们更好地理解了这些部分之间相互作用连接的机制,我们或许才能理解细胞到底是如何工作的,以及发生疾病时细胞到底哪些方面出了错?
近日,一篇发表在国际杂志Nature上的研究报告中,来自多伦多大学等机构的科学家们就通过研究绘制出了世界上最大的蛋白质互联/互作图谱,其或许对于揭示如何维持机体健康并阐明引发疾病的原因至关重要。研究者Marc Vidal表示,如今很多科学家需要一张基因编码蛋白的相互作用组(interactome)图谱,从上世纪90年代中期以来,我们就一直在推动这一理念,即利用互作组图谱来阐明生命的方方面面。
【10】Nature:突破!首次观察到神经变性疾病罪魁祸首tau蛋白在神经元细胞间来回穿梭的过程!
doi:10.1038/s41586-020-2156-5
在抵御诸如额颞叶痴呆等神经变性疾病的斗争中,tau蛋白或许就是最大的罪魁祸首,tau蛋白在脑细胞中大量存在,其能维持神经元的结构和稳定性,并帮助将营养物质从细胞的一个部分运输到另一个部分。当tau蛋白发生错误折叠时所有都会发生改变,其会变得粘性且不溶,不断聚集并在神经元中形成神经原纤维缠结,破坏神经元的功能并导致细胞最后死亡,更糟糕的是,神经元细胞中只需要相对少量的错误折叠的tau蛋白就能使附近细胞编程功能失调死亡的脑细胞。日前,一项刊登在国际杂志Nature上的研究报告中,来自加利福尼亚大学等机构的科学家们通过研究揭开了tau蛋白在神经元细胞之间来回穿梭的分子机制,相关研究结果不仅揭示了科学家们广泛研究的神经变性疾病中tau蛋白的传播,也为有效控制病理性tau蛋白的产生提供了新的思路和希望。
研究者Kosik表示,tau蛋白在细胞之间来回穿越的机制或提供了一种线索,来帮助我们开发新方法来有效阻断tau蛋白的扩散,tau蛋白来回穿梭过程中必不可少的一个“选手”就是名为LRP1(low density lipoprotein receptor-related protein 1)的低密度脂蛋白,其位于脑细胞膜上,主要参与多种机体生物学过程,同时还能帮助神经元摄取胆固醇等。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


