肺癌精准治疗!美国FDA批准默克Tepmetko:全球治疗METex14跳跃改变NSCLC的口服MET抑制剂
来源:本站原创 2021-02-06 23:00
2020年3月,Tepmetko在日本获得全球首批。

2021年02月06日讯 /生物谷BIOON/ --默克(Merck KGaA)近日宣布,美国食品和药物管理局(FDA)已批准靶向抗癌药Tepmetko(tepotinib),该药是一种高度选择性、每日一次的口服MET抑制剂,用于治疗携带MET基因第14号外显子跳过改变(METex14 skipping)的晚期非小细胞肺癌(NSCLC)成人患者。Tepmetko通过FDA实时肿瘤学审查(RTOR)试点项目获得优先审查和加速批准。该批准基于总缓解率和缓解持续时间数据,针对该适应症的持续批准将取决于验证性试验中对临床益处的验证和描述。
2020年3月,Tepmetko在日本获得全球首个监管批准,用于治疗携带METex14跳过改变的不可切除性、晚期或复发性NSCLC患者。2020年11月,欧洲药品管理局(EMA)受理了Tepmetko的申请并已启动审查程序。
值得一提的是,Tepmetko是全球第一个被批准用于治疗携带MET基因改变的晚期NSCLC患者的口服MET抑制剂。在日本,Tepmetko被授予了孤儿药资格(ODD)和SAKIGAKE资格(创新药物)。在美国,Tepmetko被授予了孤儿药资格(ODD)和突破性药物资格(BTD)。
Tepmetko也是美国FDA批准用于治疗携带METex14跳过改变转移性NSCLC患者的第一款和唯一一款每日口服一次的MET抑制剂。2020年9月,诺华靶向抗癌药Tabrecta(capmatinib)获批,是FDA批准的第一款治疗携带METex14跳过改变转移性NSCLC成人患者的MET抑制剂。
Tepmetko和Tabrecta均被批准用于:先前没有接受过治疗(一线)的患者和先前接受过治疗(经治)的患者。用药方面,Tepmekto每日口服一次,而Tabrecta每日口服2次。
Tepmetko的监管批准,基于关键II期VISION研究(NCT02864992)的数据。这是迄今为止在携带METex14跳过改变的转移性NSCLC患者中开展的最大规模临床研究,共有152例携带METex跳过改变的NSCLC患者接受了Tepmetko治疗。
结果显示:Tepmetko在先前没有接受过治疗的患者(n=69,初治组)和先前接受过治疗的患者(n=83,经治组)中的总缓解率(ORR)分别为43%(99%CI:32-56)和43%(95%CI:33-55)、2组的中位缓解持续时间(DOR)分别为10.8个月和11.1个月、2组缓解时间≥6个月的患者比例分别为67%和75%、缓解时间≥9个月的患者比例分别为30%和50%。
安全人群包括255例METex14跳过改变阳性NSCLC患者,他们在VISION研究中接受了Tepmetko治疗。1例(0.4%)死于肺炎,1例(0.4%)死于肝功能衰竭,1例(0.4%)死于液体过量引起的呼吸困难。45%接受Tepmetko治疗的患者出现严重不良反应。发生率>2%的严重不良反应,包括胸腔积液(7%)、肺炎(5%)、水肿(3.9%)、呼吸困难(3.9%)、全身健康恶化(3.5%)、肺栓塞(2%)和肌肉骨骼疼痛(2%)。服用Tepmetko的患者最常见的不良反应(≥20%)是水肿、疲劳、恶心、腹泻、肌肉骨骼疼痛和呼吸困难。
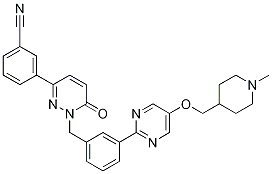
tepotinib分子结构式(图片来源:chemicalbook.com)
在全球范围内,肺癌是最常见的癌症类型,也是癌症死亡的首要原因,每年确诊200万例,死亡170万例。目前,在多种类型癌症中,已发现了3种MET信号通路改变(包括METex14跳跃改变、MET扩增、MET蛋白过度表达),这与肿瘤的侵袭行为和不良的临床预后相关。据估计,MET信号通路改变发生在3-5%的NSCLC病例中。
tepotinib是默克内部发现的一种口服MET激酶抑制剂,可强效、高度选择性抑制由MET(基因)改变——包括METex14跳跃改变、MET扩增、MET蛋白过度表达——引起的致癌信号,具有改善携带这些特定MET改变的侵袭性肿瘤患者治疗预后的潜力。除了NSCLC之外,默克也正在积极评估tepotinib联合新疗法治疗其他肿瘤适应症。
2019年9月,美国FDA授予tepotinib突破性药物资格(BTD),用于治疗接受含铂化疗后病情进展、携带METex14跳跃改变的转移性NSCLC患者。
目前,默克也在开展另一项研究INSIGHT 2(NCT03940703)评估tepotinib与酪氨酸激酶抑制剂(TKI)osimertinib联合用药方案,用于对先前接受的EGFR TKI存在获得性耐药的EGFR突变、MET扩增、局部晚期或转移性NSCLC患者。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


