HER2阳性胃癌一线免疫治疗!默沙东Keytruda(可瑞达)+曲妥珠单抗+化疗方案获美国FDA批准!
来源:本站原创 2021-05-06 23:57
Keytruda是第一个被批准与曲妥珠单抗和化疗联合应用一线治疗HER2阳性胃癌或GEJ腺癌的抗PD-1疗法。

2021年05月06日讯 /生物谷BIOON/ --默沙东(Merck & Co)近日宣布,美国食品和药物管理局(FDA)已批准抗PD-1疗法Keytruda(可瑞达®,通用名:pembrolizumab,帕博利珠单抗),联合曲妥珠单抗(trastuzumab)及含氟嘧啶和铂类药物化疗,一线治疗局部晚期不可切除性或转移性HER2阳性胃癌或胃食管交界(GEJ)腺癌患者。
值得一提的是,Keytruda是第一个被批准与曲妥珠单抗和化疗联合应用一线治疗胃癌或GEJ腺癌的抗PD-1疗法。该适应症是在FDA的实时肿瘤学审查(RTOR)试点项目下进行审查,并给予肿瘤缓解率和缓解持久性数据获得加速批准。针对该适应症的持续批准,将取决于验证性临床试验中对临床益处的验证和描述。
默沙东研究实验室首席医疗官、高级副总裁兼全球临床开发主管Roy Baynes博士表示:“今天的批准标志着一个重要的里程碑,因为这是首次批准抗PD-1疗法与抗HER2疗法和化疗联合作为这些患者的一线治疗。从Keytruda研发之初,我们就一直在不断地探索新的组合,以帮助更多的癌症患者。我们很高兴为HER2阳性胃癌和GEJ腺癌患者带来了一种新的一线联合方案,该方案与标准方案相比在ORR方面有显著改善。”
胃癌
此次Keytruda最新批准,基于正在进行的3期KEYNOTE-811试验(NCT03615326)的数据。该试验在692例未接受过系统疗法治疗转移性疾病的HER2阳性晚期胃癌或GEJ腺癌患者中开展,评估了Keytruda联合曲妥珠单抗和化疗(5-氟尿嘧啶+顺铂,或卡培他滨+奥沙利铂)用于一线治疗的疗效和安全性。
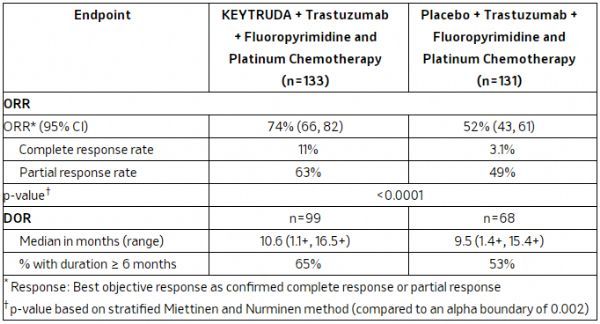
结果显示,与曲妥珠单抗+化疗组相比,Keytruda+曲妥珠单抗+化疗组表现出统计学上显著更高的客观缓解率(ORR:74% vs 52%;p<0.0001)。Keytruda方案组中,完全缓解率(CR)为11%、部分缓解率(PR)为63%。而曲妥珠单抗+化疗组中,CR为3.1%、PR为49%。
KEYNOTE-811临床数据
胃癌免疫治疗方面,今年4月中旬,百时美施贵宝(BMS)的抗PD-1疗法Opdivo(欧狄沃,通用名:nivolumab,纳武利尤单抗)获得美国FDA批准,联合氟嘧啶和铂类组合化疗,一线治疗晚期或转移性胃癌(GC)、胃食管交界(GEJ)癌、食管腺癌(EAC)成人患者,无论PD-L1表达状态如何。
Opdivo是第一个也是唯一一个联合化疗与单纯化疗在一线治疗胃癌、GEJ癌、EAC方面显著改善总生存期(OS)的免疫疗法,将成为这类患者新的护理标准。来自关键3期临床研究(CheckMate-649)的结果显示,与化疗组相比,Opdivo+化疗组总生存期(OS)和无进展生存期(PFS)有统计学意义和临床意义的改善。
具体数据为:在CPS≥5的PD-L1阳性患者中,Opdivo+化疗组的中位OS为14.4个月(95%CI:13.1-16.2),而化疗组的中位OS为11.1个月(95%CI:10.0-12.1),数据具有统计学显著差异(HR=0.71;98.4%CI:0.59-0.86;p<0.0001)。Opdivo+化疗组的中位PFS为7.7个月(95%CI:7.0-9.2),而化疗组为6.0个月(95%CI:5.6-6.9),数据也具有统计学显著差异(HR:0.68;98%CI:0.56-0.81;p<0.0001)。该试验中,Opdivo+化疗联合用药的安全性反映了Opdivo和化疗的已知安全性,没有观察到新的安全性信号。
Opdivo联合化疗对CPS≥1的PD-L1阳性患者群体、所有随机患者群体中也观察到具有统计学意义的OS益处。在所有随机患者群体中,接受Opdivo+化疗的患者中位OS为13.8个月(95%CI:12.6-14.6),仅接受化疗的患者中位OS为11.6个月(95%CI:10.9-12.5),数据具有统计学显著差异(HR:0.80;99.3%CI:0.68-0.94;p=0.0002)。在CPS≥1的PD-L1阳性患者中,接受Opdivo+化疗的患者中位OS为14.0个月(95%CI:12.6-15.0),仅接受化疗的患者中位OS为11.3个月(95%CI:10.6-12.3),数据也具有统计学显著差异(HR:0.77;99.3%CI:0.64-0.92;p=0.0001)。
胃癌是全球第五大常见癌症,也是第三大癌症死亡原因。2018年,全球胃癌新发病例超过100万例,死亡约78.3万例。胃癌的定义较为广泛,包括形成于胃和食管交界处的胃食管连接部(GEJ)癌在内的多种癌症均可被归属于胃癌。相较胃癌,胃食管连接部癌的患病率虽低,却呈持续增长趋势。
Keytruda属于抗PD-(L)1肿瘤免疫疗法,这类疗法通过提高人体免疫系统的能力来帮助检测和对抗肿瘤细胞。Keytruda是一种抗PD-1疗法,通过阻断PD-1与其配体PD-L1和PD-L2之间的相互作用,从而激活可能影响肿瘤细胞和健康细胞的T淋巴细胞。目前,Keytruda已成为多种类型癌症的基础疗法。
在全球范围内,已有10多款抗PD-(L)1疗法批准上市,Keytruda是其中的领头羊,2020年全球销售额达到143.8亿美元,较上一年增长幅度达30%。
默沙东拥有业界最大规模的免疫肿瘤学临床开发项目,目前有超过1400个临床试验正在调查Keytruda在多种类型肿瘤和治疗背景中的作用。Keytruda临床项目旨在了解该药在癌症中的作用以及可能预测患者从Keytruda治疗中受益的因素,包括探索几种不同的生物标志物。(生物谷Bioon.com)
原文出处:FDA approves Merck’s KEYTRUDA (pembrolizumab) Combined With Trastuzumab and Chemotherapy as First-line Treatment in Locally Advanced Unresectable or Metastatic HER2-Positive Gastric or Gastroesophageal Junction Adenocarcinoma
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->