利用CAR-T细胞疗法及其改进版本治疗实体瘤大有可为(第2期)
来源:本站原创 2019-10-27 22:01
2019年10月27日讯/生物谷BIOON/---CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被认为是最有前景的肿瘤治疗方式之一。正如所有的技术一样,CAR-T技术也经历一个漫长的演化过
2019年10月27日讯/生物谷BIOON/---CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被认为是最有前景的肿瘤治疗方式之一。正如所有的技术一样,CAR-T技术也经历一个漫长的演化过程,正是在这一系列的演化过程中,CAR-T技术逐渐走向成熟。
这种新的治疗策略的关键之处在于识别靶细胞的被称作嵌合抗原受体(chimeric antigen receptor, CAR)的人工受体,而且在经过基因修饰后,病人T细胞能够表达这种CAR。在人体临床试验中,科学家们通过一种类似透析的过程提取出病人体内的一些T细胞,然后在实验室对它们进行基因修饰,将编码这种CAR的基因导入,这样这些T细胞就能够表达这种新的受体。这些经过基因修饰的T细胞在实验室进行增殖,随后将它们灌注回病人体内。这些T细胞利用它们表达的CAR受体结合到靶细胞表面上的分子,而这种结合触发一种内部信号产生,接着这种内部信号如此强效地激活这些T细胞以至于它们快速地摧毁靶细胞。
CAR-T细胞免疫疗法是对病人自己的T细胞经过基因修饰而构建出的,在治疗血癌上取得成功,但是利用CAR-T细胞治疗实体瘤---是由异质的细胞群体组成的,这些异质的细胞具有不同的表面分子---并不那么成功,这是因为正常组织含有CAR-T靶向的蛋白,因而,CAR-T不仅攻击肿瘤,也会攻击正常组织。因此,利用这种细胞疗法治疗实体瘤会导致不良事件,其中最突出的就是脱靶效应。这意味着经非肿瘤组织中的抗原激活后,CAR-T细胞增殖,并释放炎性因子,导致器官发生局部损伤,甚至导致严重的细胞因子释放综合征。
虽然在文献资料上,利用CAR-T细胞在人体中治疗实体瘤尚没有成功的临床治疗案例,但是科学家们在临床前研究中取得了不少的进展,这些进展最终将为临床转化奠定基础。
1.Cell:重大进展!开发出比CAR-T细胞更安全、用途更广的cCAR-T细胞技术
doi:10.1016/j.cell.2019.10.002
在一项新的研究中,来自美国格拉斯通研究所和Xyphos生物科学公司(Xyphos Biosciences, Inc.)的研究人员描述了一种攻击被HIV感染的细胞的新技术。这种新技术是CAR-T细胞免疫疗法的一种新的改进版本。近年来,这种疗法因在抵抗血癌上取得的成功而闻名于世。通过改进使得它具有更大的覆盖范围和多功能性,这种称为convertibleCAR T细胞(cCAR-T)的新技术在多个治疗领域显示出了巨大的前景,特别是在抗击HIV方面,这是因为它可以用来缩小在接受抗逆转录病毒疗法(ART)期间HIV感染者体内持续存在的受感染细胞的库存量。相关研究结果于2019年10月24日在线发表在Cell期刊上,论文标题为“Attacking Latent HIV with convertibleCAR-T Cells, a Highly Adaptable Killing Platform”。论文通讯作者为格拉斯通研究所HIV治愈研究中心主任Warner C. Greene博士。
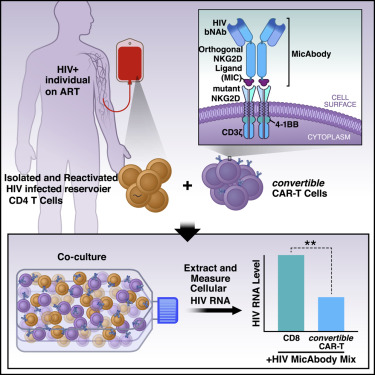
人们已证实传统的CAR-T细胞在诱导血癌(比如淋巴瘤和儿童白血病)缓解方面非常成功。但是作为抵抗HIV感染的疗法,传统的CAR-T细胞并不完美。论文第一作者、Greene实验室科学家Eytan Herzig说,“传统的CAR-T细胞的一些缺点是它们经过基因改造后靶向癌细胞表面上的单个分子,而且一旦被注射到患者体内,无法对它们进行控制。”
Xyphos生物科学公司通过从细胞毒杀伤细胞中分离出靶向抗体克服了这些缺陷。该公司首席科学家David W. Martin博士解释说:“我们对cCAR-T细胞进行了基因改造,使得这些T细胞可以在其表面上表达受到少量修饰的人类受体蛋白NKG2D。”这种受到修饰的NKG2D受体当与它的搭档结合时,可以将这些T细胞变成有效的杀手。它的搭档是一种叫做MIC-A的蛋白质,Xyphos生物科学公司的科学家对它进行了裁剪和修饰,使得它可以与cCAR-T细胞表面上这种经过修饰的NKG2D受体特异性结合。这些科学家随后将它与靶向抗体的底部融合在一起,从而构建出他们称为MicAbody的产物。因此,这种靶向性MicAbody紧密地和唯一地结合cCAR-T细胞。
为了清除潜伏性HIV病毒库,Herzig和Greene一直在实验室中测试称为广泛中和抗体(bNAb)的抗HIV抗体。他们与Xyphos生物科学公司的科学家合作,基于bNAb构建出MicAbody(称为Mic-bNAb),并在各种实验室分析中测试了cCAR-T细胞和Mic-bNAb的组合使用。
在实验室中,Herzig以感染了各种HIV毒株的多种CD4 T细胞(HIV的天然靶标)为研究对象测试了这些组合。特别是,他使用了源自人类扁桃体的细胞制剂;已知在HIV感染者中,扁桃体T细胞是潜伏性HIV病毒库。他想确保cCAR-T/Mic-bNAb组合使用能杀死代表潜伏性HIV病毒库的T细胞类型。
结果是显著的:cCAR-T细胞与Mic-bNAb的组合使用特异性地杀死了受到感染的CD4 T细胞,但未杀死未感染的细胞。它们仅与Mic-bNAb组合使用时才杀死受感染的细胞,然而,不论是单独使用还是与不靶向HIV的MicAbody组合使用都没有这种效果。他们杀死了在实验室中感染了多种HIV毒株的CD4 T细胞。当与靶向HIV的Mic-bNAb和靶向癌细胞的MicAbody组合使用时,cCAR-T细胞可以有效杀死在相同细胞培养物中混合在一起的癌细胞和受到HIV感染的细胞。换句话说,cCAR-T细胞精确地证明了它旨在实现的多功能性和特异性。
最后,Herzig和Greene测试了cCAR-T/Mic-bNAb平台是否可以攻击接受ART治疗的HIV感染者血液中存在的潜伏性HIV病毒库。为了让这些细胞对cCAR-T细胞可见,他们首先用强效的称为“潜伏逆转剂(latency-reversing agent)”的化合物活化这些细胞培养物。在接触后48小时内,一半以上活化的表达HIV靶抗原的细胞被清除。Greene总结道,“这个平台前景广阔。”
2.ACS子刊:药物和光线组合使用可对CAR-T细胞疗法进行时空控制
doi:10.1021/acssynbio.9b00175
在一项新的研究中,来自美国加州大学圣地亚哥分校的研究人员离让CAR-T细胞疗法更安全、更精确且易于控制的目标更近了一步。他们开发出一种系统,使得他们可以选择在何时何地激活CAR-T细胞从而让它们在不损害正常细胞的情况下破坏癌细胞。相关研究结果发表在2019年10月18日的ACS Synthetic Biology期刊上,论文标题为“An AND-Gated Drug and Photoactivatable Cre-loxP System for Spatiotemporal Control in Cell-Based Therapeutics”。
这种系统需要两把“钥匙”---药物他莫昔芬(Tamoxifen)和蓝光---来激活CAR-T细胞,使得它们能够结合它们的靶标。仅一把钥匙无法激活这些细胞。作为概念验证,这些研究人员在活细胞培养物中测试了他们的系统。他们的下一步是针对小鼠中的肿瘤进行测试。
论文共同通讯作者、加州大学圣地亚哥分校生物工程教授Yingxiao Wang和他的同事们设计出仅在接受两个输入信号---用小分子药物他莫昔芬进行治疗,然后暴露于短脉冲的低强度蓝光下---后才能被激活的T细胞。Wang说:“发生意外激活的机会极低,这是因为这需要同时接受两个输入信号。这种药物可以让这些T细胞作好准备,而蓝光可以让我们精确地引导它们到达它们被激活的位点。”
起初,这些CAR-T细胞处于待机模式。为了激活它们,两种特定的蛋白(一种在细胞核外,一种在细胞核内)结合在一起,以触发这种抗原靶向受体的表达。药物他莫昔芬首先与这些两种特定蛋白中的一种结合,并帮助它进入细胞核,而另一种蛋白在那里等待着它的到来。蓝光随后诱导这种两种蛋白结合在一起。用这种药物处理但未暴露于蓝光的所有细胞仍然保持在待机模式。
蓝光无法深入人体内,因此,Wang认为这种方法可能能够用于治疗皮肤癌和头颈癌。他如今在正在寻找与临床医生合作以便在体内测试对黑色素瘤的治疗。
3.Nat Biotechnol:新型CAR-T细胞疗法高效攻击致命性脑瘤,可清除80%的肿瘤
doi:10.1038/s41587-019-0192-1
在一项新的研究中,来自美国麻省总医院和哈佛医学院的研究人员发现一种令人兴奋的新型癌症免疫疗法对患有胶质母细胞瘤(一种最常见和最致命的脑癌类型)的患者有疗效。他们构建出的一种新方法可能让免疫疗法再次变得对脑瘤有效,而且这可能有助于利用它治疗其他类型的实体瘤。相关研究结果于2019年7月22日在线发表在Nature Biotechnology期刊上,论文标题为“CAR-T cells secreting BiTEs circumvent antigen escape without detectable toxicity”。
这种称为嵌合抗原受体T细胞疗法(CAR-T)的免疫疗法涉及收集患者体内具有免疫攻击性的T细胞,并对它们进行基因修饰,使得它们能够识别肿瘤表面上的特定靶标(抗原),然后将它们灌注回相同患者体内。
论文通讯作者、麻省总医院细胞免疫治疗主任、哈佛医学院医学助理教授Marcela V. Maus博士解释道,常规抗癌药很难治疗诸如胶质母细胞瘤之类的实体瘤,这是因为大多数药物分子都太大而无法穿过血脑屏障,而且免疫疗法在这方面也存在问题。
Maus说道,“我们之前制造出治疗胶质母细胞瘤的CAR-T细胞,胶质母细胞瘤面临的挑战之一就是并非所有的肿瘤细胞都能表达T细胞能够靶向的靶标。”它们的靶标是表皮生长因子受体变体III(EGFRvIII),这是一种突变的致癌蛋白,存在于许多但并非所有胶质母细胞瘤的表面。
因此,为了提高CAR-T细胞的疗效,他们决定靶向第二种抗原,即天然存在的EGFR,或者说“野生型”EGFR。但是鉴于EGFR存在于体内许多细胞中,因此靶向这种蛋白的药物可引起严重的副作用。为了克服这种毒性问题,Maus及其同事们构建出一种可被递送到大脑底部的脑脊液中的CAR-T细胞。当进入大脑中时,这种CAR-T细胞随后分泌第二种类型的免疫治疗分子,称为双特异性T细胞衔接蛋白(bi-specific T-cell engager, BiTE)。BiTE是将细胞杀伤性的T细胞引导至特定靶标的抗体,这有点类似于所谓的“智能炸弹”上的自动引导装置。
虽然BiTE比抗体类药物小,但是如果进行静脉注射的话,那么BiTE仍然太大而无法穿过血脑屏障,因此他们构建出的分泌BiTE 的CAR-T构建体“能够通过靶向第二种抗原产生局部肿瘤效应,这是一种克服这种肿瘤异质性并且能够一次性靶向两种物质的方法。但是,鉴于它是在血脑屏障的另一侧少量产生的,它不会对其他器官造成毒性”。当在人胶质母细胞瘤模型中进行测试时,他们发现这些经过基因改进的分泌BiTE的CAR-T细胞消除了大约80%的肿瘤。
4.Science:重磅!利用疫苗增强CAR-T细胞治疗实体瘤的疗效,可完全清除60%小鼠体内的实体瘤
doi:10.1126/science.aav8692
一种有希望的治疗某些类型癌症的新方法是对患者自身的T细胞进行编程,使得它们能够破坏癌细胞。这种称为CAR-T细胞疗法的方法目前可用于抵抗某些类型的白血病,但是到目前为止它还不能很好地治疗实体瘤,如肺肿瘤或乳腺肿瘤。
如今,在一项新的研究中,来自美国麻省理工学院的研究人员开发出一种新的方法对这种疗法进行改进,使得它可用作一种抵抗几乎任何癌症类型的武器。具体而言,他们开发出一种疫苗,它可显著地增强抗肿瘤T细胞群体,并且允许这些T细胞大力地侵入实体瘤中。相关研究结果发表在2019年7月12日的Science期刊上,论文标题为“Enhanced CAR–T cell activity against solid tumors by vaccine boosting through the chimeric receptor”。
在一项针对小鼠的研究中,这些研究人员发现他们能够完全清除60%的在接受CAR-T细胞治疗的同时还接受了强化疫苗接种的小鼠体内的实体瘤。在治疗实体瘤时,这些接受基因改造的T细胞独自地几乎没有效果。
论文通讯作者、麻省理工学院科赫综合癌症研究所副主任Darrell Irvine说道,“通过添加一种疫苗,对存活没有影响的CAR-T细胞治疗经这种疫苗强化后可导致一半以上的小鼠发生完全缓解。”此外,论文第一作者为麻省理工学院博士后研究员Leyuan Ma。
5.PNAS:靶向TOX和TOX2有望改善CAR-T细胞免疫疗法对实体瘤的治疗
doi:10.1073/pnas.1905675116
十年前,科学家们已宣布开发出一种称为CAR(嵌合抗原受体)-T的癌症免疫疗法:对来自患者的T细胞进行基因修饰,使得它们具有强大的抗肿瘤作用,随后再将这些经过基因修饰的T细胞灌注到患者自己的体内。从那以后,CAR-T方法(统称为“过继性T细胞转移”的几种策略中的一种)作为新型细胞免疫治疗工具成为头条新闻。迄今为止,它们最为成功地用于对抗所谓的“液体癌症(liquid cancer)”,如白血病和淋巴瘤。
肉瘤和癌症对这些方法更有抵抗力,这部分上是因为经过基因修饰的T细胞一旦浸润到肿瘤中就逐渐地失去抗肿瘤能力。免疫学家将这种细胞疲劳称为T细胞“衰竭(exhaustion)”或“功能障碍(dysfunction)”。为了理解其中的原因,美国拉荷亚免疫学研究所的Anjana Rao博士和Patrick Hogan博士在过去几年中发表了一系列论文,报道了一种称为NFAT的调节基因表达的转录因子开启削弱T细胞抗肿瘤反应的“下游”基因表达,因而导致T细胞衰竭。其中的一组下游基因编码转录因子NR4A,而且前研究生Joyce Chen已发现通过基因手段清除肿瘤浸润CAR-T细胞中的NR4A蛋白可改善肿瘤排斥。然而,在这个途径中与NFAT和NR4A发挥协同作用的其他参与者的身份仍然未知。
如今,在一项新的研究中,Rao实验室和Hogan实验室在一个建立并维持T细胞衰竭的广泛基因表达网络中,提供了一个更为完整的参与者列表。这项研究利用小鼠模型发现通过基因手段清除两个新的转录因子--- TOX和TOX2---也会改善CAR-T方法中对“实体”黑色素瘤的根除。它表明在患者中靶向NR4A和TOX因子的类似干预措施可能将基于CAR-T的免疫疗法的应用扩展到实体瘤中。相关研究结果于2019年5月31日在线发表在PNAS期刊上,论文标题为“TOX and TOX2 transcription factors cooperate with NR4A transcription factors to impose CD8+ T cell exhaustion”。
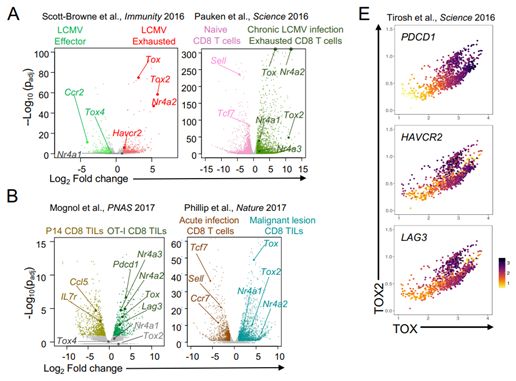
他们首先比较了正常的与“衰竭的”T细胞样本中的基因表达谱,寻找与NR4A同时上调的因子作为T细胞功能障碍的同谋者。论文第一作者、Rao实验室博士后研究员Hyungseok Seo博士说道,“我们发现两种称为TOX和TOX2的DNA结合蛋白与NR4A转录因子一起高度表达。这一发现表明诸如NFAT或NR4A之类的因子可能会控制TOX的表达。”
值得注意的是,相比于接受正常的T细胞灌注的小鼠,接受缺乏TOX的CAR-T细胞灌注的小鼠显示出更为强烈的黑色素瘤消退。此外,接受缺乏TOX的CAR-T细胞治疗的小鼠表现出显著增加的存活率,这就表明TOX因子的缺乏对抗T细胞衰竭并且允许T细胞更有效地破坏肿瘤细胞。
6.Adv Mat:CAR T治疗实体瘤取得突破!华人学者利用光热疗法突破实体瘤障碍!
doi:10.1002/adma.201900192
加州大学洛杉矶分校(UCLA)Jonsson综合癌症研究所的科学家领导的一项临床前研究表明,在CAR T细胞治疗期间加热实体肿瘤可以提高治疗的成功率。研究人员发现,将光热消融的加热技术与CAR T细胞灌注结合在一起,可以抑制小鼠黑色素瘤的生长长达20天。在接受联合治疗的小鼠中,33%的小鼠在20天后仍然没有肿瘤。
用嵌合抗原受体(CAR)进行基因工程的T细胞已成功地用于治疗许多淋巴瘤和白血病患者。但是CAR T细胞疗法在治疗实体肿瘤方面效果不太好,这是因为实体肿瘤有一个保护性的微环境,这使得CAR T细胞更难进入肿瘤并保持T细胞活性。UCLA的科学家们决定测试CAR T疗法与光热疗法结合是否能克服这个障碍。光热疗法是一种利用激光能量的热量杀死癌细胞的微创技术;它已经被用于治疗各种癌症和其他疾病。
研究人员测试了大约40摄氏度的轻度热疗是否可以帮助CAR T细胞更有效地攻击肿瘤。UCLA领导的研究小组在注射了人类黑色素瘤的老鼠身上测试了这项技术。研究人员将光热剂注入肿瘤,然后用激光照射使其升温。然后,静脉注射CAR T细胞。利用激光将肿瘤温度提高到40摄氏度左右,有助于肿瘤相关血管的扩张,同时可以促进T细胞生长。
该技术通过增强CAR T细胞治疗的能力,最终可以改善难以治疗的实体肿瘤患者的预后。研究人员将继续在动物身上测试这一策略,以优化加热时间和温度,然后再决定是否可以在人体进行测试。UCLA Samueli工程学院生物工程学教授、Jonsson癌症中心成员、UCLA纳米系统研究所成员顾臻教授是这项研究的共同通讯作者,论文的另一位通讯作者是北卡罗来纳大学教堂山分校的Gianpietro Dotti博士,该论文第一作者是顾教授实验室博士后研究员陈倩博士。该研究发表在《Advanced Materials》上。
7.PNAS:基于纳米抗体的CAR-T细胞有望治疗实体瘤
doi:10.1073/pnas.1817147116
1989年,比利时布鲁塞尔自由大学的两名本科生被要求测试骆驼的冷冻血清,偶然间发现了一类以前未知的抗体。它是人体抗体的小型化版本,仅由两条重蛋白链组成,而不是由两条轻链和两条重链组成。正如他们最终报道的那样,这类抗体的存在不仅在骆驼中得到证实,而且也在美洲驼和羊驼中得到证实。
嵌合抗原受体(CAR)-T细胞疗法具有很高的治疗血癌的前景,它通过对患者自身的T细胞进行基因改造,使得它们更好地攻击癌细胞。比如,达纳-法伯/波士顿儿童癌症癌症与血液疾病中心当前正在利用CAR-T细胞疗法治疗复发性急性淋巴细胞白血病(ALL)。但是,CAR-T细胞并不擅长清除实体瘤。人们在实体瘤上很难找到可以作为安全靶标的癌症特异性蛋白。实体瘤也受到胞外基质和免疫抑制分子的保护,其中胞外基质是一种起着屏障作用的蛋白网络,免疫抑制分子削弱T细胞攻击。
30年后,在一项新的研究中,来自美国波士顿儿童医院和麻省理工学院的研究人员发现这些微型抗体(mini-antibody)经进一步缩小后可形成所谓的纳米抗体(nanobody),可能有助于解决癌症领域的一个问题:让CAR-T细胞疗法在实体瘤中发挥作用。相关研究结果于2019年4月1日在线发表在PNAS期刊上,论文标题为“Nanobody-based CAR T cells that target the tumor microenvironment inhibit the growth of solid tumors in immunocompetent mice”。论文通讯作者为波士顿儿童医院细胞与分子医学项目免疫学家Hidde Ploegh博士。论文第一作者是波士顿儿童医院细胞与分子医学项目的研究生Yushu Joy Xie。

通过在两种不同的黑色素瘤小鼠模型中进行测试,这些基于纳米抗体的CAR-T细胞杀死肿瘤细胞,显著减缓肿瘤生长并改善这些小鼠的存活,并且没有产生明显的副作用。Ploegh认为这些经过基因改造的T细胞通过多种因素发挥作用。它们对肿瘤组织造成损伤,而这往往会刺激炎症免疫反应。靶向EIIIB可能以一种减少肿瘤血液供应的方式损害血管,同时让它们对癌症药物更具渗透性。
8.Nature:重磅!在CAR-T细胞疗法中,找到一种抵抗T细胞衰竭的新策略
doi:10.1038/s41586-019-0985-x
越来越多的癌症患者正在接受一种有前景的称为CAR-T细胞疗法的新疗法。在这种疗法中,将患者自身的T细胞从体内取出,它们经过基因改造后更好地识别癌细胞。这些经过基因改造的T细胞随后被灌注回患者体内,在那里它们发起免疫反应以摧毁癌症。CAR-T细胞疗法挽救了血癌患者的生命,但是存在一个缺点:由于一种称为T细胞衰竭(T cell exhaustion)的现象,进入实体瘤的T细胞可能停止发挥作用。
如今,在一项新的研究中,来自美国拉霍亚免疫学研究所(LJI)的研究人员找到了一种抵抗T细胞衰竭并让CAR-T细胞疗法更有效的方法。他们发现一个称为Nr4a转录因子的蛋白家族在调节与T细胞衰竭相关的基因方面起着突出作用。通过使用小鼠模型,他们证实利用缺乏Nr4a转录因子的CAR-T细胞治疗小鼠可让肿瘤缩小和提高生存率。相关研究结果于2019年2月27日在线发表在Nature期刊上,论文标题为“NR4A transcription factors limit CAR T cell function in solid tumours”。论文通讯作者为拉霍亚免疫学研究所信号转导与基因表达部门的Anjana Rao博士和James P. Scott-Browne博士。
这些研究人员证实Nr4a转录因子确实在调节T细胞衰竭中发挥作用。接受Nr4a缺失的CAR-T细胞输注的大多数小鼠存活下来,而且它们的肿瘤在90天的实验过程中发生消退并保持较小的体积。相反,几乎所有接受具有天然存在的Nr4a转录因子的正常CAR-T细胞输注的小鼠在第35天死亡死于它们的肿瘤。
9.Hum Gene Ther:四川大学在靶向实体瘤的CAR T疗法中取得新突破
doi:10.1089/hum.2018.229
研究人员已经发现靶向肿瘤生物标志物上皮细胞粘附分子(epithelial cell adhesion molecule,EpCAM)的癌症免疫疗法对小鼠安全无毒,而且可以显著延缓肿瘤的形成和生长。EpCAM在多种类型的肿瘤、循环肿瘤细胞和肿瘤干细胞中均过表达,因此这些发现具有广泛的意义。相关研究结果于近日发表在《Human Gene Therapy》特刊上。
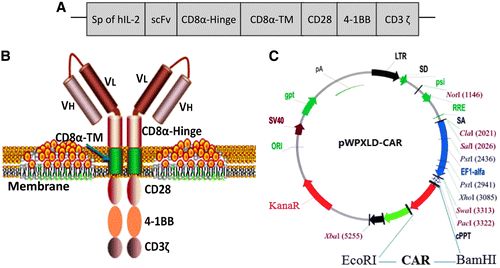
特拉维夫大学博士、以色列基因与细胞治疗学会会长Adi Barzel博士是本期特刊的客座编辑。这篇文章题为“Preclinical Evaluation of Chimeric Antigen Receptor-Modified T Cells Specific to EpCAM for Treating Colorectal Cancer”,共同作者包括Wei Wang和一组来自华西医院、四川大学生物治疗协同创新中心和重庆医科大学第一附属医院的研究人员。
研究人员制造了第三代嵌合抗原受体修饰的T (chi-meric antigen receptor-modified T,CAR-T)细胞。他们使用慢病毒载体特异性靶向了细胞中的EpCAM。
“CAR-T疗法代表了一个治疗B细胞白血病和淋巴瘤患者的突破,但不幸的是在实体肿瘤治疗方面进展缓慢。”该杂志主编Terence R. Flotte医学博士说道。“这项针对结直肠癌患者的关键研究表明,靶向癌症免疫治疗确实可能在这种非常常见的恶性肿瘤中发挥作用。”
10.Nat Commun:中国科学家发现CAR-T来源的外泌体抗癌疗效显著、毒性低更安全
doi:10.1038/s41467-019-12321-3
表达嵌合抗原受体(CAR)的基因工程T细胞正迅速成为治疗血源性和非血源性恶性肿瘤的一种有前途的新疗法。CAR-T治疗可诱导快速和持久的临床反应,但却存在独特的细胞毒性。此外,CAR-T细胞疗法的疗效易受免疫抑制机制的影响。
近日来自上海交通大学、第二军医大学和Pharchoice Therapeutics Inc的研究人员发现CAR-T细胞会释放细胞外囊泡,主要以外泌体的形式存在,而这些外泌体的表面携带CAR。研究人员发现含有CAR的外泌体表达高水平的细胞毒性分子,可以显着抑制肿瘤生长。
通过进一步的实验,研究人员发现与CAR-T细胞疗法相比,CAR外泌体不表达程序性细胞死亡蛋白1 (PD1),重组PD-L1的治疗不会削弱CAR外泌体的抗肿瘤作用。研究人员在细胞因子释放综合征的体内临床前模型中进行的实验表明,CAR外泌体的应用相对于CAR-T治疗而言更安全。(生物谷 Bioon.com)
这种新的治疗策略的关键之处在于识别靶细胞的被称作嵌合抗原受体(chimeric antigen receptor, CAR)的人工受体,而且在经过基因修饰后,病人T细胞能够表达这种CAR。在人体临床试验中,科学家们通过一种类似透析的过程提取出病人体内的一些T细胞,然后在实验室对它们进行基因修饰,将编码这种CAR的基因导入,这样这些T细胞就能够表达这种新的受体。这些经过基因修饰的T细胞在实验室进行增殖,随后将它们灌注回病人体内。这些T细胞利用它们表达的CAR受体结合到靶细胞表面上的分子,而这种结合触发一种内部信号产生,接着这种内部信号如此强效地激活这些T细胞以至于它们快速地摧毁靶细胞。
CAR-T细胞免疫疗法是对病人自己的T细胞经过基因修饰而构建出的,在治疗血癌上取得成功,但是利用CAR-T细胞治疗实体瘤---是由异质的细胞群体组成的,这些异质的细胞具有不同的表面分子---并不那么成功,这是因为正常组织含有CAR-T靶向的蛋白,因而,CAR-T不仅攻击肿瘤,也会攻击正常组织。因此,利用这种细胞疗法治疗实体瘤会导致不良事件,其中最突出的就是脱靶效应。这意味着经非肿瘤组织中的抗原激活后,CAR-T细胞增殖,并释放炎性因子,导致器官发生局部损伤,甚至导致严重的细胞因子释放综合征。
虽然在文献资料上,利用CAR-T细胞在人体中治疗实体瘤尚没有成功的临床治疗案例,但是科学家们在临床前研究中取得了不少的进展,这些进展最终将为临床转化奠定基础。
1.Cell:重大进展!开发出比CAR-T细胞更安全、用途更广的cCAR-T细胞技术
doi:10.1016/j.cell.2019.10.002
在一项新的研究中,来自美国格拉斯通研究所和Xyphos生物科学公司(Xyphos Biosciences, Inc.)的研究人员描述了一种攻击被HIV感染的细胞的新技术。这种新技术是CAR-T细胞免疫疗法的一种新的改进版本。近年来,这种疗法因在抵抗血癌上取得的成功而闻名于世。通过改进使得它具有更大的覆盖范围和多功能性,这种称为convertibleCAR T细胞(cCAR-T)的新技术在多个治疗领域显示出了巨大的前景,特别是在抗击HIV方面,这是因为它可以用来缩小在接受抗逆转录病毒疗法(ART)期间HIV感染者体内持续存在的受感染细胞的库存量。相关研究结果于2019年10月24日在线发表在Cell期刊上,论文标题为“Attacking Latent HIV with convertibleCAR-T Cells, a Highly Adaptable Killing Platform”。论文通讯作者为格拉斯通研究所HIV治愈研究中心主任Warner C. Greene博士。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.10.002。
人们已证实传统的CAR-T细胞在诱导血癌(比如淋巴瘤和儿童白血病)缓解方面非常成功。但是作为抵抗HIV感染的疗法,传统的CAR-T细胞并不完美。论文第一作者、Greene实验室科学家Eytan Herzig说,“传统的CAR-T细胞的一些缺点是它们经过基因改造后靶向癌细胞表面上的单个分子,而且一旦被注射到患者体内,无法对它们进行控制。”
Xyphos生物科学公司通过从细胞毒杀伤细胞中分离出靶向抗体克服了这些缺陷。该公司首席科学家David W. Martin博士解释说:“我们对cCAR-T细胞进行了基因改造,使得这些T细胞可以在其表面上表达受到少量修饰的人类受体蛋白NKG2D。”这种受到修饰的NKG2D受体当与它的搭档结合时,可以将这些T细胞变成有效的杀手。它的搭档是一种叫做MIC-A的蛋白质,Xyphos生物科学公司的科学家对它进行了裁剪和修饰,使得它可以与cCAR-T细胞表面上这种经过修饰的NKG2D受体特异性结合。这些科学家随后将它与靶向抗体的底部融合在一起,从而构建出他们称为MicAbody的产物。因此,这种靶向性MicAbody紧密地和唯一地结合cCAR-T细胞。
为了清除潜伏性HIV病毒库,Herzig和Greene一直在实验室中测试称为广泛中和抗体(bNAb)的抗HIV抗体。他们与Xyphos生物科学公司的科学家合作,基于bNAb构建出MicAbody(称为Mic-bNAb),并在各种实验室分析中测试了cCAR-T细胞和Mic-bNAb的组合使用。
在实验室中,Herzig以感染了各种HIV毒株的多种CD4 T细胞(HIV的天然靶标)为研究对象测试了这些组合。特别是,他使用了源自人类扁桃体的细胞制剂;已知在HIV感染者中,扁桃体T细胞是潜伏性HIV病毒库。他想确保cCAR-T/Mic-bNAb组合使用能杀死代表潜伏性HIV病毒库的T细胞类型。
结果是显著的:cCAR-T细胞与Mic-bNAb的组合使用特异性地杀死了受到感染的CD4 T细胞,但未杀死未感染的细胞。它们仅与Mic-bNAb组合使用时才杀死受感染的细胞,然而,不论是单独使用还是与不靶向HIV的MicAbody组合使用都没有这种效果。他们杀死了在实验室中感染了多种HIV毒株的CD4 T细胞。当与靶向HIV的Mic-bNAb和靶向癌细胞的MicAbody组合使用时,cCAR-T细胞可以有效杀死在相同细胞培养物中混合在一起的癌细胞和受到HIV感染的细胞。换句话说,cCAR-T细胞精确地证明了它旨在实现的多功能性和特异性。
最后,Herzig和Greene测试了cCAR-T/Mic-bNAb平台是否可以攻击接受ART治疗的HIV感染者血液中存在的潜伏性HIV病毒库。为了让这些细胞对cCAR-T细胞可见,他们首先用强效的称为“潜伏逆转剂(latency-reversing agent)”的化合物活化这些细胞培养物。在接触后48小时内,一半以上活化的表达HIV靶抗原的细胞被清除。Greene总结道,“这个平台前景广阔。”
2.ACS子刊:药物和光线组合使用可对CAR-T细胞疗法进行时空控制
doi:10.1021/acssynbio.9b00175
在一项新的研究中,来自美国加州大学圣地亚哥分校的研究人员离让CAR-T细胞疗法更安全、更精确且易于控制的目标更近了一步。他们开发出一种系统,使得他们可以选择在何时何地激活CAR-T细胞从而让它们在不损害正常细胞的情况下破坏癌细胞。相关研究结果发表在2019年10月18日的ACS Synthetic Biology期刊上,论文标题为“An AND-Gated Drug and Photoactivatable Cre-loxP System for Spatiotemporal Control in Cell-Based Therapeutics”。
这种系统需要两把“钥匙”---药物他莫昔芬(Tamoxifen)和蓝光---来激活CAR-T细胞,使得它们能够结合它们的靶标。仅一把钥匙无法激活这些细胞。作为概念验证,这些研究人员在活细胞培养物中测试了他们的系统。他们的下一步是针对小鼠中的肿瘤进行测试。
论文共同通讯作者、加州大学圣地亚哥分校生物工程教授Yingxiao Wang和他的同事们设计出仅在接受两个输入信号---用小分子药物他莫昔芬进行治疗,然后暴露于短脉冲的低强度蓝光下---后才能被激活的T细胞。Wang说:“发生意外激活的机会极低,这是因为这需要同时接受两个输入信号。这种药物可以让这些T细胞作好准备,而蓝光可以让我们精确地引导它们到达它们被激活的位点。”
起初,这些CAR-T细胞处于待机模式。为了激活它们,两种特定的蛋白(一种在细胞核外,一种在细胞核内)结合在一起,以触发这种抗原靶向受体的表达。药物他莫昔芬首先与这些两种特定蛋白中的一种结合,并帮助它进入细胞核,而另一种蛋白在那里等待着它的到来。蓝光随后诱导这种两种蛋白结合在一起。用这种药物处理但未暴露于蓝光的所有细胞仍然保持在待机模式。
蓝光无法深入人体内,因此,Wang认为这种方法可能能够用于治疗皮肤癌和头颈癌。他如今在正在寻找与临床医生合作以便在体内测试对黑色素瘤的治疗。
3.Nat Biotechnol:新型CAR-T细胞疗法高效攻击致命性脑瘤,可清除80%的肿瘤
doi:10.1038/s41587-019-0192-1
在一项新的研究中,来自美国麻省总医院和哈佛医学院的研究人员发现一种令人兴奋的新型癌症免疫疗法对患有胶质母细胞瘤(一种最常见和最致命的脑癌类型)的患者有疗效。他们构建出的一种新方法可能让免疫疗法再次变得对脑瘤有效,而且这可能有助于利用它治疗其他类型的实体瘤。相关研究结果于2019年7月22日在线发表在Nature Biotechnology期刊上,论文标题为“CAR-T cells secreting BiTEs circumvent antigen escape without detectable toxicity”。

图片来自CC0 Public Domain。
这种称为嵌合抗原受体T细胞疗法(CAR-T)的免疫疗法涉及收集患者体内具有免疫攻击性的T细胞,并对它们进行基因修饰,使得它们能够识别肿瘤表面上的特定靶标(抗原),然后将它们灌注回相同患者体内。
论文通讯作者、麻省总医院细胞免疫治疗主任、哈佛医学院医学助理教授Marcela V. Maus博士解释道,常规抗癌药很难治疗诸如胶质母细胞瘤之类的实体瘤,这是因为大多数药物分子都太大而无法穿过血脑屏障,而且免疫疗法在这方面也存在问题。
Maus说道,“我们之前制造出治疗胶质母细胞瘤的CAR-T细胞,胶质母细胞瘤面临的挑战之一就是并非所有的肿瘤细胞都能表达T细胞能够靶向的靶标。”它们的靶标是表皮生长因子受体变体III(EGFRvIII),这是一种突变的致癌蛋白,存在于许多但并非所有胶质母细胞瘤的表面。
因此,为了提高CAR-T细胞的疗效,他们决定靶向第二种抗原,即天然存在的EGFR,或者说“野生型”EGFR。但是鉴于EGFR存在于体内许多细胞中,因此靶向这种蛋白的药物可引起严重的副作用。为了克服这种毒性问题,Maus及其同事们构建出一种可被递送到大脑底部的脑脊液中的CAR-T细胞。当进入大脑中时,这种CAR-T细胞随后分泌第二种类型的免疫治疗分子,称为双特异性T细胞衔接蛋白(bi-specific T-cell engager, BiTE)。BiTE是将细胞杀伤性的T细胞引导至特定靶标的抗体,这有点类似于所谓的“智能炸弹”上的自动引导装置。
虽然BiTE比抗体类药物小,但是如果进行静脉注射的话,那么BiTE仍然太大而无法穿过血脑屏障,因此他们构建出的分泌BiTE 的CAR-T构建体“能够通过靶向第二种抗原产生局部肿瘤效应,这是一种克服这种肿瘤异质性并且能够一次性靶向两种物质的方法。但是,鉴于它是在血脑屏障的另一侧少量产生的,它不会对其他器官造成毒性”。当在人胶质母细胞瘤模型中进行测试时,他们发现这些经过基因改进的分泌BiTE的CAR-T细胞消除了大约80%的肿瘤。
4.Science:重磅!利用疫苗增强CAR-T细胞治疗实体瘤的疗效,可完全清除60%小鼠体内的实体瘤
doi:10.1126/science.aav8692
一种有希望的治疗某些类型癌症的新方法是对患者自身的T细胞进行编程,使得它们能够破坏癌细胞。这种称为CAR-T细胞疗法的方法目前可用于抵抗某些类型的白血病,但是到目前为止它还不能很好地治疗实体瘤,如肺肿瘤或乳腺肿瘤。
如今,在一项新的研究中,来自美国麻省理工学院的研究人员开发出一种新的方法对这种疗法进行改进,使得它可用作一种抵抗几乎任何癌症类型的武器。具体而言,他们开发出一种疫苗,它可显著地增强抗肿瘤T细胞群体,并且允许这些T细胞大力地侵入实体瘤中。相关研究结果发表在2019年7月12日的Science期刊上,论文标题为“Enhanced CAR–T cell activity against solid tumors by vaccine boosting through the chimeric receptor”。
在一项针对小鼠的研究中,这些研究人员发现他们能够完全清除60%的在接受CAR-T细胞治疗的同时还接受了强化疫苗接种的小鼠体内的实体瘤。在治疗实体瘤时,这些接受基因改造的T细胞独自地几乎没有效果。
论文通讯作者、麻省理工学院科赫综合癌症研究所副主任Darrell Irvine说道,“通过添加一种疫苗,对存活没有影响的CAR-T细胞治疗经这种疫苗强化后可导致一半以上的小鼠发生完全缓解。”此外,论文第一作者为麻省理工学院博士后研究员Leyuan Ma。
5.PNAS:靶向TOX和TOX2有望改善CAR-T细胞免疫疗法对实体瘤的治疗
doi:10.1073/pnas.1905675116
十年前,科学家们已宣布开发出一种称为CAR(嵌合抗原受体)-T的癌症免疫疗法:对来自患者的T细胞进行基因修饰,使得它们具有强大的抗肿瘤作用,随后再将这些经过基因修饰的T细胞灌注到患者自己的体内。从那以后,CAR-T方法(统称为“过继性T细胞转移”的几种策略中的一种)作为新型细胞免疫治疗工具成为头条新闻。迄今为止,它们最为成功地用于对抗所谓的“液体癌症(liquid cancer)”,如白血病和淋巴瘤。
肉瘤和癌症对这些方法更有抵抗力,这部分上是因为经过基因修饰的T细胞一旦浸润到肿瘤中就逐渐地失去抗肿瘤能力。免疫学家将这种细胞疲劳称为T细胞“衰竭(exhaustion)”或“功能障碍(dysfunction)”。为了理解其中的原因,美国拉荷亚免疫学研究所的Anjana Rao博士和Patrick Hogan博士在过去几年中发表了一系列论文,报道了一种称为NFAT的调节基因表达的转录因子开启削弱T细胞抗肿瘤反应的“下游”基因表达,因而导致T细胞衰竭。其中的一组下游基因编码转录因子NR4A,而且前研究生Joyce Chen已发现通过基因手段清除肿瘤浸润CAR-T细胞中的NR4A蛋白可改善肿瘤排斥。然而,在这个途径中与NFAT和NR4A发挥协同作用的其他参与者的身份仍然未知。
如今,在一项新的研究中,Rao实验室和Hogan实验室在一个建立并维持T细胞衰竭的广泛基因表达网络中,提供了一个更为完整的参与者列表。这项研究利用小鼠模型发现通过基因手段清除两个新的转录因子--- TOX和TOX2---也会改善CAR-T方法中对“实体”黑色素瘤的根除。它表明在患者中靶向NR4A和TOX因子的类似干预措施可能将基于CAR-T的免疫疗法的应用扩展到实体瘤中。相关研究结果于2019年5月31日在线发表在PNAS期刊上,论文标题为“TOX and TOX2 transcription factors cooperate with NR4A transcription factors to impose CD8+ T cell exhaustion”。

图片来自PNAS, 2019, doi:10.1073/pnas.1905675116。
他们首先比较了正常的与“衰竭的”T细胞样本中的基因表达谱,寻找与NR4A同时上调的因子作为T细胞功能障碍的同谋者。论文第一作者、Rao实验室博士后研究员Hyungseok Seo博士说道,“我们发现两种称为TOX和TOX2的DNA结合蛋白与NR4A转录因子一起高度表达。这一发现表明诸如NFAT或NR4A之类的因子可能会控制TOX的表达。”
值得注意的是,相比于接受正常的T细胞灌注的小鼠,接受缺乏TOX的CAR-T细胞灌注的小鼠显示出更为强烈的黑色素瘤消退。此外,接受缺乏TOX的CAR-T细胞治疗的小鼠表现出显著增加的存活率,这就表明TOX因子的缺乏对抗T细胞衰竭并且允许T细胞更有效地破坏肿瘤细胞。
6.Adv Mat:CAR T治疗实体瘤取得突破!华人学者利用光热疗法突破实体瘤障碍!
doi:10.1002/adma.201900192
加州大学洛杉矶分校(UCLA)Jonsson综合癌症研究所的科学家领导的一项临床前研究表明,在CAR T细胞治疗期间加热实体肿瘤可以提高治疗的成功率。研究人员发现,将光热消融的加热技术与CAR T细胞灌注结合在一起,可以抑制小鼠黑色素瘤的生长长达20天。在接受联合治疗的小鼠中,33%的小鼠在20天后仍然没有肿瘤。
用嵌合抗原受体(CAR)进行基因工程的T细胞已成功地用于治疗许多淋巴瘤和白血病患者。但是CAR T细胞疗法在治疗实体肿瘤方面效果不太好,这是因为实体肿瘤有一个保护性的微环境,这使得CAR T细胞更难进入肿瘤并保持T细胞活性。UCLA的科学家们决定测试CAR T疗法与光热疗法结合是否能克服这个障碍。光热疗法是一种利用激光能量的热量杀死癌细胞的微创技术;它已经被用于治疗各种癌症和其他疾病。
研究人员测试了大约40摄氏度的轻度热疗是否可以帮助CAR T细胞更有效地攻击肿瘤。UCLA领导的研究小组在注射了人类黑色素瘤的老鼠身上测试了这项技术。研究人员将光热剂注入肿瘤,然后用激光照射使其升温。然后,静脉注射CAR T细胞。利用激光将肿瘤温度提高到40摄氏度左右,有助于肿瘤相关血管的扩张,同时可以促进T细胞生长。
该技术通过增强CAR T细胞治疗的能力,最终可以改善难以治疗的实体肿瘤患者的预后。研究人员将继续在动物身上测试这一策略,以优化加热时间和温度,然后再决定是否可以在人体进行测试。UCLA Samueli工程学院生物工程学教授、Jonsson癌症中心成员、UCLA纳米系统研究所成员顾臻教授是这项研究的共同通讯作者,论文的另一位通讯作者是北卡罗来纳大学教堂山分校的Gianpietro Dotti博士,该论文第一作者是顾教授实验室博士后研究员陈倩博士。该研究发表在《Advanced Materials》上。
7.PNAS:基于纳米抗体的CAR-T细胞有望治疗实体瘤
doi:10.1073/pnas.1817147116
1989年,比利时布鲁塞尔自由大学的两名本科生被要求测试骆驼的冷冻血清,偶然间发现了一类以前未知的抗体。它是人体抗体的小型化版本,仅由两条重蛋白链组成,而不是由两条轻链和两条重链组成。正如他们最终报道的那样,这类抗体的存在不仅在骆驼中得到证实,而且也在美洲驼和羊驼中得到证实。
嵌合抗原受体(CAR)-T细胞疗法具有很高的治疗血癌的前景,它通过对患者自身的T细胞进行基因改造,使得它们更好地攻击癌细胞。比如,达纳-法伯/波士顿儿童癌症癌症与血液疾病中心当前正在利用CAR-T细胞疗法治疗复发性急性淋巴细胞白血病(ALL)。但是,CAR-T细胞并不擅长清除实体瘤。人们在实体瘤上很难找到可以作为安全靶标的癌症特异性蛋白。实体瘤也受到胞外基质和免疫抑制分子的保护,其中胞外基质是一种起着屏障作用的蛋白网络,免疫抑制分子削弱T细胞攻击。
30年后,在一项新的研究中,来自美国波士顿儿童医院和麻省理工学院的研究人员发现这些微型抗体(mini-antibody)经进一步缩小后可形成所谓的纳米抗体(nanobody),可能有助于解决癌症领域的一个问题:让CAR-T细胞疗法在实体瘤中发挥作用。相关研究结果于2019年4月1日在线发表在PNAS期刊上,论文标题为“Nanobody-based CAR T cells that target the tumor microenvironment inhibit the growth of solid tumors in immunocompetent mice”。论文通讯作者为波士顿儿童医院细胞与分子医学项目免疫学家Hidde Ploegh博士。论文第一作者是波士顿儿童医院细胞与分子医学项目的研究生Yushu Joy Xie。

图片来自Boston Children's Hospital。
通过在两种不同的黑色素瘤小鼠模型中进行测试,这些基于纳米抗体的CAR-T细胞杀死肿瘤细胞,显著减缓肿瘤生长并改善这些小鼠的存活,并且没有产生明显的副作用。Ploegh认为这些经过基因改造的T细胞通过多种因素发挥作用。它们对肿瘤组织造成损伤,而这往往会刺激炎症免疫反应。靶向EIIIB可能以一种减少肿瘤血液供应的方式损害血管,同时让它们对癌症药物更具渗透性。
8.Nature:重磅!在CAR-T细胞疗法中,找到一种抵抗T细胞衰竭的新策略
doi:10.1038/s41586-019-0985-x
越来越多的癌症患者正在接受一种有前景的称为CAR-T细胞疗法的新疗法。在这种疗法中,将患者自身的T细胞从体内取出,它们经过基因改造后更好地识别癌细胞。这些经过基因改造的T细胞随后被灌注回患者体内,在那里它们发起免疫反应以摧毁癌症。CAR-T细胞疗法挽救了血癌患者的生命,但是存在一个缺点:由于一种称为T细胞衰竭(T cell exhaustion)的现象,进入实体瘤的T细胞可能停止发挥作用。
如今,在一项新的研究中,来自美国拉霍亚免疫学研究所(LJI)的研究人员找到了一种抵抗T细胞衰竭并让CAR-T细胞疗法更有效的方法。他们发现一个称为Nr4a转录因子的蛋白家族在调节与T细胞衰竭相关的基因方面起着突出作用。通过使用小鼠模型,他们证实利用缺乏Nr4a转录因子的CAR-T细胞治疗小鼠可让肿瘤缩小和提高生存率。相关研究结果于2019年2月27日在线发表在Nature期刊上,论文标题为“NR4A transcription factors limit CAR T cell function in solid tumours”。论文通讯作者为拉霍亚免疫学研究所信号转导与基因表达部门的Anjana Rao博士和James P. Scott-Browne博士。
这些研究人员证实Nr4a转录因子确实在调节T细胞衰竭中发挥作用。接受Nr4a缺失的CAR-T细胞输注的大多数小鼠存活下来,而且它们的肿瘤在90天的实验过程中发生消退并保持较小的体积。相反,几乎所有接受具有天然存在的Nr4a转录因子的正常CAR-T细胞输注的小鼠在第35天死亡死于它们的肿瘤。
9.Hum Gene Ther:四川大学在靶向实体瘤的CAR T疗法中取得新突破
doi:10.1089/hum.2018.229
研究人员已经发现靶向肿瘤生物标志物上皮细胞粘附分子(epithelial cell adhesion molecule,EpCAM)的癌症免疫疗法对小鼠安全无毒,而且可以显著延缓肿瘤的形成和生长。EpCAM在多种类型的肿瘤、循环肿瘤细胞和肿瘤干细胞中均过表达,因此这些发现具有广泛的意义。相关研究结果于近日发表在《Human Gene Therapy》特刊上。

图片来源:Human Gene Therapy。
特拉维夫大学博士、以色列基因与细胞治疗学会会长Adi Barzel博士是本期特刊的客座编辑。这篇文章题为“Preclinical Evaluation of Chimeric Antigen Receptor-Modified T Cells Specific to EpCAM for Treating Colorectal Cancer”,共同作者包括Wei Wang和一组来自华西医院、四川大学生物治疗协同创新中心和重庆医科大学第一附属医院的研究人员。
研究人员制造了第三代嵌合抗原受体修饰的T (chi-meric antigen receptor-modified T,CAR-T)细胞。他们使用慢病毒载体特异性靶向了细胞中的EpCAM。
“CAR-T疗法代表了一个治疗B细胞白血病和淋巴瘤患者的突破,但不幸的是在实体肿瘤治疗方面进展缓慢。”该杂志主编Terence R. Flotte医学博士说道。“这项针对结直肠癌患者的关键研究表明,靶向癌症免疫治疗确实可能在这种非常常见的恶性肿瘤中发挥作用。”
10.Nat Commun:中国科学家发现CAR-T来源的外泌体抗癌疗效显著、毒性低更安全
doi:10.1038/s41467-019-12321-3
表达嵌合抗原受体(CAR)的基因工程T细胞正迅速成为治疗血源性和非血源性恶性肿瘤的一种有前途的新疗法。CAR-T治疗可诱导快速和持久的临床反应,但却存在独特的细胞毒性。此外,CAR-T细胞疗法的疗效易受免疫抑制机制的影响。
近日来自上海交通大学、第二军医大学和Pharchoice Therapeutics Inc的研究人员发现CAR-T细胞会释放细胞外囊泡,主要以外泌体的形式存在,而这些外泌体的表面携带CAR。研究人员发现含有CAR的外泌体表达高水平的细胞毒性分子,可以显着抑制肿瘤生长。
通过进一步的实验,研究人员发现与CAR-T细胞疗法相比,CAR外泌体不表达程序性细胞死亡蛋白1 (PD1),重组PD-L1的治疗不会削弱CAR外泌体的抗肿瘤作用。研究人员在细胞因子释放综合征的体内临床前模型中进行的实验表明,CAR外泌体的应用相对于CAR-T治疗而言更安全。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


