头颈癌一线免疫治疗!阿斯利康抗PD-L1疗法Imfinzi(英飞凡)3期临床失败!
来源:本站原创 2021-02-10 00:54
头颈癌免疫治疗方面,默沙东Keytruda是第一个获批的免疫疗法,2020年全球销售额143.8亿美元。

2021年02月09日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)近日宣布,评估抗PD-L1疗法Imfinzi(英飞凡,通用名:durvalumab,度伐利尤单抗)一线治疗复发或转移性头颈癌的3期KESTREL试验没有达到改善总生存期(OS)的主要终点。
KESTREL是一项随机、开放标签、多中心、全球性3期试验,在先前没有接受过治疗的复发或转移性头颈部鳞状细胞癌(HNSCC)患者中开展,评估了Imfinzi、Imfinzi联用抗CTLA-4免疫疗法tremelimumab用于一线治疗的疗效和安全性,并与标准护理方案EXTREME(化疗+西妥昔单抗)进行了对比。该研究中,高PD-L1表达水平被定义为≥50%的肿瘤细胞或≥25%的肿瘤浸润性免疫细胞表达PD-L1。
该试验在全球23个国家的200多个临床中心开展,包括美国、欧洲、南美和亚洲的临床中心。主要终点是:在高PD-L1表达水平患者中Imfinzi单药治疗组的总生存期(OS)。关键次要终点是:接受Imfinzi+tremelimumab治疗的所有患者中的OS。
结果显示,与肿瘤表达高水平PD-L1的的复发或转移性HNSCC患者中,与标准护理方案EXTREME相比,Imfinzi单药治疗没有达到显著改善总生存期(OS)的主要终点。此外,在所有患者中,与标准护理方案EXTREME相比,Imfinzi+tremelimumab双重免疫治疗也没有显示出OS益处。该试验中,Imfinzi单药治疗、Imfinzi与tremelimumab联合治疗的安全性和耐受性与以前的试验一致。
该试验的数据将在适当时候共享。阿斯利康肿瘤事业部执行副总裁Dave Fredrickson表示:“转移性头颈癌是一种复杂且具有挑战性的疾病,预后很差。虽然我们对这些结果感到失望,但来自KESTREL 3期试验的见解将促进我们对免疫疗法在整个临床开发计划中的理解和应用。我们将继续利用Imfinzi在早期肺癌和小细胞肺癌方面的既定优势,为所有可能受益的患者提供免疫治疗选择。”
头颈癌(图片来源:Medgadget)
2020年,全世界有近75万名患者被诊断为头颈癌。其中三分之二的患者在晚期确诊,而接受治疗的患者中有超过一半最终复发。无法治愈或转移性复发患者的预后很差,中位生存期在1年以下。所有头颈部癌症中,90%以上起源于口腔、鼻腔和咽喉部鳞状细胞,称为头颈部鳞状细胞癌(HNSCC)。
Imfinzi(英飞凡,度伐利尤单抗)是一种人源化的PD-L1单克隆抗体,能够阻断PD-L1跟PD-1和CD80的结合,从而阻断肿瘤免疫逃逸并释放被抑制的免疫反应。截至目前,Imfinzi已在多个国家(包括美国、日本、中国、整个欧盟)被批准,用于接受铂类药物为基础的化疗同步放疗后未出现疾病进展的不可切除性、III期非小细胞肺癌(NSCLC)患者的治愈性治疗。此外,Imfinzi在欧盟、美国、日本和许多其他国家被批准用于治疗广泛期小细胞肺癌(ES-SCLC)患者,在美国和其他一些国家也被批准用于治疗既往接受过含铂化疗的晚期膀胱癌患者。
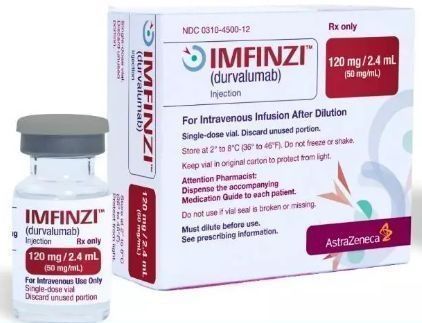
当前,阿斯利康正在开展一个大型临床项目,评估Imfinzi作为单药疗法以及联合tremelimumab和其药物的组合疗法用于NSCLC、SCLC、膀胱癌、头颈癌、肝癌、宫颈癌、胆道癌及其他实体瘤的治疗。
tremelimumab是一种人单克隆抗体,靶向细胞毒性T淋巴细胞抗原4(CTLA-4),阻断CTLA-4的活性、促进T细胞活化、启动肿瘤免疫反应、促进癌细胞死亡。tremelimumab与百时美施贵宝已上市抗体药物Yervoy(伊匹木单抗)靶向的是同一个靶点CTLA-4。
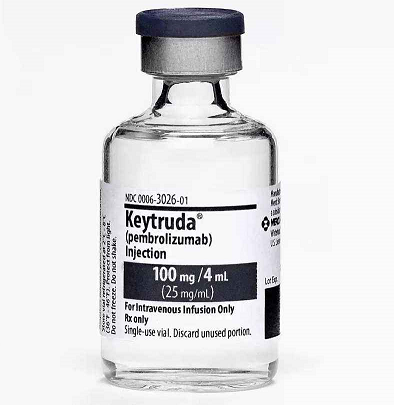
头颈癌免疫治疗方面,2019年6月,默沙东抗PD-1疗法Keytruda(可瑞达,通用名:pembrolizumab,帕博利珠单抗)获美国FDA批准2个新适应症,一线治疗转移性或不可切除性复发性HNSCC患者,具体为:(1)作为一种单药疗法,用于肿瘤表达PD-L1(合并阳性评分[CPS]≥1)的患者;(2)联合一种常用的化疗方案(铂+5-氟尿嘧啶[5-FU]),无论患者肿瘤PD-L1表达状态如何。
值得一提的是,Keytruda是首个获批一线治疗转移性或不可切除性复发性HNSCC患者的抗PD-1疗法,同时也是首个在这类患者中使总生存期(OS)在统计学上显著改善的抗PD-1疗法。
该批准基于关键性3期临床研究KEYNOTE-048(NCT02358031)的数据。这是一项随机、开放标签研究,旨在评估Keytruda作为单药疗法或与铂(顺铂或卡铂)及5-氟尿嘧啶化疗联合疗法相对于目前HNSCC一线治疗标准护理方案EXTREME(Erbitux[cetuximab,西妥昔单抗]+铂[顺铂或卡铂]+5-氟尿嘧啶联合疗法)的疗效和安全性。结果显示:在肿瘤表达PD-L1(CPS≥1)的头颈癌患者群体中,与一线标准治疗方案EXTREME相比,Keytruda作为单药疗法(HR=0.74[95%CI:0.61-0.90],p=0.00133)和联合化疗(HR=0.65[95%CI:0.53-0.80],p=0.00002)显著延长了总生存期(OS)。
Keytruda是属于PD-(L)1肿瘤免疫疗法,通过提高人体免疫系统的能力来帮助检测和对抗肿瘤细胞。Keytruda是一种人源化单克隆抗体,阻断PD-1与其配体PD-L1和PD-L2之间的相互作用,从而激活可能影响肿瘤细胞和健康细胞的T淋巴细胞。
截止目前,在全球范围内,已有多款PD-(L)1肿瘤免疫疗法获批,其中Keytruda是该领域的领头羊,已批准20多个治疗适应症,2020年的全球销售额高达143.8亿美元。(生物谷Bioon.com)
原文出处:Update on KESTREL Phase III trial of Imfinzi with or without tremelimumab in the 1st-line treatment of recurrent or metastatic head and neck cancer
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


