白血病告别化疗!罗氏/艾伯维Venclexta+美罗华组合治疗复发/难治CLL:四年生存率达85%!
来源:本站原创 2019-12-11 11:19
2019年12月11日讯 /生物谷BIOON/ --2019年第61届美国血液学会年会(ASH2019)于近日在美国佛罗里达州奥兰多召开。此次会议上,罗氏(Roche)与艾伯维(AbbVie)公布了靶向抗癌药Venclexta/Venclyxto(venetoclax)联合MabThera/Rituxan(rituximab,利妥昔单抗)治疗复发或难治性慢性

2019年12月11日讯 /生物谷BIOON/ --2019年第61届美国血液学会年会(ASH2019)于近日在美国佛罗里达州奥兰多召开。此次会议上,罗氏(Roche)与艾伯维(AbbVie)公布了靶向抗癌药Venclexta/Venclyxto(venetoclax)联合MabThera/Rituxan(rituximab,利妥昔单抗)治疗复发或难治性慢性淋巴细胞白血病(R/R CLL)关键性III期临床研究MURANO的更新数据。
四年随访数据显示,与苯达莫司汀(bendamustine)+MabThera/Rituxan(简写:BR)方案相比,Venclexta/Venclyxto+MabThera/Rituxan方案(简写:VenR)显示出持续的总生存期(OS)和无进展生存期(PFS)益处。研究中没有报告新的安全事件。
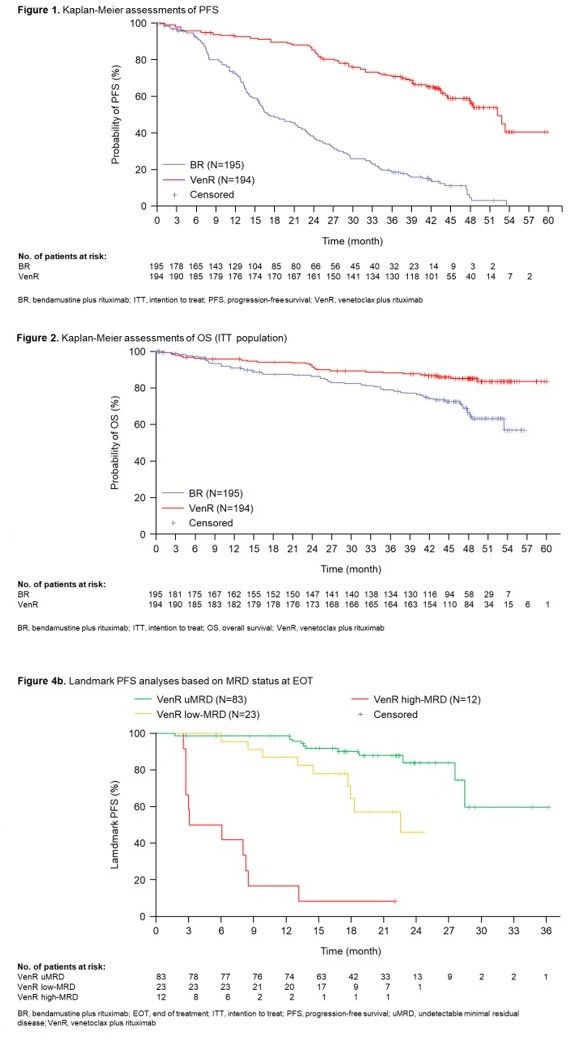
具体数据为:(1)与BR方案,VenR方案将疾病进展或死亡风险显著降低81%(HR=0.19;95%CI:0.14-0.25,p<0.0001);4年PFS率估计值,VenR方案组为57.3%(95%CI:49.4-65.3),BR方案组为4.6%(95%CI:0.1-9.2)。(2)与BR方案相比,VenR方案将死亡风险显著降低57.3%(HR=0.41;95%CI:0.26-0.65,p<0.0001);VenR方案组与BR方案组相比显示出持续更长的OS,4年OS率分别为85.3%和66.8%。(3)VenR方案组实现MRD阴性的患者在治疗结束时PFS表现出改善。(4)此次延长随访中,没有发现新的安全信号;与BR方案相比,VenR方案最常见的3-4级不良事件为白细胞介素低(58.8% vs 39.9%)、贫血(11.3% vs 13.8%)和血小板计数低(5.7% vs 10.1%)。
来自MURANO研究的结果是批准Venclexta/Venclyxto+MabThera/Rituxan方案(VenR)作为全球R/R CLL患者治疗方案的基础。
慢性淋巴细胞白血病(CLL)是最常见的白血病类型。CLL主要影响男性,确诊的中位年龄为70岁。在全球范围内,所有白血病的发病率超过每年40万例,CLL约占所有新诊白血病病例的三分之一。
Venclexta的活性药物成分为venetoclax,这是一种口服的B细胞淋巴瘤因子-2(BCL-2)抑制剂,BCL-2在细胞凋亡(程序性细胞死亡)中发挥重要作用,可阻止一些细胞(包括淋巴细胞)的凋亡,并且在某些类型癌症中过度表达,与耐药性的形成相关。venetoclax旨在选择性抑制BCL-2的功能,恢复细胞的通讯系统,让癌细胞自我毁灭,达到治疗肿瘤的目的。
Venclexta由艾伯维与罗氏合作开发,双方共同负责该药在美国市场的商业化,艾伯维负责美国以外市场的商业化(品牌名为Venclyxto)。目前,双方正在开展一个大型临床项目,调查venetoclax单药及组合疗法治疗多种类型血癌,包括CLL、霍奇金淋巴瘤(NHL)、弥漫性大B细胞淋巴癌(DLBCL)、急性髓性白血病(AML)和多发性骨髓瘤(MM)等。
在美国,Venclexta已被FDA授予5个突破性药物资格(BTD):1个授予先前未治疗的CLL、2个授予治疗复发或难治CLL、2个授予先前未治疗的急性髓性白血病(AML)。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


