食管癌(ESCC)免疫治疗!美国FDA受理百济神州/诺华抗PD-1抗体百泽安®(替雷利珠单抗)!
来源:本站原创 2021-09-14 01:35
在中国,默沙东Keytruda(可瑞达)已获批:一线、二线治疗ESCC。
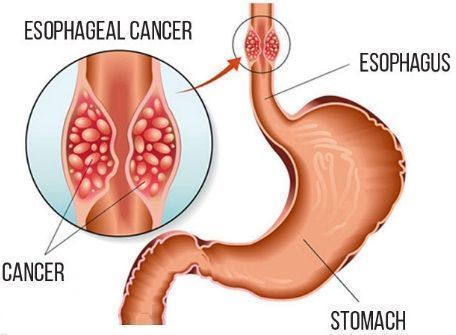
食管癌(图片来源:medindia.net)
2021年09月13日讯 /生物谷BIOON/ --百济神州(BeiGene)近日宣布,美国食品和药物管理局(FDA)已受理其抗PD-1抗体药物百泽安®(替雷利珠单抗注射液,tislelizumab)的生物制品许可申请(BLA),用于治疗既往经系统治疗后不可切除、复发性局部晚期或转移性食管鳞状细胞癌(ESCC)患者。FDA已指定该BLA的《处方药用户收费法》(PDUFA)目标日期为2022年7月12日。
值得一提的是,这是百泽安®在中国境外的首项药政申报,此前在国内已有5项适应症获批。此次BLA由百济神州与诺华联合申报。2021年1月,百济神州和诺华达成一项合作与授权协议,授权诺华在北美、欧洲和日本开发、生产和商业化百泽安®。
食管癌是一种毁灭性的疾病,5年生存率为19.9%,转移性疾病的5年生存率仅为5.2%。在临床试验中,百泽安®显示出了令人信服的结果:与化疗相比,显著延长患者生存,并具有良好的安全性。
目前,百泽安®治疗ESCC的新适应症申请也正在接受国家药品监督管理局(NMPA)的审查:作为一种单药疗法,用于治疗既往接受过一线标准化疗后进展或对一线标准化疗不耐受的局部晚期或转移性食管鳞状细胞癌(ESCC)患者。
此次上市申请是基于一项随机、开放标签、多中心全球3期临床试验RATIONALE 302(NCT03430843)的研究结果。该试验旨在评估百泽安®对比研究者选择的化疗,作为局部晚期或转移性ESCC患者二线治疗的有效性和安全性。共有512例来自亚洲、欧洲和北美的11个国家或地区的患者入组试验,这些患者以1:1的比例随机分配至百泽安®组或化疗组(化疗组的治疗方案为研究者选择的紫杉醇、多西他赛或伊立替康)。
该试验的主要终点是意向性治疗(ITT)人群的总生存期(OS);关键次要终点是PD-L1高表达人群(定义为目测估计综合阳性评分 [vCPS] ≥10%)的OS,其他次要终点包括无进展生存期(PFS)、客观缓解率(ORR)、缓解持续时间(DoR)和安全性,
今年6月初,百济神州在2021年美国临床肿瘤学会(ASCO 2021)年会上公布了该项临床试验的结果。数据显示,与化疗相比,百泽安®在ITT人群(主要终点)和PD-L1高表达患者(关键次要终点)中均显示出具有统计学显著性和临床意义的OS改善。
主要终点和关键次要终点数据为:(1)在ITT人群中,百泽安®组的中位OS为8.6个月、化疗组为6.3个月(p=0.0001;HR=0.70[95%CI:0.57,0.85])。百泽安®组6个月和12个月的OS率分别为62.3%和37.4%,化疗组分别为51.8%和23.7%。(2)在 PD-L1高表达患者中,百泽安®组的中位OS为10.3个月、化疗组为6.8个月(p=0.0006;HR=0.54[95%CI:0.36,0.79]),百泽安®组6个月和12个月的OS率分别为67.4%和44.0%,化疗组分别为50.8%和27.0%。
食管癌是消化道领域最常见的恶性肿瘤之一,在美国每年新发病例数约为1.84万例。根据癌发生的细胞,食管癌分为2种主要类型:鳞状细胞癌(ESCC)和腺癌(EAC)。ESCC约占美国食管癌病例的30%,是全球范围内最常见的食管癌类型。由于许多患者在疾病后期确诊,食管癌的治疗非常具有挑战性,总体预后仍然很差。在中国,食管癌是第五大最常见的癌症,也是第四大癌症死亡原因,90%的食管癌是ESCC。
百百泽安®(替雷利珠单抗)属于PD-(L)1肿瘤免疫疗法,这类疗法旨在通过提高人体免疫系统的能力来帮助检测和对抗肿瘤细胞。
截止目前,在全球范围内,已有10多款PD-(L)1肿瘤免疫疗法获批上市。其中,默沙东抗PD-1疗法Keytruda(可瑞达,通用名:pembrolizumab,帕博利珠单抗)是该领域的领头羊,2020年全球销售额高达143.8亿美元。排在第二位的百时美施贵宝抗PD-1疗法Opdivo(欧狄沃,纳武利尤单抗),在2020年的销售额为69.92亿美元。
在中国,Keytruda于2020年6月获得国家药监局批准,作为单药疗法,用于治疗先前系统疗法治疗失败、肿瘤表达PD-L1(合并阳性评分[CPS]≥10)的局部晚期或转移性食管鳞状细胞癌(ESCC)患者。这一新的适应症是根据全球III期KEYNOTE-181试验的总生存期(OS)结果获得完全批准,包括在中国患者中的扩展数据。来自中国患者的KEYNOTE-181研究扩展数据与KEYNOTE-181全球研究一致,显示:在肿瘤表达PD-L1(CPS≥10)的复发性或转移性ESCC患者中,与化疗相比,Keytruda单药治疗延长了总生存期(中位OS:12.0个月 vs 5.4个月)、死亡风险降低62%(HR=0.38[95%CI,0.19-0.77])。
2021年9月,Keytruda再获国家药监局批准,联合化疗(铂+氟嘧啶),一线治疗局部晚期不可切除性或转移性食管癌或胃食管连接部(GEJ)腺癌患者。截至目前,Keytruda在中国已被批准用于5种不同癌症的8个治疗适应症。
值得一提的是,Keytruda是中国批准一线治疗晚期食管癌或GEJ癌的第一个抗PD-1方案,无论其组织学或PD-L1表达如何。这一批准,将改变目前这类患者的一线治疗模式。在关键3期KEYNOTE-590试验中,无论组织学或PD-L1表达状态如何,与化疗相比,Keytruda+化疗方案显著延长了总生存期(中位OS:12.4个月 vs 9.8个月;HR=0.73,p<0.0001)和无进展生存期(中位PFS:6.3个月 vs 5.8个月;HR=0.65,p<0.0001)、显著提高了了总缓解率(ORR:45% vs 29%;p<0.0001)、延长了缓解持续时间(中位DOR:8.3个月 vs 6.0个月)。
食管癌是一种侵袭性、毁灭性的恶性肿瘤,死亡率高,除化疗外几乎没有其他治疗选择。对于新诊断、之前未经治疗的患者,迫切需要取得治疗进展。根据KEYNOTE-590试验结果,Keytruda是第一个联合化疗一线治疗食管癌与目前的标准护理化疗相比显示出优越OS、PFS、ORR疗效的抗PD-1疗法,无论肿瘤组织学或PD-L1表达状态如何。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


