2021年终盘点:肠道微生物组重磅级研究成果!
来源:本站原创 2021-01-02 17:43
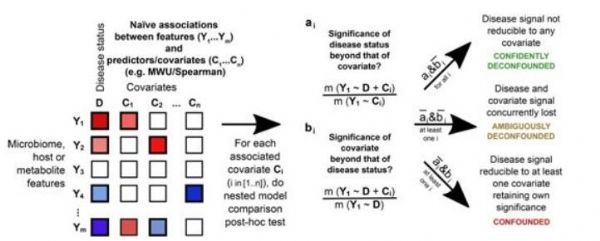
时至岁末,转眼间2021年已经接近尾声,迎接我们的将是崭新的2022年,在即将过去的2021年里,科学家们在肠道微生物组研究领域获得了多项重要研究成果,本文中,小编就对本年度科学家们在该研究领域取得的重磅级研究成果进行整理,分享给大家!一种针对多种药物和风险因素的消除单变量生物标志物分析的事后检测方法。图片来源:Nature, 2021, doi:10.10
时至岁末,转眼间2021年已经接近尾声,迎接我们的将是崭新的2022年,在即将过去的2021年里,科学家们在肠道微生物组研究领域获得了多项重要研究成果,本文中,小编就对本年度科学家们在该研究领域取得的重磅级研究成果进行整理,分享给大家!
一种针对多种药物和风险因素的消除单变量生物标志物分析的事后检测方法。
图片来源:Nature, 2021, doi:10.1038/s41586-021-04177-9。
【1】Nature:药物对肠道微生物组的影响比人们想象的要大
doi:10.1038/s41586-021-04177-9
我们是生活在地球上用药最多的几代人之一。2型糖尿病、肥胖和冠状动脉疾病等心脏代谢性疾病的发病率持续上升,并共同构成了全世界最高的死亡原因。受影响的人往往不得不连续数月甚至数年每天服用多种药物。如今,在一项新的研究中,位于德国海德堡的欧洲分子生物学实验室(EMBL)的Peer Bork团队与一个涉及20多个欧洲机构的欧洲MetaCardis联盟合作,发现许多常用药物对我们的肠道微生物有强大的影响。这些药物包括用于治疗心脏代谢紊乱的药物和抗生素。相关研究结果于2021年12月8日在线发表在Nature期刊上。
肠道微生物组由数十亿个对身体正常功能至关重要的微生物组成。Bork解释说,“我们分析了28种不同药物和几种药物组合的影响。许多药物对肠道细菌的组成和状态有负面影响,但包括阿司匹林在内的其他药物可以对肠道微生物组产生积极影响。我们发现,药物对宿主肠道微生物组的影响比疾病、饮食和吸烟的影响加起来还要明显。”
虽然抗生素对肠道细菌的负面影响和持久影响已经众所周知,但是这项新的研究表明,这种影响很可能会随着时间的推移而积累。论文共同第一作者、Bork团队前博士后研究员Sofia Forslund说,“我们发现在五年内服用多个疗程的抗生素的患者的肠道微生物组变得不太健康。”
研究者Maria Zimmermann-Kogadeeva说道,“我们想把疾病对宿主肠道微生物组的影响与药物的影响分开,特别是在同时服用一种以上药物的患者中。作为MetaCardis联盟的一部分,我们能够使用来自2000多名心脏代谢疾病患者的多组学数据。”这个大型队列还使得这些作者能够确定处方药物的剂量对肠道微生物组的影响水平也有重大影响。
【2】Immunity:在肠道微生物组中加入特定类型的细菌或能增强机体的抗肿瘤免疫力
doi:10.1016/j.immuni.2021.11.003
肠道微生物群落的组成与肿瘤的发展即机体抗肿瘤免疫力的效率均有关联,近日,一篇发表在国际杂志Immunity上题为“Microbiota-specific T follicular helper cells drive tertiary lymphoid structures and anti-tumor immunity against colorectal cancer”的研究报告中,来自匹兹堡大学等机构的科学家们通过研究发现,小鼠肠道微生物组中常见的一种细菌或能为机体免疫系统“充电”从而帮助抵御结肠中的癌细胞进展。
本文研究结果表明,肝螺旋杆菌(Helicobacter hepaticus)或能促进机体的适应性免疫反应,并促使辅助性T细胞和产生抗体的B细胞的选择性激活,并引发结肠肿瘤缩小从而延长小鼠的生存期;这项开创性的研究提供了强有力的证据来支持利用机体肠道菌群来治疗对常规药物和免疫疗法产生耐受性的晚期结肠癌肿瘤。
研究者Timothy Hand教授表示,改变肠道微生物组或许并不必依赖于偶然性来获得治疗优势;与其使用粪便移植并希望获得正确的微生物组成,如今研究人员更有条件基于有益细菌所产生的分子来开发更有效的药物疗法。结肠癌是一种常见的致命性疾病,由于肿瘤有能力修饰其所处的微环境并躲避免疫系统的识别,因此其并不会对免疫疗法产生反应。为了帮助这些患者,肿瘤学家不得不依赖于“更粗暴”的治疗方法,比如手术、化疗和放疗等,所有这些方法都会产生副作用,而寻找到一种新方法来使无法产生反应的癌症对免疫疗法产生反应或许有望改善癌症治疗的游戏规则。
【3】Cell:自闭症患者肠道微生物组的差异可能与饮食偏好有关
doi:10.1016/j.cell.2021.10.015
已有研究表明自闭症谱系障碍(autism spectrum disorder, ASD)可能至少部分是由肠道微生物群组成的差异引起的,其依据是观察到某些类型的微生物在自闭症患者中更常见。但是,在一项新的研究中,来自澳大利亚昆士兰大学等研究机构的研究人员这种关联性实际上可能反过来起作用:在自闭症儿童的肠道中发现的微生物物种多样性可能是由于他们与自闭症有关的限制性饮食偏好,而不是他们症状的原因。相关研究结果于2021年11月11日在线发表在Cell期刊上。
研究者Jacob Gratten说道,“人们对肠道微生物组在自闭症中的作用很感兴趣,但并没有很多确凿的证据。我们的研究是迄今为止最大的研究,旨在克服先前研究的一些局限性。”在过去的十年里,随着对肠道内微生物物种的下一代测序使得对肠道微生物组的分析更加自动化,耗时更少,一些研究已经探究了肠道内特定的微生物物种与心理健康之间的联系。这种肠-脑轴(gut-brain axis)不仅与ASD有关,而且还与焦虑、抑郁和精神分裂症有关。靶向肠道微生物群可能是一个不断增长的用于新疗法开发的研究领域。
在这项新的研究中,这些作者分析了247名2至17岁儿童的粪便样本。这些样本收集自99名被诊断为ASD的儿童,51名配对的未确诊的兄弟姐妹,以及97名无亲缘关系的未确诊的儿童。纳入分析的对象来自澳大利亚自闭症生物库(Australian Autism Biobank)和昆士兰双胞胎青少年大脑项目(Queensland Twin Adolescent Brain Project)。
【4】Cell Rep:年龄增长及机体衰老或会对肠道微生物组产生显著影响
doi:10.1016/j.celrep.2021.109765
肠道微生物的多样性会随着机体年龄的增长而逐渐减少,但当前的研究使用的是粪便样本进行的,其并不能代表整个机体肠道组织。近日,一篇发表在国际杂志Cell Reports上题为“Age and the aging process significantly alter the small bowel microbiome”的研究报告中,来自西达赛奈医学中心等机构的科学家们通过研究发现,衰老或会引起人类小肠组织的微生物组出现明显的改变,而这一点与药物或疾病负担所引起的变化不同。
研究者Ruchi Mathur博士指出,通过分析随着年龄增长、药物使用和疾病发生时小肠中所发生的微生物学变化,我们希望能够识别出微生物群落的特殊组分,从而以其作为靶点来帮助开发治疗性或干预性措施来促进机体的健康衰老。揭示肠道微生物组及其对机体健康的影响主要依赖于粪便样本,而这并不代表整个肠道组织,这篇研究报告中,研究人员对小肠组织进行了相关分析,旨在检测肠道微生物组及其与机体衰老之间的关联,小肠的长度超过了20英尺,其表面积相当于一个网球场那么大。
这篇研究中,研究人员首次分析了18-80岁参与者机体小肠中的微生物组成,如今他们知道,特定的微生物群体或受药物的影响更大,而其它微生物则受特定疾病的影响较大;研究人员识别出了一些仅会被个体机体实际年龄所影响的特定微生物。21世纪被称之为“肠道微生物组的时代”,因为随着研究的深入,如今科学家们对数以万亿计的肠道菌群、真菌和病毒在人类疾病和健康中所扮演的关键角色进行了极大的关注。微生物组是对存在于这些细胞中基因的总称,而有研究表明,微生物群体的功能紊乱或许会导致严重的疾病,包括胃肠道疾病、糖尿病、肥胖和一些神经系统疾病等。
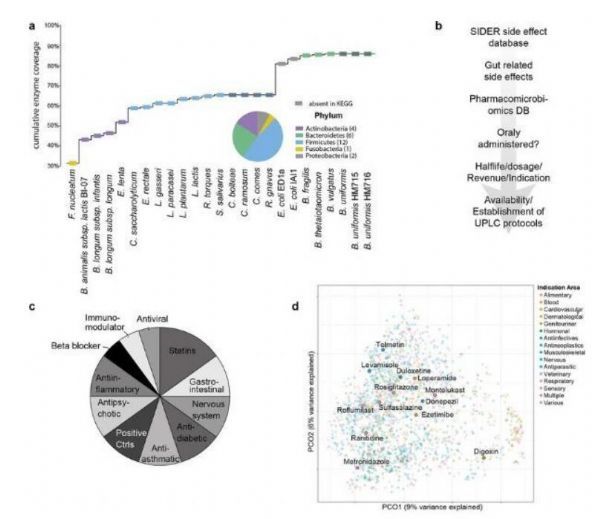
细菌和药物选择。
图片来源:Klünemann, M., et al.Nature (2021). doi:10.1038/s41586-021-03891-8
【5】Nature:重磅级发现!常见药物或能在人类机体肠道菌群中积累 或会降低药物的有效性且能改变肠道微生物组的功能!
doi:10.1038/s41586-021-03891-8
肠道中的细菌能帮助调节治疗性药物的可用性及疗效,然而研究人员最近才开始对药物和细菌之间相互作用进行系统性的分析,近日,一篇发表在国际杂志Nature上题为“Bioaccumulation of therapeutic drugs by human gut bacteria”的研究报告中,来自欧洲分子生物学实验室等机构的科学家们通过研究发现,普通的药物或能在肠道菌群中积累,从而改变细菌的功能并潜在降低药物的有效性,这种相互作用或能帮助更好地理解药物有效性和副作用的个体差异特性。
众所周知,细菌能化学性地修饰某些药物,这一过程被成为生物转化(biotransformation),这篇研究报告中,研究人员首次揭示了,特定的肠道菌群或能积累人类药物并改变细菌的类型及其活性。这或许会直接改变药物的有效性,因为药物在肠道菌群中的积累会降低机体对其可利用性,而且细菌的功能和组成的改变也与药物所产生的副作用有关。
文章中,研究人员培养了25种常见的肠道细菌,并分析了其与15种口服药物之间是如何相互作用的,选择的药物能代表一系列不同类型的药物,包括抗抑郁药物等,众所周知,这些药物对个体的影响是不同的,其会产生一定的药物副作用,比如肠道问题和体重增加等。研究人员检测了15种药物中每种药物是如何与选定的细菌相互作用的,总共进行了375次细菌-药物测试;结果发现细菌和药物之间存在70种相互作用,其中29种相互作用此前并未研究过。
尽管早期研究结果表明,细菌能化学性地修饰药物,但当科学家们进一步研究其相互作用时,他们发现,在29种新的相互作用的17种相互作用中,药物会在细菌中积累而不被修饰;让研究人员惊讶的时,目前他们所观察到的细菌和药物之间大部分相互作用是药物在细菌中的积累,因为截止到目前为止,生物转化被认为是细菌影响药物可用性的主要方式。这很有可能是个体之间的差异,其取决于个体机体肠道微生物的组成,研究人员甚至能在同一种类细菌的不同菌株之间观察到差异。
【6】Science:揭示肠道微生物组中的肠球菌增强免疫检查点抑制剂的抗肿瘤反应机制
doi:10.1126/science.abc9113
尽管一些科学家认为癌症患者对免疫疗法的反应与患者癌细胞突变和微卫星不稳定性有关,但是越来越多的研究表明肠道微生物组也可以影响接受PD-L1免疫疗法的癌症患者的治疗结果。Ayelet Sivan等人发现免疫检查点抑制剂对于患有癌症且肠道微生物缺失的小鼠的治疗效果并不明显(Science, 2015, doi:10.1126/science.aad1329)。Marie Vétizou等人发现肠道微生物种群的差异影响了接受PD-L1免疫疗法的黑色瘤小鼠模型中的肿瘤生长,并且发现肠道微生物组中的双歧杆菌是导致这种差异出现的一种关键的细菌类型(Science, 2015, doi:10.1126/science.aac4255)。Takeshi Tanoue等人鉴定并筛选出一种合理确定的源自人类微生物组的细菌菌株混合物可诱导产生干扰素γ(IFNγ)的CD8+ T细胞在肠道和肿瘤中积累,并协同性地加强对免疫检查点抑制剂和免疫挑战作出的反应(Nature, 2019, doi:10.1038/s41586-019-0878-z)。
这些研究结果意味着癌症免疫疗法的抗肿瘤疗效可能与肠道微生物组中某些细菌物种的存在相关。然而,影响宿主对免疫疗法反应的许多分子机制仍然难以捉摸。在一项新的研究中,来自美国洛克菲勒大学和斯克里普斯研究所等研究机构的研究人员发现在肠道微生物组中肠球菌属的成员能够改善小鼠肿瘤模型对免疫检查点抑制剂的反应。相关研究结果发表在2021年8月27日的Science期刊上。
这些作者发现活跃的肠球菌表达和分泌NlpC/p60肽聚糖水解酶SagA的同源物,该酶可以分解细菌细胞壁的成分。这一过程导致了胞壁肽(muramyl peptide)片段的释放,而这些片段又作为刺激性分子,促进先天免疫感应蛋白NOD2的信号传递,从而改善免疫治疗反应。SagA在非保护性粪肠球菌中的表达足以促进免疫治疗反应。
【7】Nature:百岁老人的独特肠道微生物组可能有助于长寿
doi:10.1038/s41586-021-03832-5
百岁老人不太容易受到与年龄有关的慢性疾病的影响,更有可能在传染病中存活下来。如今,一项新的研究显示,活到100岁或以上的人有一种独特的肠道微生物组,这种肠道微生物组可能会保护他们免受某些细菌感染,包括那些由耐多药细菌引起的感染。这些研究结果可能帮助人们开发治疗慢性炎症和细菌性疾病的新方法。相关研究结果于2021年7月29日在线发表在Nature期刊上。
这些作者研究了从160名平均年龄为107岁的日本百岁老人的粪便样本中发现的微生物。他们发现,与85至89岁的人和21至55岁的人相比,百岁老人的几种细菌含量更高,这些细菌产生称为次级胆汁酸的分子。次级胆汁酸是由结肠中的微生物产生的,并被认为有助于保护肠道免受病原体的侵害和调节身体的免疫反应。
这些作者接下来在实验室里用百岁老人体内升高的次级胆汁酸来处理常见的致病细菌。其中的一种称为isoalloLCA的次级胆汁酸分子,强烈抑制了艰难梭菌的生长,其中艰难梭菌是一种抗生素耐药菌,会导致严重的腹泻和肠道炎症。给感染了艰难梭菌的小鼠喂食补充了IsoalloLCA的食物,同样抑制了这种病原菌的水平。他们还发现,IsoalloLCA有力地抑制了许多其他革兰氏阳性病原菌的生长或将其杀死,这表明IsoalloLCA可能有助于身体保持健康肠道中微生物群落的微妙平衡。

肠道微生物菌群靶向性饮食或能调节人类机体的免疫状态。
图片来源:Hannah C. Wastyk,et al. Cell (2021) doi:10.1016/j.cell.2021.06.019
【8】Cell:富含发酵食物的饮食方式或能增加机体微生物组的多样性并能帮助降低机体炎症水平
doi:10.1016/j.cell.2021.06.019
饮食可以调节机体肠道微生物组,从而影响机体免疫系统的功能;近日,一篇发表在国际杂志Cell上题为“Gut-microbiota-targeted diets modulate human immune status”的研究报告中,来自斯坦福大学医学院等机构的科学家们通过研究发现,富含发酵食物的饮食方式或能增强机体肠道菌群的多样性并降低炎性分子信号的水平。
研究者表示,在一项临床试验中,他们招募了36名健康成年人,将其随机分配到为期10周的饮食模式中,其中包括发酵食物或高纤维食物,这两种饮食方式会对机体肠道微生物组和免疫系统产生不同的效应。摄入诸如酸奶、泡菜等食物会导致机体总体微生物多样性增加,其中较大的食物摄入分量会产生更大的影响。本文研究提供了一个例子揭示了饮食中的简单改变或能重塑健康人群机体中的微生物菌群。
此外,在摄入发酵食物的参与者组中,四类免疫细胞也表现出了较少的活性,血液样本中所测定的19种炎性蛋白的水平也随之下降了。其中一种名为白介素6的特殊蛋白则与多种疾病发生直接相关,包括风湿性关节炎、2型糖尿病和慢性压力等。研究者Christopher Gardner说道,靶向微生物的饮食模式或能改变机体的免疫状态,从而就为健康人群降低机体的炎症水平提供了一定的帮助。这一研究发现在所有被分配到摄入高发酵食物的研究组中是一致的。
相比之下,被分配到摄入富含豆类、种子、全谷物等高纤维饮食中的参与者机体中的19种炎性蛋白的水平并未发生下降;平均而言,其机体肠道微生物菌群的多样性也能保持稳定;研究者推测,高纤维饮食会产生普遍的有益影响,并增加微生物菌群的多样性,相关研究数据表明,仅在短时间内增加膳食纤维的摄入量或许并不足以增加机体的微生物多样性。目前有大量研究证据表明,饮食能塑造机体肠道微生物组,从而影响机体免疫系统的功能和整体健康;而较低的微生物组多样性则与肥胖和糖尿病发生直接相关。
doi:10.1038/s41586-021-03663-4
在一项新的研究中,来自德国柏林大学附属夏里特医院和美国福尼亚大学的研究人员能够首次发现,极低热量的饮食改变了人类肠道中存在的微生物群的组成。他们报告说,节食会导致特定细菌---特别是与抗生素引起的腹泻和结肠炎有关的艰难梭菌(Clostridioidesdifficile)---的增加。这些细菌通过影响肠道对营养物的吸收而明显地影响身体的能量平衡。相关研究结果发表在2021年7月8日的Nature期刊上。
人类的肠道微生物组由数万亿个微生物组成,并且因人而异。例如,在超重或肥胖的人中,已知他们的肠道微生物组组成与正常体重的人不同。我们中的许多人都会在我们生命中的某个时刻尝试节食,以减轻体重。但是这种饮食上的巨大变化对我们的身体有什么影响?这些作者在这项新的研究中解决了这个问题;研究者Joachim Spranger博士说道,“我们第一次能够证实,极低热量的饮食会使肠道微生物组的组成发生重大变化,这些变化对宿主的能量平衡有影响。”
为了探索节食的影响,这些作者对80名老年(绝经后)女性进行了为期16周的研究,她们的体重从轻微超重到严重肥胖不等。这些女性要么遵循医疗监督下的代餐方案,每天摄入总热量低于800卡路里的奶昔,要么在研究期间保持她们的体重。这些参与者在由夏里特和马克斯-德尔布吕克分子医学中心(MDC)联合运营的实验与临床研究中心接受检查。
定期的粪便样本分析显示,节食减少了肠道中存在的微生物数量,并改变了肠道微生物组的组成。论文第一作者、柏林大学附属夏里特医院内分泌学与代谢疾病系研究员Reiner Jumpertz von Schwartzenberg博士说,“我们能够观察到这些细菌如何调整它们的代谢,以便吸收更多的糖分子,并且通过这样做使它们不能被人类宿主所利用。”
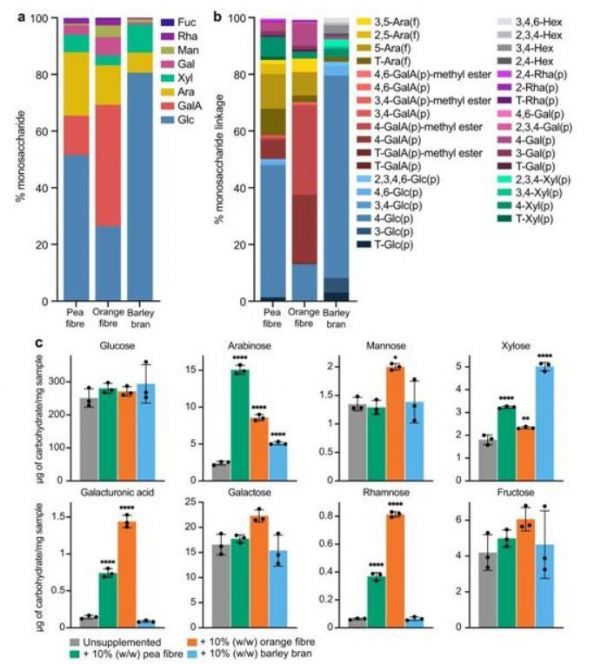
纤维制剂中单糖含量和糖苷键的存在,以及饲喂给无菌小鼠的未添加和添加纤维的HiSF LoFV饮食中的单糖含量和糖苷键。
图片来源:Nature, 2021, doi:10.1038/s41586-021-03671-4。
【10】Nature:新型含纤维零食可培育出健康的肠道微生物组
doi:10.1038/s41586-021-03671-4
在一项新的研究中,来自美国华盛顿大学圣路易斯医学院的研究人员鉴定出一些零食(snack food)原型的成分,这些零食原型经过精心设计,可以以与健康相关的方式改变肠道微生物组。相关研究结果发表在2021年7月1日的Nature期刊上。
这些作者将动物模型的结果进行了转化,在两项针对超重参与者的初步人体临床试验中显示,含有特别选择的纤维类型组合的零食会影响参与纤维成分代谢的肠道微生物组的成员。肠道微生物组的这种变化与一组血液蛋白的变化有关,这些血液蛋白是生理学和新陈代谢许多方面的生物标志物和调节因子。从长远来看,这些血液蛋白的变化可能改善健康状况。
研究者Jeffrey I. Gordon博士说道,“营养不良是全世界面临的一个紧迫而复杂的问题,由许多因素驱动,包括典型西方饮食中过多的高脂肪和低纤维食物。由于零食是西方饮食的一个流行部分,我们正在努力帮助开发人们喜欢吃的新一代零食配方。”
人类肠道是由几十万亿个微生物组成的肠道微生物组的家园,这些微生物含有数百万种不同的基因,其功能是人类基因组中大约2万个蛋白质编码基因所不能提供的。根据这些作者的说法,食物的营养价值部分是由它们经肠道微生物组代谢的独特产物决定的。
Gordon和他的同事们专注于确定哪些食物成分与肠道微生物组的哪些成分相互作用,以及这种相互作用如何塑造人类生物学的不同特征。其目标预示着营养科学的新时代,即从可持续的来源中产生可负担的、更有营养的食物,可用于治疗或预防各种形式的营养不良---无论是儿童或成人的营养不足或肥胖。
【11】Cell解读!科学家有望利用人类机体的肠道微生物组来开发治疗神经系统疾病的新型靶向性疗法!
doi:10.1016/j.cell.2021.02.009
当我们想到诱发神经系统疾病的原因以及如何治疗时,我们通常会想到针对大脑来进行研究;但这到底是不是最佳的方法或者唯一的方向呢?日前,一篇发表在国际杂志Cell上题为“Dissecting the contribution of host genetics and the microbiome in complex behaviors”的研究报告中,来自美国贝勒医学院等机构的科学家们通过研究发现,肠道中的微生物或许会诱发与复杂神经系统疾病相关的某些疾病症状,因此基于微生物的疗法未来或有望帮助治疗人类的神经系统疾病。
研究者Mauro Costa-Mattioli说道,机体不同的异常行为或许是由宿主的基因和其机体的微生物组进行相互依存调节的,具体而言,在神经发育障碍小鼠模型中,其多动行为是由宿主机体的遗传特性所空的,而社会行为缺陷则是由肠道微生物组所介导的。更重要的是,从治疗学的角度来讲,利用促进肠道中生物喋呤家族中特定化合物产生的特定微生物进行治疗,或者利用一种代谢活性的生物喋呤分子进行治疗,就能够改善机体的社会行为,但并不能改善机体的运动活性。
人类是宿主基因和微生物基因的携带者,虽然传统上大部分的关注点都在宿主基因上,但肠道微生物组(即生活在机体中的所有微生物群落)是遗传信息的另一个重要来源。本文研究为分析人类和微生物基因相互作用所诱发的神经系统疾病提供了一种不同的方法,相关研究结果表明,有效的治疗方法很可能需要同时针对大脑和肠道,从而解决所有症状,此外,研究人员还提出了另外一种可能性,即诸如癌症、糖尿病、病毒感染或其它神经性疾病等复杂的疾病或许也可能会携带微生物组的成分。
【12】Nat Med:重磅!机体肠道微生物组、日常饮食和代谢健康之间或密切相关!
doi:10.1038/s41591-020-01183-8
近日,一篇刊登在国际杂志Nature Medicine上的研究报告中,来自麻省总医院等机构的科学家们通过研究发现,富含健康和植物性食物的饮食方式或与特定肠道菌群的存在及丰度直接相关,而这些肠道菌群则与机体多种疾病的发病风险降低有关,比如肥胖、2型糖尿病和心血管疾病等。
研究者Chan说道,我们发现,肠道中特定的微生物种类、特定食物和某些常见疾病的风险之间存在明确的关联;我们希望能够利用这些信息来帮助人们通过改变日常针对其机体肠道微生物组的饮食方式,从而避免严重健康问题的发生。这项名为PREDICT 1(Personalized Responses to Dietary Composition Trial 1,膳食组成个体化反应试验1期)的宏基因组研究分析了参与者机体微生物组的组成、其饮食习惯和心血管代谢的血液生物标志物的水平,研究者发现了明确的证据表明,微生物组或与特定食物和饮食直接相关,微生物组的组成也与机体疾病的代谢生物标志物水平直接相关;此外,相比诸如遗传因素等因素而言,机体的微生物组也与这些生物标志物之间存在密切关联。
研究机体微生物组、饮食和疾病之间的相互关联往往涉及很多变量,因为目前人们的饮食趋向于个体化,而且会随着时间延续发生一些改变;这项试验的两个优点是参与者的数量和研究者所收集到的详细信息。PREDICT 1研究计划是一项国际化的联合研究项目,研究人员旨在阐明人群饮食、微生物组和心血管代谢的生物标志物之间的关联,他们从来自英国和美国近1100多名参与者中收集到了微生物组的测序数据、详细的长期饮食信息和数百种心血管代谢血液生物标志物的信息。结果发现,摄入富含健康基于植物食物的饮食的人群机体中特定肠道菌群的水平往往较高,而参与者肠道微生物组的组成与特定的营养物质、食物组分和一般的饮食指数之间存在强相关性,此外研究人员还发现了可靠的基于微生物组的肥胖生物标志物、心血管疾病和糖耐量受损的生物标志物。(生物谷Bioon.com)
生物谷2021年终盘点正在进行!更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。