克罗恩病(CD)新药!艾伯维IL-23抑制剂Skyrizi新适应症审查期遭美国FDA延长3个月!
来源:本站原创 2022-03-03 01:19
在临床研究中,接受Skyrizi治疗的患者中,有高比例患者实现临床缓解和内镜应答!
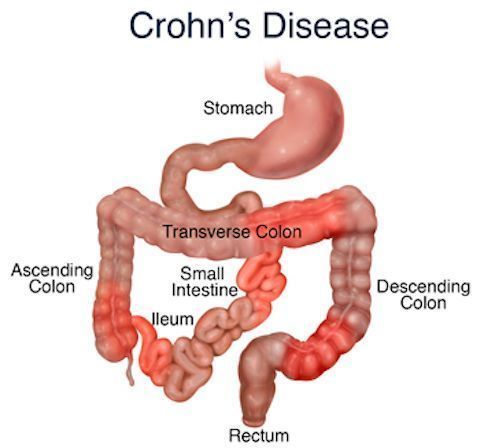
克罗恩病(CD)
2022年03月01日讯 /生物谷BIOON/ --艾伯维(AbbVie)近日宣布,美国食品和药物管理局(FDA)已延长了新型抗炎药IL-23抑制剂Skyrizi(risankizumab,150mg)一份补充生物制品许可申请(sBLA)的审查期。该sBLA寻求批准Skyrizi,用于治疗年龄≥16岁的中度至重度克罗恩病(CD)患者。
FDA已将sBLA的《处方药申报者付费法案(PDUFA)》的目标日期延长了3个月,以审查艾伯维提交的额外数据,包括关于贴身(on-body)注射器的信息。Skyrizi当前已批准的适应症不受此次审查延期的影响。
目前,Skyrizi治疗CD的新适应症申请也正在接受欧洲药品管理局(EMA)的审查,具体为:将Skyrizi 600mg静脉(IV)诱导和360mg(皮下)维持治疗方案,用于治疗对常规或生物制剂应答不足、失应答或不耐受的中度至重度活动性克罗恩病(CD)患者(年龄≥16岁)。
在美国和欧盟,Skyrizi已获批2个适应症:(1)用于治疗中度至重度斑块型银屑病(PsO)成人患者;(2)用于治疗活动性银屑病关节炎(PsA)成人患者。
CD新适应症申请,基于3项关键3期临床研究(ADVANCE,MOTIVATE,FORTIFY)的支持。在3期ADVANCE和MOTIVE诱导研究中,与安慰剂相比,接受600mg Skyrizi IV诱导治疗的患者中,达到2个主要终点(第12周临床缓解和内镜应答)的患者比例显著增加。
3期FORTIFY维持研究在接受Skyrizi IV诱导治疗有应答的患者中开展。数据显示,与停用Skyrizi的患者相比,接受Skyrizi 360mg SC维持治疗的患者中,有显著更高比例的患者在治疗一年(52周)后达到内镜应答和临床缓解。3项研究中,Skyrizi的安全性概况与该药已知的安全性概况一致,没有观察到新的安全风险。
克罗恩病(CD)是一种慢性系统性疾病,表现为胃肠道(或消化道)内的炎症,引起持续性腹泻、腹痛和直肠出血。该病是一种进行性疾病,意味着随着时间的推移病情会恶化。因为CD的体征和症状是不可预测的,不仅在身体上而且在情感上和经济上给患者造成巨大的负担。
Skyrizi的活性药物成分为risankizumab,这是一种单克隆抗体药物,通过特异性靶向IL-23p19亚基选择性阻断体内免疫炎性介质白细胞介素-23(IL-23),IL-23是一种细胞因子,被认为在许多慢性免疫性疾病中起着关键作用。risankizumab最初是由德国药企勃林格殷格翰(BI)研制,艾伯维在2016年2月支付一笔6亿美元的预付款获得了risankizumab的全球商业化权利。
目前,Skyrizi治疗银屑病、克罗恩病、银屑病关节炎的3期临床试验正在进行中。Skyrizi进入的是一个十分拥挤的市场,该药将与多款药物展开竞争,其中包括:诺华Cosentyx和Ilaris、礼来的Taltz、Valeant的Siliq、强生的Tremfya、太阳制药的Ilumya等等。这些药物中,Tremfya和Ilumya也是选择性靶向IL-23的生物疗法。
然而,尽管面临所有这些竞争对手,Skyrizi的销售表现非常强劲,2021年的全球销售额达到了29.39亿美元,较上一年增长幅度达84.9%。随着一系列3期临床试验的成功,艾伯维乐观预计,Skyrizi与另一款口服抗炎药JAK抑制剂Rinvoq在2025年的销售额将达到150亿美元,这将能够弥补旗舰产品Humira(修美乐,阿达木单抗)在美国市场自2023年开始遭遇生物仿制药竞争带来的销售损失。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


