转甲状腺素蛋白淀粉样变心肌病(ATTR-CM)药物!!辉瑞Vyndaqel/Vyndamax:治疗5年全因死亡率降低41%!
来源:本站原创 2021-12-22 01:08
Vyndaqel和Vyndamax是首创转甲状腺素蛋白(transthyretin)稳定剂tafamidis的2种口服制剂

ATTR-CM(图片来源:healthxchange.sg)
2021年12月21日讯 /生物谷BIOON/ --辉瑞(Pfizer)近日公布了一项事后中期分析报告,数据显示:在治疗5年期间,Vyndaqel(tafamidis meglumine)/Vyndamax(tafamidis)为转甲状腺素蛋白淀粉样变心肌病(ATTR-CM)患者提供了临床显著的生存益处,将全因死亡率降低了41%。这项分析报告来自3期ATTR-ACT及长期扩展(LTE)研究,数据已发表于国际医学期刊《Circulation: Heart Failure》。
这些长期结果进一步支持了初步分析中观察到的生存益处,强调了对ATTR-CM患者进行早期诊断并使用Vyndaqel/Vyndamax进行早期治疗的重要性。在Vyndaqel/Vyndamax获批之前,ATTR-CM患者的治疗方案仅限于症状管理,在少数情况下,还包括心脏(或心脏和肝脏)移植。ATTR-CM是一种罕见的危及生命的疾病,其特征是在心脏中积聚一种称为淀粉样蛋白的错误折叠蛋白,其定义为限制性心肌病和进行性心力衰竭。平均而言,确诊后未经治疗的患者只能存活2-3.5年。
在ATTR-ACT研究中,患者被随机分配接受Vyndaqel 80mg、20mg、或安慰剂,在30个月完成研究后可入组LTE研究。在LTE研究中,先前接受Vyndaqel 80mg治疗的患者继续这种治疗,然后转为生物等效单胶囊Vyndamax。在LTE研究中,在ATTR-ACT研究中接受安慰剂治疗的患者随机分配接受Vyndaqel 80mg或20mg,随后转为Vyndamax。Vyndamax 61mg与Vyndaqel 80mg生物等效,但基于mg不能互换。
在ATTR-ACT研究中,治疗30个月时,与安慰剂相比,Vyndaqel将死亡率降低30%。中位随访近5年,发表在《Circulation: Heart Failure》上的分析显示:与在LTE研究中过渡到Vyndaqel/Vyndamax之前首先在ATTR-ACT研究中接受安慰剂治疗的患者(中位随访57.1个月)相比,接受持续Vyndaqel/Vyndamax治疗的患者(中位随访58.5个月)全因死亡率降低了41%(HR=0.59;95%CI:0.44–0.79;p<0.001),具有临床意义。持续治疗组的中位生存期为67个月(95%CI:47.0–N/E),而安慰剂组为35.8个月(95%CI:29.7–41.1)。持续治疗组的初步5年生存率为53.2%,安慰剂组为32.4%。
所有亚组的死亡率降低是一致的,包括野生型和遗传型ATTR-CM。与安慰剂组相比,接受持续Vyndaqel/Vyndamax治疗的患者中,野生型ATTR-CM患者的全因死亡风险降低39%(HR=0.61;95%CI:0.43–0.87;p=0.006)、遗传型ATTR-CM患者减少43%(HR=0.57;95%CI:0.33–0.99;p=0.05)。
此外,分析表明,与安慰剂组相比,接受持续Vyndaqel/Vyndamax治疗的患者中,基线NYHA I或II级患者的全因死亡风险降低44%(HR=0.56;95%CI:0.38–0.82;p=0.003),基线NYHA III级患者的全因死亡风险降低35%(HR=0.65;95%CI:0.41–1.01;p=0.06)。在ATTR-ACT研究中,Vyndaqel的安全性与安慰剂相当。在整个LTE研究中未发现新的安全性问题,不良事件与安慰剂相似。
辉瑞全球产品开发部罕见病首席开发官Brenda Cooperstone医学博士表示:“本分析的结果建立在关键试验ATTR-ACT的积极初步结果基础上,并进一步证明Vyndaqel和Vyndamax有潜力显著延长ATTR-CM患者的生存期。这些患者没有其他批准的药物,Vyndaqel和Vyndamax代表着这些患者的治疗突破,ATTR-ACT和LTE研究表明,早期治疗对ATTR-CM患者至关重要。”
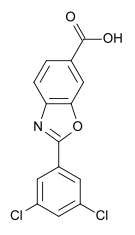
tafamidis分子结构(来自维基百科)
ATTR淀粉样变性是一种罕见的进行性疾病,其特征是由错误折叠的转甲状腺素蛋白组成的淀粉样沉积在人体器官和组织中的异常堆积。淀粉样变性可影响身体的许多器官和组织,包括外周神经系统,以及心脏、肾脏、胃肠道和眼睛等器官。ATTR-CM和ATTR-PN是该病的两种表现。
转甲状腺素蛋白淀粉样变心肌病(ATTR-CM)是一种罕见的、致命的、严重诊断不足的疾病,与渐进性心力衰竭相关。ATTR-CM是由名为转甲状腺素蛋白(TTR)的转运蛋白不稳定而引起的,该转运蛋白由4个相同的亚单元(四聚体)组成。在ATTR-CM中,不稳定的四聚体解离时发生心力衰竭,导致错误折叠的蛋白质聚集成淀粉样纤维并主要沉积在心脏中,最终导致心力衰竭。一经确诊,未经治疗的ATTR-CM患者的平均预期寿命仅为2-3.5年。
Vyndaqel和Vyndamax是首个被批准治疗野生型和遗传型ATTR-CM的药物。2款药物适用于治疗野生型和遗传型ATTR-CM成人患者,降低心血管死亡和心血管相关住院。
ATTR治疗药物(图片来源:seekingalpha.com)
Vyndaqel和Vyndamax是首创转甲状腺素蛋白(transthyretin)稳定剂tafamidis的2种口服制剂。tafamidis可选择性结合转甲状腺素蛋白,稳定转甲状腺素转运蛋白的四聚体,减缓导致ATTR-CM的淀粉样蛋白的形成。截至目前,tafamidis已在55个国家被批准用于治疗ATTR-CM,包括美国和欧盟。
Vyndamax 61mg和Vyndaqel 80mg是美国FDA批准用于治疗ATTR-CM的唯一剂量。Vyndamax 61mg是为方便患者而开发的每日一次口服胶囊,单粒Vyndamax 61mg胶囊与Vyndaqel 80mg(4粒20mg胶囊)生物等效,但基于mg不可互换。
2011年,Vyndaqel 20mg在欧盟首次获得批准,用于治疗1期症状性多发性神经病成人患者的转甲状腺素蛋白淀粉样变性(ATTR-PN),以延缓周围神经功能损害。目前,Vyndaqel 20mg已在40多个国家获批治疗ATTR-PN。在美国,Vyndaqel和Vyndamax尚未被批准用于治疗ATTR-PN。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



