诺华、拜耳等都在开发 IDH靶点在癌症治疗领域还有多大潜力?
来源:医药观澜 2020-08-12 12:24
由IDH突变导致的细胞内致癌代谢物(oncometabolites)积聚会促进肿瘤发展。近期发表在Nature上的一项研究揭示了癌症两个共同特征——代谢改变与基因组不稳定性之间的直接联系。这一研究为基于IDH开发肿瘤靶向疗法提供了新思路。目前,全球已有Idhifa和Tibsovo两款IDH抑制剂获批上市,包括新基(Celgene)、诺华(Nova
由IDH突变导致的细胞内致癌代谢物(oncometabolites)积聚会促进肿瘤发展。近期发表在Nature上的一项研究揭示了癌症两个共同特征——代谢改变与基因组不稳定性之间的直接联系。这一研究为基于IDH开发肿瘤靶向疗法提供了新思路。
目前,全球已有Idhifa和Tibsovo两款IDH抑制剂获批上市,包括新基(Celgene)、诺华(Novartis)、拜耳(Bayer)、基石药业、和黄医药、海和生物等众多公司均有涉足这一领域。另外一些另辟蹊径的做法也开始受到人们关注,如基于IDH突变形成的新酶活性、三级驱动基因改变等开发潜在疗法。今日,我们将为读者介绍IDH领域的最新研究进展。
IDH突变与肿瘤
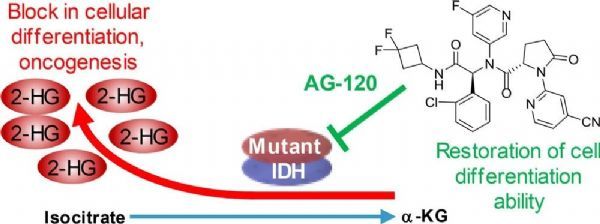
异柠檬酸脱氢酶(IDH)是人体内参与细胞能量代谢的限速酶,主要有IDH1、IDH2和IDH3三个亚型。其中,IDH1和IDH2基因突变会导致细胞内致癌代谢物2-羟基戊二酸(2-HG)的积聚。由于2-HG在结构上与α-酮戊二酸(α-KG)分子相似,2-HG的聚集将与α-KG竞争结合催化部位,从而抑制双加氧酶家族中的一些酶。
其中,有一种赖氨酸组蛋白去甲基化酶(KDM)能修饰染色质,催化DNA结合组蛋白3(H3)上的内赖氨酸氨基酸残基(K9)去甲基化。这个作用与修复DNA双链断裂的同源依赖性修复(HDR)途径相关。当发生DNA双链断裂时,H3K9会在损伤部位甲基化,这一局部甲基化信号可以帮助招募DNA修复因子。
然而,当IDH突变引起代谢物2-HG积聚时,相关酶的作用受到抑制,这会引起整个基因组发生H3K9高度甲基化。这将掩盖DNA损伤部位的H3K9局部甲基化信号,从而阻碍DNA修复因子的招募。未修复的DNA双链断裂,会导致基因组不稳定,进而促进肿瘤生长。
研究显示,在包括急性髓系白血病(AML)、神经胶质瘤、软骨肉瘤、前列腺癌、黑色素瘤和胆管癌等多种肿瘤中,均发现了IDH1和IDH2突变。此外,IDH还被编入《WHO中枢神经系统肿瘤分类指南》必检项目中,是指导脑胶质瘤分型和预后的关键基因。当下,IDH已成为肿瘤治疗领域的热门研究方向。
有望诞生新治疗策略
目前,全球已有两款IDH抑制剂获批上市,除了对急性髓系白血病有效,它还有望成为IDH1突变胆管癌患者的新型靶向疗法。不过,对于存在IDH突变的肿瘤而言,其潜在治疗方法远不止于此。
根据2018年在Cancer Cell刊登的一篇文章,除了针对IDH突变开发相关抑制剂外,一些研究还发现,基于IDH突变形成的新酶活性,可以寻找治疗IDH突变患者的潜在治疗靶点。另外,针对肿瘤进展过程中出现的三级驱动基因改变如IDH1 R132H进行靶向治疗,也有望成为肿瘤治疗潜在方法。
其中研究较多的一个方向是合成致死。我们知道,利用合成致死的原理,科学家已成功开发出可以阻碍DNA损伤修复的PARP抑制剂用以治疗特定癌症。在合成致死中,细胞能容忍单个基因功能的丢失,但是基因组合功能的同时丢失会导致细胞死亡。
研究发现,产生代谢物2-HG的肿瘤细胞在接受PARP抑制剂治疗时尤其容易死亡。同时,携带IDH1或IDH2基因突变的胶质瘤患者,对于可诱导DNA损伤的化疗和放疗联合疗法反应良好。
由此可见,针对IDH的研究和药物开发还有极大的潜力等待发掘。这个领域有望为肿瘤带来更多新的治疗策略。
已上市的两款IDH抑制剂
根据公开资料,全球已有多款IDH抑制剂正在开发中。这类产品通过作用于IDH突变位点,减少2-HG的产生,诱导组蛋白去甲基化,达到抑制肿瘤发展的效果。根据作用靶点不同,可以分为IDH1抑制剂、IDH2抑制剂和IDH1/IDH2抑制剂3种。
2017年8月,由Agios公司与新基公司带来的首款IDH2抑制剂Idhifa(enasidenib)被FDA批准上市,用于治疗携带IDH2基因突变的复发/难治性AML患者。在AML患者中,大约有8%~19%的患者带有IDH2突变。这种突变会抑制正常的血细胞发育,导致过多不成熟的血细胞产生。Idhifa通过抑制突变的IDH2蛋白来控制疾病发展。值得一提的是,该药还在2018年盖伦奖中摘得最佳生物技术产品奖。
2018年7月,由Agios公司发现并开发的一种全球首创的强效、高选择性口服突变型IDH1抑制剂Tibsovo(ivosidenib)在美国获批上市,成为全球首款IDH1抑制剂。目前,该药已被FDA批准用于治疗经检测携带IDH1突变的复发性或难治性AML,以及符合特定条件的新诊断AML成人患者。此外,它还获得FDA突破性疗法认定,用于治疗携带IDH1突变的复发或难治性骨髓增生异常综合征(MDS)。
除了针对AML患者,ivosidenib还在针对胆管癌的一项名为ClarIDHyd的全球3期试验中达到主要终点。研究显示,肝内胆管癌的病例中有近1/5患者携带IDH1基因突变。数据表明,对于危及生命的晚期胆管癌,携带IDH1突变的患者可以从Tibsovo得到显着的临床益处。
除了上述已上市的两款产品外,在中国境外还有多款IDH抑制剂目前正处于不同研究阶段,包括诺华的IDH305,拜耳的BAY1436032以及Forma Therapeutics的FT-2002等候选药。
基石药业、和黄医药、海和生物等正在开发
在中国,目前尚无靶向IDH抑制剂获批上市。但基石药业、和黄医药、海和生物、圣和药业等多家公司正在涉足这一领域。其中,基石药业从Agios公司引进的ivosidenib进展最快,目前正在进行多项注册性试验,预计将于2021年上半年在中国提交新药申请。
基石药业:Ivosidenib是Agios公司发现并开发的IDH1抑制剂,已在美国获批上市,基石药业拥有该药在大中华区的临床开发和商业化权益。在中国,基石药业已于2019年5月在中国台湾地区提交了ivosidenib的新药申请,预计将于2020年获得市场批准。此外,两项针对IDH1突变AML的注册性试验也正在中国进行中。其中,一项研究针对IDH1突变复发或难治性AML的注册性试验预计于2020年完成,并于2021年上半年在中国提交新药申请。
和黄医药:HMPL-306是一款IDH1/2双重抑制剂,为和黄医药第9个自主研发的创新肿瘤药物,拟开发适应症为伴有易感IDH1/2突变的血液肿瘤和实体肿瘤。据了解,HMPL-306有望解决潜在IDH突变体转化。目前,该产品在中国的1期临床试验已于7月下旬完成首位患者给药,该公司计划在未来半年在美国提交其IND并启动1期临床。在和黄医药的下一波创新开发计划中,HMPL-306是重点开发项目之一。
海和生物:HH2301是海和生物与上海药物所共同研发的一种新型、高效、特异性的mIDH1抑制剂。临床前研究显示,它具有优异的体内外抗肿瘤活性,在所有测试种属中均有良好的药代动力学性质和安全性。今年5月,该产品获得美国FDA临床试验默示许可,拟用于治疗IDH1突变的实体瘤,包括晚期胆管癌、软骨肉瘤和胶质瘤。
圣和药业:SH1573胶囊是圣和药业独立研发、具有自主产权的IDH2抑制剂,属化药1类新药,主要适应症为IDH2突变的AML。2019年6月,该产品在IDH2突变的复发或难治性AML患者中的多中心1/2期临床研究顺利召开。目前,该公司正在开展SH1573的1期临床研究。
此外,根据药物临床试验登记与信息公示平台,由正大天晴和赛林泰医药联合申报的1类新药TQB3455片已在中国登记开展3项1期临床试验,针对晚期恶性实体肿瘤或血液肿瘤患者,及IDH2基因突变的实体肿瘤和AML。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。