Cell:重大进展!利用改造的病毒样颗粒在体内高效递送基因编辑蛋白到宿主细胞中
来源:本站原创 2022-01-18 07:18
在一项新的研究中,来自美国布罗德研究所、加州大学欧文分校和宾夕法尼亚大学佩雷尔曼医学院等研究机构的研究人员开发出一种可以将基因编辑蛋白以足够高的效率递送到动物模型的细胞中并显示治疗效果的方法。
2022年1月18日讯/生物谷BIOON/---基因编辑方法有望治疗一系列的疾病,但事实证明,将用于基因编辑的试剂安全有效地递送到动物模型和人类细胞中充满挑战。如今,在一项新的研究中,来自美国布罗德研究所、加州大学欧文分校和宾夕法尼亚大学佩雷尔曼医学院等研究机构的研究人员开发出一种可以将基因编辑蛋白以足够高的效率递送到动物模型的细胞中并显示治疗效果的方法。相关研究结果于2022年1月11日在线发表在Cell期刊上,论文标题为“Engineered virus-like particles for efficient in vivo delivery of therapeutic proteins”。
在这项新的研究中,这些作者展示了他们如何使用改造的病毒样颗粒(engineered virus-like particle, eVLP)来递送碱基编辑器--在DNA中实现可编程的单碱基变化的蛋白---以及CRISPR-Cas9核酸酶,即一种在基因组中的目标位点切割DNA的蛋白。他们利用他们开发的eVLP让小鼠体内可能与高胆固醇水平有关的基因失效,并部分恢复了携带导致遗传性失明的基因突变的小鼠的视觉功能。
科学家们长期以来一直在研究病毒样颗粒(VLP)作为潜在的药物递送载体。VLP是由携带分子货物的病毒蛋白组成的小型结构,但不包含病毒的遗传物质,也不会引起感染。由于VLP缺乏病毒的遗传物质,它们可能比其他使用实际病毒的递送方法更安全,因为病毒可能将其遗传物质插入细胞的基因组中并可能导致癌症。
这些作者确定了VLP的几个限制其递送效率的特性,并对这种颗粒的结构进行了改造以克服这些瓶颈。他们说,由此产生的eVLP是首个向成年动物的多种组织递送治疗性基因编辑蛋白的VLP。
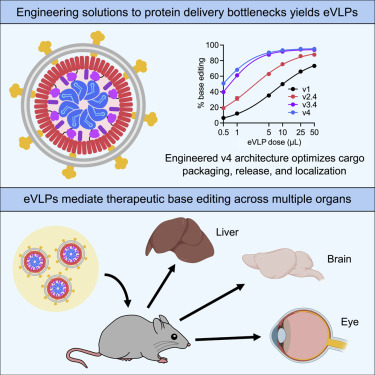
图片来自Cell, 2022, doi:10.1016/j.cell.2021.12.021。
在这项新的研究中,当利用eVLP将基因编辑复合物作为蛋白递送时,这些作者没有检测到任何脱靶编辑,但当基因编辑器作为DNA递送时却检测到了。他们的观察结果证实了之前的研究显示使用蛋白形式的基因编辑试剂的好处,并表明eVLP可以安全地传递它们。他们补充说,他们开发的eVLP有可能不仅用于基因编辑,还可用于递送其他的治疗性蛋白。
论文通讯作者、布罗德研究所默金医疗改革技术研究所主任David Liu教授说,“尽管体内递送是一个反复出现的挑战,但是它是未来基因编辑发挥主要作用的一个至关重要的方面。”
Liu说,“VLP一直是最有吸引力的递送技术之一,但一直受到体内蛋白递送效率低下的困扰。通过合理地开发分子解决方案来解决VLP递送过程中的具体挑战,我们开发了eVLP,它可极大地增加了在体外培养的细胞中的递送效力,同时也实现了在动物中的高效递送。”
递送瓶颈
几十年来,VLP一直受到科学家们的关注,因为它的行为与病毒相似,可以进入细胞并递送货物,如治疗性蛋白。人们可以通过使用VLP表面上的不同分子来影响它们在体内的最终目的地,比如肝脏或神经元。
为了利用这些特性并改递送效率,Liu及其研究团队系统性地改造了VLP架构的不同部分,以优化几个关键步骤---VLP的产生,货物如何被包装到VLP中,以及货物如何在细胞内释放和分布。
他们最终版本的eVLP包装的货物蛋白比他们以前设计的VLP多16倍,并且能够将细胞和动物中的编辑效率提高了8至26倍。正如他们所假设的那样,他们几乎没有看到在不希望的位点进行编辑的证据,也没有看到病毒DNA被整入用eVLP处理的细胞的基因组中。
论文共同第一作者、Liu实验室博士生Aditya Raguram说,“由于eVLP提供了强大的靶向编辑,并将非靶向编辑降至最低,我们希望它将作为一种更安全的方法,在体内递送基因编辑试剂。”
eVLP在起作用
这些作者使用他们优化的eVLP系统来校正一系列小鼠和人类细胞中的突变,在某些情况下观察到95%的编辑效率。
这些作者随后使用eVLP将碱基编辑器递送到小鼠的肝脏中,在那里他们有效地编辑了Pcsk9基因,其中这个基因一旦发生突变,就能大幅降低血液中的“坏”胆固醇水平,从而降低心脏病风险。他们发现单次注射经编程后引发Pcsk9基因突变的eVLP就能使Pcsk9的平均编辑率达到63%,Pcsk9蛋白水平下降78%。他们说,他们预计这些结果将大大降低个人患冠心病的风险。
这些作者还利用单次注射eVLP来恢复携带失明突变的小鼠的视觉功能。他们校正了Rpe65基因的突变,所实现的编辑效率与其他碱基编辑递送技术相当,但脱靶编辑和病毒DNA整合的风险较小。
这些作者还将eVLP直接注射到小鼠的大脑中,观察到暴露在eVLP下的细胞可实现大约50%的编辑效率。未来的研究工作将集中在改善eVLP在整个大脑中的分布,但是这些结果表明有望向极其难以靶向的器官递送基因编辑试剂。
论文共同第一作者、Liu实验室博士后研究员Samagya Banskota说,“eVLP结合了病毒递送系统和非病毒递送系统的优点。它也是可编程的,而且相对容易生产,这使它成为有前途的蛋白递送工具。我们期待着科学界采用我们的eVLP,并利用它改善对患者的治疗性大分子递送。”
Liu团队如今正在扩大eVLP在动物体内可以靶向的器官和细胞类型的范围。他们还将继续对eVLP进行表征,以更好地预测和减轻它们可能产生的任何不需要的免疫反应。
Liu说,“鉴于我们知道了一些关键的eVLP瓶颈,以及我们如何解决这些瓶颈,即使我们不得不为不寻常的蛋白货物开发新的eVLP,我们很可能可以做得更有效率。”他指出,他们的eVLP研究工作始于2018年初。
Liu说,“如今非常需要一种更好的方法,将蛋白递送到动物和患者体内的多种组织中。我们希望eVLP不仅可以用于递送碱基编辑器,还可以用于递送其他的治疗相关蛋白。”(生物谷 Bioon.com)
参考资料:
Samagya Banskota et al. Engineered virus-like particles for efficient in vivo delivery of therapeutic proteins. Cell, 2022, doi:10.1016/j.cell.2021.12.021.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


