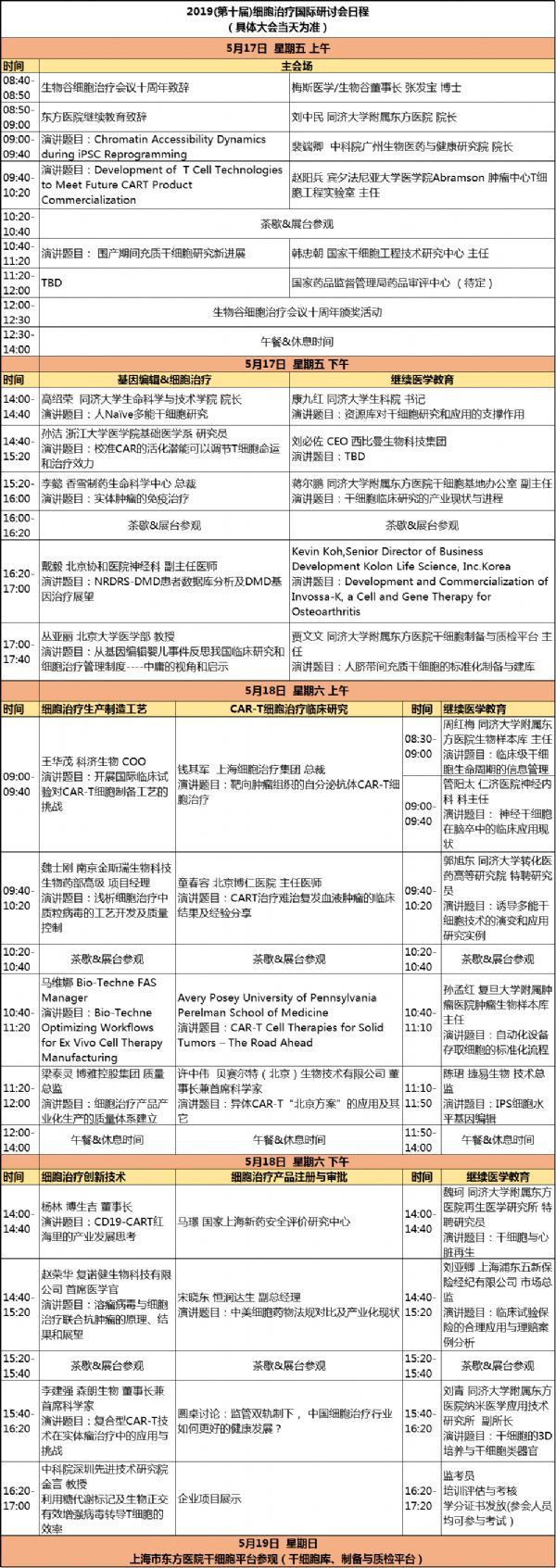
基因治疗方面的核心技术及产业前景
来源:本站原创 2019-05-05 11:19
一、 基因治疗:基于遗传操控的疾病治疗方案基因治疗是指用正常的基因导入人体细胞,以纠正或补充因基因缺陷和异常所引起的疾病,是一种根本性的治疗策略。导入的基因可以是与缺陷基因对应、在体内表达具有特异功能的同源基因,也可以是与缺陷基因无关的治疗基因。与常规的药物/治疗方案相比,基因治疗能从源头上解决疾病的发生,故而在一些目前无法治疗或疗效不佳的疾病上有明显优势,比如血友病等。在安全性上,基因
一、 基因治疗:基于遗传操控的疾病治疗方案
基因治疗是指用正常的基因导入人体细胞,以纠正或补充因基因缺陷和异常所引起的疾病,是一种根本性的治疗策略。导入的基因可以是与缺陷基因对应、在体内表达具有特异功能的同源基因,也可以是与缺陷基因无关的治疗基因。
与常规的药物/治疗方案相比,基因治疗能从源头上解决疾病的发生,故而在一些目前无法治疗或疗效不佳的疾病上有明显优势,比如血友病等。在安全性上,基因治疗仍属于新兴技术,基因更改后通常难以逆转,潜在风险较大。因此常规药物仍然是疾病治疗的首选方案,基因治疗更多地是作为常规治疗方案的补充。
二、 核心技术:转基因和基因编辑
(一)转基因技术发展早、更成熟,是目前基因治疗主流技术,但应用受限
基因治疗最初主要就是用于正常基因功能缺失遗传病的治疗,如联合免疫缺陷病(患者20号染色体上的遗传突变)。因此对于该类疾病的治疗,最直接的思路就是利用载体将正常基因导入患者体内实现治疗作用。目前最常用的载体就是人工改造后的工程病毒,目前临床上基因治疗使用最多的病毒载体就是逆转录病毒、慢病毒和腺相关病毒。
1. 逆转录病毒Retrovirus
逆转录病毒是由两条单链RNA、逆转录酶、核衣壳和包膜组成。其主要优势表现在感染效率高、感染细胞谱系广和基因稳定表达等。然而逆转录病毒载体其病毒本身的特性也带来了诸如病毒毒性、免疫原性、基因插入突变等诸多问题。
2. 慢病毒Lentivirus
针对第一代逆转录病毒的局限性,科学家又做了改进,发明了第二代逆转录病毒,主要代表就是慢病毒。慢病毒突破了“只感染分裂细胞”的局限性,对分裂细胞和非分裂细胞均可感染,可携带的目的基因片段更大,而且诱发癌变的风险也降低。但是病毒毒性、免疫原性、基因整合引起的宿主基因突变等问题依然存在。
3. 腺相关病毒AAV
腺相关病毒是一类单链线性DNA病毒,不能独立复制,只有在辅助病毒存在下才能感染并裂解宿主细胞。腺相关病毒的主要优势是基因组非整合性,其进入宿主细胞后是以游离DNA的形式存在,不会插入宿主基因组,也就不会引起宿主细胞基因组的插入突变,从而提高了基因治疗的安全性。腺相关病毒的另一个优势就是组织靶向性,不同亚型的病毒对不同的组织具有不同的亲和力。但是腺相关病毒也存在一些弊端,如可携带的基因片段小,且目的基因易被稀释等。
4. 非病毒载体
近年来科学家们开始利用非病毒载体将目的基因运送到患者细胞内,物理方法有显微注射、基因枪和电转导等,化学方法有脂质体和纳米颗粒等。非病毒载体具有低细胞毒性、弱免疫原性的优势,并且生产流程更加标准化,大规模生产更为容易。目前非病毒载体技术还在不断优化,待技术更加成熟以后,未来也会迎来更大的应用范围。
(二)基因编辑技术更强大,市场前景广阔
如果遗传疾病不是由于基因缺失,而是由于基因突变所导致的,那么转基因的策略就行不通了。对于这类疾病的治疗,就是需要把出错的基因找出来进行纠正,使其恢复到正常的状态,也就是基因编辑。基因编辑主要分为3个步骤:定位异常基因、切除异常基因片段和修补恢复成正常基因。目前主要的技术可分为锌指酶技术、转录激活样效应因子核酸酶技术和成簇规律性间隔的短回文重复序列技术三大类。
1. 锌指酶技术ZFN
一个锌指核酸酶由DNA识别域和DNA剪切域两部分组成。该技术主要的优势在于基因修复方式多样、精准更换基因、对基因表达强度影响较小。但是存在脱靶风险且细胞毒性较大,更大的问题是专利上的封锁,制约了该技术的进展和应用。
2. 转录激活样效应因子核酸酶技术TALEN
转录激活样效应因子核酸酶技术工作原理与锌指酶技术类似,均由DNA识别域和DNA剪切域组成,区别在于DNA序列的识别模式的区别。其工具蛋白设计更简便、可编辑性高、成本降低、细胞毒性也降低。但是TALEN的工具蛋白不可通用,不同的基因仍需特异性的设计,而且脱靶效应也存在很大的风险。
3. 成簇规律性间隔的短回文重复序列技术CRISPR
CRISPER系统的DNA定位和剪切元件由Guide RNA(gRNA)和Cas9蛋白组成,gRNA通过碱基互补原则结合到目标DNA上,Cas9也顺势结合发挥剪切活性,进而利用细胞自带的DNA修复系统实现基因编辑。与ZFN和TALEN相比,CRISPR系统设计简便、易于操作、可实现多基因编辑,但仍存在脱靶风险。科学家们一直致力于优化CRISPR系统,相信未来基因编辑将会是CRISPR的天下。
三、 基因治疗的行业现状:转基因仍是主流,基因编辑潜力巨大
(一)基因治疗临床意义重大
在部分适应症上,基因治疗比传统治疗方案有明显优势,但是仍然只是对传统治疗方案的补充,主要用于对传统治疗方案效果不佳、致病机制或治疗方案非常明确的疾病的治疗,如基因遗传病、肿瘤CAR-T疗法等。因此对于大部分疾病来说,未来传统治疗方案仍是主流。作为新兴产业,能够解决行业痛点的关键技术和人才仍是现阶段基因治疗行业最大的壁垒。
(二)国外多款产品接连上市,研发管线强劲;国内积极追赶,差距逐步缩小
近年来国外已有多款基因治疗产品上市,如诺华公司的CAR-T细胞疗法Kymriah2017年上市,用于治疗复发或难治性急性淋巴细胞白血病;Spark公司的AAV为载体的基因治疗药物AAV-RPE65(Luxturna),用于治疗RPE65基因缺陷引起的视网膜疾病;同月,FDA批准了Kite Pharma公司的CAR-T细胞疗法Yescarta上市,用于治疗成人复发/难治性大B细胞淋巴瘤。
临床在研项目众多,部分也取得了非常好的效果,进入到临床后期阶段,如美国Sangamo Therapeutics公司利用锌指核酸酶(ZFN)技术实现人类历史上首次患者体内基因组的编辑;Editas获批FDA首例CRISPR-CAS9体内基因编辑进入临床1/2期试验。目前国外基因治疗行业已经逐步跨入成长期,有望于未来几年迎来大爆发。美国FDA预测在2025年,他们将能每年批准10-20个细胞疗法或者基因治疗产品。
由于起步晚、基础科研薄弱、政策更进不及时等原因,在包括基因治疗在内的创新药领域国内企业一直落后于国外,更多是成为国际制药巨头的追随者。因此,目前国内基因治疗主要集中在国外已经取得突破的领域,如CAR-T疗法等。此外,基因治疗在经历了10多年的行业大整改之后刚刚进入成长期,国内外的差距远小于其他传统医药领域,国内企业仍有后来居上的潜力。5月17-18日,生物谷将举办2019(第十届)细胞治疗国际研讨会,本次会议的主题是“加快中国细胞治疗产品的上市”,设置主会场、基因编辑与细胞治疗专场、CAR-T与干细胞临床研究专场、细胞治疗生产制造工艺专场和细胞治疗产品注册与临床申报专场。 会议将继续以转化医学为切入点,以基础研究与临床应用相结合,邀请国内外顶尖的细胞治疗基础研究和临床专家,瞄准细胞治疗研究的最新研究动态和进展, 围绕上市从细胞治疗的临床监管、治疗规范、细胞治疗安全性,新型细胞治疗技术、实体瘤治疗、肿瘤免疫检查点抑制剂、间充质干细胞临床应用、干细胞移植治疗、基因编辑与细胞治疗、细胞治疗生产制造工艺等热门议题进行讨论。
基因治疗是指用正常的基因导入人体细胞,以纠正或补充因基因缺陷和异常所引起的疾病,是一种根本性的治疗策略。导入的基因可以是与缺陷基因对应、在体内表达具有特异功能的同源基因,也可以是与缺陷基因无关的治疗基因。
与常规的药物/治疗方案相比,基因治疗能从源头上解决疾病的发生,故而在一些目前无法治疗或疗效不佳的疾病上有明显优势,比如血友病等。在安全性上,基因治疗仍属于新兴技术,基因更改后通常难以逆转,潜在风险较大。因此常规药物仍然是疾病治疗的首选方案,基因治疗更多地是作为常规治疗方案的补充。
二、 核心技术:转基因和基因编辑
(一)转基因技术发展早、更成熟,是目前基因治疗主流技术,但应用受限
基因治疗最初主要就是用于正常基因功能缺失遗传病的治疗,如联合免疫缺陷病(患者20号染色体上的遗传突变)。因此对于该类疾病的治疗,最直接的思路就是利用载体将正常基因导入患者体内实现治疗作用。目前最常用的载体就是人工改造后的工程病毒,目前临床上基因治疗使用最多的病毒载体就是逆转录病毒、慢病毒和腺相关病毒。
1. 逆转录病毒Retrovirus
逆转录病毒是由两条单链RNA、逆转录酶、核衣壳和包膜组成。其主要优势表现在感染效率高、感染细胞谱系广和基因稳定表达等。然而逆转录病毒载体其病毒本身的特性也带来了诸如病毒毒性、免疫原性、基因插入突变等诸多问题。
2. 慢病毒Lentivirus
针对第一代逆转录病毒的局限性,科学家又做了改进,发明了第二代逆转录病毒,主要代表就是慢病毒。慢病毒突破了“只感染分裂细胞”的局限性,对分裂细胞和非分裂细胞均可感染,可携带的目的基因片段更大,而且诱发癌变的风险也降低。但是病毒毒性、免疫原性、基因整合引起的宿主基因突变等问题依然存在。
3. 腺相关病毒AAV
腺相关病毒是一类单链线性DNA病毒,不能独立复制,只有在辅助病毒存在下才能感染并裂解宿主细胞。腺相关病毒的主要优势是基因组非整合性,其进入宿主细胞后是以游离DNA的形式存在,不会插入宿主基因组,也就不会引起宿主细胞基因组的插入突变,从而提高了基因治疗的安全性。腺相关病毒的另一个优势就是组织靶向性,不同亚型的病毒对不同的组织具有不同的亲和力。但是腺相关病毒也存在一些弊端,如可携带的基因片段小,且目的基因易被稀释等。
4. 非病毒载体
近年来科学家们开始利用非病毒载体将目的基因运送到患者细胞内,物理方法有显微注射、基因枪和电转导等,化学方法有脂质体和纳米颗粒等。非病毒载体具有低细胞毒性、弱免疫原性的优势,并且生产流程更加标准化,大规模生产更为容易。目前非病毒载体技术还在不断优化,待技术更加成熟以后,未来也会迎来更大的应用范围。
(二)基因编辑技术更强大,市场前景广阔
如果遗传疾病不是由于基因缺失,而是由于基因突变所导致的,那么转基因的策略就行不通了。对于这类疾病的治疗,就是需要把出错的基因找出来进行纠正,使其恢复到正常的状态,也就是基因编辑。基因编辑主要分为3个步骤:定位异常基因、切除异常基因片段和修补恢复成正常基因。目前主要的技术可分为锌指酶技术、转录激活样效应因子核酸酶技术和成簇规律性间隔的短回文重复序列技术三大类。
1. 锌指酶技术ZFN
一个锌指核酸酶由DNA识别域和DNA剪切域两部分组成。该技术主要的优势在于基因修复方式多样、精准更换基因、对基因表达强度影响较小。但是存在脱靶风险且细胞毒性较大,更大的问题是专利上的封锁,制约了该技术的进展和应用。
2. 转录激活样效应因子核酸酶技术TALEN
转录激活样效应因子核酸酶技术工作原理与锌指酶技术类似,均由DNA识别域和DNA剪切域组成,区别在于DNA序列的识别模式的区别。其工具蛋白设计更简便、可编辑性高、成本降低、细胞毒性也降低。但是TALEN的工具蛋白不可通用,不同的基因仍需特异性的设计,而且脱靶效应也存在很大的风险。
3. 成簇规律性间隔的短回文重复序列技术CRISPR
CRISPER系统的DNA定位和剪切元件由Guide RNA(gRNA)和Cas9蛋白组成,gRNA通过碱基互补原则结合到目标DNA上,Cas9也顺势结合发挥剪切活性,进而利用细胞自带的DNA修复系统实现基因编辑。与ZFN和TALEN相比,CRISPR系统设计简便、易于操作、可实现多基因编辑,但仍存在脱靶风险。科学家们一直致力于优化CRISPR系统,相信未来基因编辑将会是CRISPR的天下。
三、 基因治疗的行业现状:转基因仍是主流,基因编辑潜力巨大
(一)基因治疗临床意义重大
在部分适应症上,基因治疗比传统治疗方案有明显优势,但是仍然只是对传统治疗方案的补充,主要用于对传统治疗方案效果不佳、致病机制或治疗方案非常明确的疾病的治疗,如基因遗传病、肿瘤CAR-T疗法等。因此对于大部分疾病来说,未来传统治疗方案仍是主流。作为新兴产业,能够解决行业痛点的关键技术和人才仍是现阶段基因治疗行业最大的壁垒。
(二)国外多款产品接连上市,研发管线强劲;国内积极追赶,差距逐步缩小
近年来国外已有多款基因治疗产品上市,如诺华公司的CAR-T细胞疗法Kymriah2017年上市,用于治疗复发或难治性急性淋巴细胞白血病;Spark公司的AAV为载体的基因治疗药物AAV-RPE65(Luxturna),用于治疗RPE65基因缺陷引起的视网膜疾病;同月,FDA批准了Kite Pharma公司的CAR-T细胞疗法Yescarta上市,用于治疗成人复发/难治性大B细胞淋巴瘤。
临床在研项目众多,部分也取得了非常好的效果,进入到临床后期阶段,如美国Sangamo Therapeutics公司利用锌指核酸酶(ZFN)技术实现人类历史上首次患者体内基因组的编辑;Editas获批FDA首例CRISPR-CAS9体内基因编辑进入临床1/2期试验。目前国外基因治疗行业已经逐步跨入成长期,有望于未来几年迎来大爆发。美国FDA预测在2025年,他们将能每年批准10-20个细胞疗法或者基因治疗产品。
由于起步晚、基础科研薄弱、政策更进不及时等原因,在包括基因治疗在内的创新药领域国内企业一直落后于国外,更多是成为国际制药巨头的追随者。因此,目前国内基因治疗主要集中在国外已经取得突破的领域,如CAR-T疗法等。此外,基因治疗在经历了10多年的行业大整改之后刚刚进入成长期,国内外的差距远小于其他传统医药领域,国内企业仍有后来居上的潜力。5月17-18日,生物谷将举办2019(第十届)细胞治疗国际研讨会,本次会议的主题是“加快中国细胞治疗产品的上市”,设置主会场、基因编辑与细胞治疗专场、CAR-T与干细胞临床研究专场、细胞治疗生产制造工艺专场和细胞治疗产品注册与临床申报专场。 会议将继续以转化医学为切入点,以基础研究与临床应用相结合,邀请国内外顶尖的细胞治疗基础研究和临床专家,瞄准细胞治疗研究的最新研究动态和进展, 围绕上市从细胞治疗的临床监管、治疗规范、细胞治疗安全性,新型细胞治疗技术、实体瘤治疗、肿瘤免疫检查点抑制剂、间充质干细胞临床应用、干细胞移植治疗、基因编辑与细胞治疗、细胞治疗生产制造工艺等热门议题进行讨论。
会议联系人:
何老师
E-mail: chunxing.he@medsci.cn
Mt: 17321098232
何老师
E-mail: chunxing.he@medsci.cn
Mt: 17321098232
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->