鼻内CGRP偏头痛新药!Biohaven第三代小分子CGRP受体拮抗剂BHV-3500进入III期临床开发
来源:本站原创 2019-04-02 15:10
2019年04月02日讯 /生物谷BIOON/ --Biohaven是一家临床阶段的生物制药公司,拥有一系列针对神经疾病(包括罕见疾病)的创新后期候选产品,其先导项目包括涵盖CGRP受体拮抗剂、谷氨酸调节、髓过氧化物酶抑制剂平台的多种化合物。近日,该公司宣布,评估鼻内给药BHV-3500治疗偏头痛急性发作的II/III期临床研究已完成受理患者入组。该项II/III期研究是一项随机、双盲、安慰剂对照

2019年04月02日讯 /生物谷BIOON/ --Biohaven是一家临床阶段的生物制药公司,拥有一系列针对神经疾病(包括罕见疾病)的创新后期候选产品,其先导项目包括涵盖CGRP受体拮抗剂、谷氨酸调节、髓过氧化物酶抑制剂平台的多种化合物。
近日,该公司宣布,评估鼻内给药BHV-3500治疗偏头痛急性发作的II/III期临床研究已完成受理患者入组。该项II/III期研究是一项随机、双盲、安慰剂对照、剂量范围研究,将比较3种剂量BHV-3500(5、10、20mg)治疗偏头痛发作时相对于安慰剂的疗效和安全性。该研究计划在每个治疗组中入组约400例受试者,旨在证明在给药后2小时内对疼痛和最烦人偏头痛相关症状等监管终点的缓解效果,同时检测对患者非常重要的其他临床措施的早期启用,包括疼痛缓解以及恢复正常功能的能力。该研究预计2019年第四季度获得顶线疗效和安全性结果。
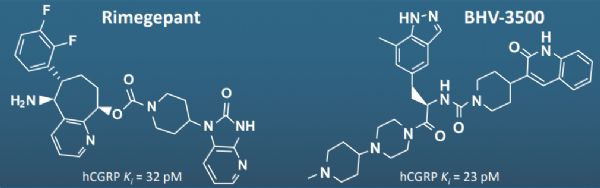
BHV-3500是一种新型、结构独特、低蛋白结合、高亲和力、第三代小分子降钙素基因相关肽(CGRP)受体拮抗剂,是第一种在后期临床研究中以鼻内(IN)制剂形式给药的CGRP受体拮抗剂,也是来自Biohaven公司NOJECTION偏头痛平台的第二个候选药物。BHV-3500在结构上不同于该公司先导药物rimegepant,该药计划今年第二季度在美国提交上市申请。BHV-3500的物理化学性质使其可能用于多种递送途径,包括鼻、吸入或口服,给药最初是作为一种鼻内制剂,开发用于急性偏头痛治疗。
BHV-3500与rimegepant结构差异
鼻内BHV-3500采用Aptar制药公司的单位剂量系统(UDS)给药,该系统旨在通过鼻内给药实现药物的全身性输送。目前,该系统已被批准用于在美国已上市的采用Aptar技术开发的多种产品。
来自I期临床研究的初步药代动力学(PK)数据显示,鼻内BHV-3500给药达到最大浓度(Tmax)的时间明显早于其他小分子CGRP受体拮抗剂。
BioHaven首席执行官Vlad Coric表示,“这是第一个后期临床试验,旨在评估鼻内给药的CGRP受体拮抗剂在急性偏头痛治疗中的疗效。我们最近完成的I期研究的PK数据证实了BHV-3500在无需注射的情况下超快速起效的可能性,这使其与其他CGRP拮抗剂区分开来,可能为患者提供一个重要的新治疗选择。BHV-3500是我们的先导偏头痛资产rimegepant的补充,后者在3项已完成的III期临床研究中达到了主要疗效终点,并具有良好的安全性。我们相信,鼻内BHV-3500可以为偏头痛患者群体提供超快速的偏头痛缓解,其便利的给药方式可以很容易地在偏头痛发作的任何时候和任何地方自我管理。”
CGRP领域竞争格局:3款单抗已上市,2款口服疗法争夺首发上市
CGRP及其受体在与偏头痛病理生理学相关的神经系统区域表达。CGRP受体拮抗作用是偏头痛急性治疗的一种新的作用机制,与现有的曲坦类(血清素1B / 1D激动剂)和阿片类药物的作用机制明显不同。目前,CGRP受体已成为偏头痛药物研发的热门靶点。
截至目前,已有3款靶向CGRP受体的单抗类偏头痛药物上市,分别为:诺华/安进Aimovig(erenumab-aooe)、梯瓦Ajovy(fremanezumab-vfrm)、礼来Emgality(galcanezumab-gnlm)。用药方面,Aimovig和Emgality均每月一次皮下注射,Ajovy则可每月一次或每3个月一次皮下注射,用药方面更具便利性,将为患者提供一种差异化的治疗选择。此外,Alder公司单抗药物eptinezumab(3月静脉输注1次)已于今年2月底在美国已提交申请,该药在某些患者中应答率高达100%。
另有一些公司正在开发口服CGRP受体拮抗剂,除了Biohaven公司的rimegepant之外,还包括艾尔建的ubrogepant和atogepant。今年3月11日,美国FDA受理了艾尔建ubrogepant用于成人偏头痛急性治疗的新药申请(NDA),并已指定处方药用户收费法(PDUFA)目标日期为2019年第四季度。
如果获得批准,ubrogepant有望成为美国市场过去25年来用于偏头痛(有或无先兆)急性治疗的首个口服CGRP受体拮抗剂。然而,山个月,Biohaven豪掷1.05亿美金从GW制药公司买进一张优先审评券(PRV),并计划今年第二季度向美国FDA提交口服CGRP受体拮抗剂Zydis(rimegepant)口腔崩解片的上市申请,这张PRV将用于该药NDA的加速审查,将审查周期由常规的10个月缩短4个月,在6个月内完成审查。这意味着,双方在争夺“首个口服CGRP受体拮抗剂”方面已展开直接对抗,究竟谁能拔得头筹,让我们拭目以待。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->