2020年终巨献:阿尔兹海默病研究领域重要研究成果解读!
来源:本站原创 2020-12-31 17:33
时至岁末,转眼间2020年已经接近尾声,迎接我们的将是崭新的2021年,在即将过去的2020年里,科学家们在阿尔兹海默病研究领域都取得了哪些重要的研究成果呢,本文中,小编就对本年度科学家们在该研究领域取得的重磅级研究成果进行整理,分享给大家!【1】bioRxiv:通过编辑人类神经细胞中的关键基因或有望改变其患阿尔兹海默病的风险doi:10.1101/2020
时至岁末,转眼间2020年已经接近尾声,迎接我们的将是崭新的2021年,在即将过去的2020年里,科学家们在阿尔兹海默病研究领域都取得了哪些重要的研究成果呢,本文中,小编就对本年度科学家们在该研究领域取得的重磅级研究成果进行整理,分享给大家!
图片来源:Pixabay/CC0 Public Domain
【1】bioRxiv:通过编辑人类神经细胞中的关键基因或有望改变其患阿尔兹海默病的风险
doi:10.1101/2020.10.27.357830
近日,一篇发表在预印版平台bioRxiv上的研究报告中,来自拉瓦尔大学等机构的科学家们通过研究表示,通过编辑神经细胞中的关键基因或能增加个体患阿尔兹海默病的风险,文章中研究人员描述了如何对相关基因进行编辑以及其所产生的影响效应。
此前研究结果表明,参与阿尔兹海默病发生的其中一个风险因素就是脑细胞中β-淀粉样蛋白的积累,而且某些人群机体中携带有名为A673T的基因突变,相比一般人群而言,表达该基因突变的人群患阿尔兹海默病的风险要比前者低4倍,这项研究中,研究人员通过研究编辑人类脑细胞使得个体机体携带基因突变A673T,同时他们发现这或许会降低个体患阿尔兹海默病的风险。
【2】Cell:阿尔兹海默症患者随年龄增长体内Tau蛋白的变化情况
doi:10.1016/j.cell.2020.10.029
长期以来,对阿尔茨海默氏病的研究一直集中在了解两种关键蛋白(β淀粉样蛋白和tau蛋白)的作用上。 tau蛋白的病变形式会在患者大脑组织中积累,从而有助于疾病的恶化。一项发表在Cell杂志的最新研究中,Judith Steen博士和Hanno Steen博士首次显示出这种病理性tau蛋白会随着时间的推移而改变其形式,这可能意味着它将需要多种药物才能有效地靶向。
多年以来,制药公司在开发针对β淀粉样蛋白的阿尔茨海默氏病药物方面的成功非常有限。最近,药物发现已经转向针对tau的药物的研发。这个新发现可能有助于目前针对tau的药物的开发,因为它表明该蛋白可能在疾病早期出现一组靶标,而在疾病后期则会发生改变。首席研究员Judith Steen说:“阿尔茨海默氏病中的tau蛋白在每个阶段看起来都不同。我们发现tau在与疾病严重程度相关的逐步过程中经历了一系列化学修饰。这表明我们需要针对疾病的每个阶段进行不同的诊断和治疗。”
【3】Nat Neurosci:大脑星形细胞过度激活与阿尔兹海默症发生之间的联系
doi:10.1038/s41593-020-00735-y
尽管阿尔茨海默氏病(AD)是一种常见且致命的神经退行性脑部疾病,但大多数AD治疗在解决其原因方面并未取得太大进展。许多AD药物的目标是消除β-淀粉样蛋白(Aβ)或淀粉样蛋白斑块,它们会阻止突触中的细胞间信号传导。但是,即使去除了淀粉样斑块,一些AD患者仍然表现出神经变性和认知能力下降。相反,即使在很高的Aβ水平下,许多人也没有神经退化和认知障碍的迹象。同样,关于星形非神经元细胞(星形胶质细胞)为何从AD发病初期就发生形状变化和功能变化,并在整个AD进展过程中以这种反应性状态继续存在的原因,目前还不清楚。
近日,韩国基础科学研究所(IBS)和韩国科学技术研究所(KIST)认知与社会研究中心的研究人员证明,“反应性星形胶质细胞”的严重程度是AD发病的关键指标,这使人们认识到对于当前的AD机制理论具有重要意义。在其基于毒素受体的动物模型中,研究小组对体内的星形细胞反应性进行了微调。他们发现,轻度反应性星形胶质细胞可自然逆转其反应性,而重度反应性星形胶质细胞可引起不可逆的神经变性,脑萎缩和认知缺陷。值得注意的是,这种严重的反应性星形胶质细胞诱导的神经变性已在注射病毒的app / PS1小鼠中成功复制。这些结果表明严重的反应性星形胶质细胞足以神经变性。
【4】PNAS & Cell Rep:科学家成功揭示阿尔兹海默病的新型治疗性靶点 有望开发新型靶向性疗法
doi:10.1073/pnas.2008762117
日前,发表在国际杂志PNAS和Cell Reports上的研究报告中,来自香港科技大学等机构的科学家们通过研究利用一种新开发的方法对患者大脑进行研究识别出了阿尔兹海默病的新型治疗靶点,这种新方法能帮助研究人员测定潜在药物对阿尔兹海默病患者的治疗效应,相关研究或为进行阿尔兹海默病研究及药物开发指明了方向。
尽管近些年来科学家们清楚研究了阿尔兹海默病发病的病理学机制,但目前针对这种疾病依然没有一种有效的治愈手段,其中一个原因就是常规的研究方法限制了科学家们用于识别药物开发分子靶点的能力,分子和病理学途径分析一般会将阿尔兹海默病患者的大脑作为一个单一的单元进行分析,通常也会低估不同脑细胞类型对阿尔兹海默病的作用及其异常表现;尤其是那些并不常见的细胞类型,比如小胶质细胞(大脑中固有的免疫细胞)和神经血管细胞(尤其是内皮细胞),其二者分别在总的大脑细胞群体中占到了不到5%和1%的比例。
【5】JNNP:新发现!中国科学家发现10种阿尔兹海默病发病风险因素!
doi:10.1136/jnnp-2019-321913
日前,一篇发表在国际杂志Journal of Neurology,Neurosurgery & Psychiatry上题为“Evidence-based prevention of Alzheimer's disease: systematic review and meta-analysis of 243 observational prospective studies and 153 randomized controlled trials”的研究报告中,来自中国复旦大学等机构的科学家们通过研究识别出了10种阿尔兹海默病发生的风险因素,这10种因素包括糖尿病、较差的BMI、较低的教育水平、中年高血压、低血压、头部创伤、高水平的高半胱氨酸、较低的认知活动水平、压力和抑郁症。
痴呆症是由一系列物理性的脑部疾病所引发,而最常见的痴呆症就是阿尔兹海默病,研究者表示,诸如阿尔兹海默病等疾病是由多种复杂的因素所引起,包括年龄、遗传因素和生活方式等。2017年,一项具有里程碑意义的研究报告就发现了9种与痴呆症发病相关的可修饰的风险因素,与这篇报告一样,这项最新研究中,科学家们回顾了此前发表的大量研究报告,有意思的是,研究人员发现,头部创伤及机体高半胱氨酸水平较高或与阿尔兹海默病发病风险直接相关。
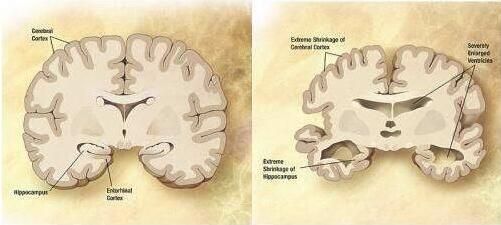
图片来源:Wikipedia/public domain
【6】Nat Rev Neurol:人工智能技术或有望加速并改善阿尔兹海默病的诊断
doi:10.1038/s41582-020-0377-8
近日,一项刊登在国际杂志Nature Reviews Neurology上的研究报告中,来自谢菲尔德大学等机构的科学家们通过研究表示,利用人工智能(AI)或能帮助快速诊断阿尔兹海默病并改善患者的预后;文章中,研究人员分析了在医疗领域中如何使用AI来帮助改善常见神经变性疾病给英国国民健康保险制度(NHS)所带来的时间和经济的影响,比如阿尔兹海默病和帕金森疾病等。
很多神经性障碍的主要风险因素是年龄,随着全球人群预期寿命的延长,患有神经变性疾病的患者的数量预计也会达到前所未有的数量,研究者预测,截止到2050年,仅阿尔兹海默病患者的数量就会增加两倍,达到1.15亿,这对健康卫生系统会带来一定的挑战;这项研究中,研究人员利用AI技术(比如机器学习算法)在疾病症状恶化前检测神经变性疾病,这就能够改善患者因成功疾病修饰疗法而获益的机会。
【7】Nature子刊深度解析!阿尔兹海默病与糖尿病发生之间的神秘关联!
doi:10.1038/s41594-020-0442-4
日前,一篇发表在国际杂志Nature Structural & Molecular Biology上的研究报告中,来自德国于利希研究中心等机构的科学家们通过研究揭示了阿尔兹海默病和糖尿病之间的分子关联;病理性蛋白团块的积累时一系列疾病发生的主要特征,比如阿尔兹海默病、帕金森疾病和2型糖尿病等。这项研究中,研究人员利用低温电子显微镜技术首次获得了单分子如何在蛋白质链中排列的清晰图像,这些蛋白质链构成了典型的糖尿病沉积物,原纤维的结构与阿尔兹海默病中原纤维的结构非常相似,相关研究发现或与此前研究人员发现的结果基本一致。
大约120年前,美国的医生Eugene Lindsay Opie在2型糖尿病患者胰腺中发现了不寻常的蛋白沉积物,其与多种神经变性疾病患者大脑中发现的沉积物非常相似,2型糖尿病是一种最广泛的疾病之一,此前被称为成人糖尿病,这种名为胰岛淀粉样蛋白的沉积物由称之为原纤维的小型蛋白线束组成,在糖尿病发生的情况下,其由肽类激素Iapp组成,而在胰腺中,其则会促进负责产生胰岛素的β细胞功能异常甚至死亡,胰岛素在帮助机体降低血糖方面扮演着非常重要的角色。
【8】JAMA Neurol:深度解析!科学家鉴别出能有效降低人群阿尔兹海默病风险的关键基因突变!
doi:10.1001/jamaneurol.2020.0414
目前大约有500万美国人都患有症状性的阿尔兹海默病,65岁及以上的人群中大约1人就患有该病,而85岁及以上人群中则有三分之一的患者;甚至有很多人都患有轻度认知障碍,即轻微的阿尔兹海默病前兆,大约一半这种症状的人群会转化为全面的阿尔兹海默病,当前有药物能在一定程度上减缓患者症状的进展,但并没有一种可用的药物能够完全阻断疾病的进展或者延长患者的寿命。
克洛索基因(Klotho,KL)是一种跨膜蛋白和长寿因子,其在减少年龄相关的疾病表型和认知能力下降中扮演着非常关键的角色,两种KL错义突变子( F352V [rs9536314]和C370S [rs9527025])当发生完全联动失衡(linkage disequilibrium)时就会形成名为KL-VS的功能性的单体型,研究人员发现,KL-VS的杂合性(heterozygosity)(即KL-VS HET+状态)能够增加KL在血清中的水平,并与携带杂合性主要或次要等位基因(KL-VS HET-)的个体相比时,其能对机体健康衰老和长寿施加一定的保护作用。
目前研究人员并不清楚是否KL-VS HET+状态能够保护机体抵御衰老相关的神经变性疾病,比如阿尔兹海默病(AD)等;近日,一项刊登在国际杂志JAMA Neurology上题为“Association of Klotho-VS HeterozygosityWith Risk of Alzheimer Disease in IndividualsWho Carry APOE4”的研究报告中,来自斯坦福大学等机构的研究人员通过研究在寻找能与APOE4(载脂蛋白e4)等位基因相互作用降低阿尔兹海默病风险的遗传因素时,他们发现,KL-VS的杂合状态或能保护机体抵御年龄相关的表型变化及认知功能下降,但目前研究人员并不确定其是否能保护携带APOE4的人群免于AD。
【9】Nat Med:迄今为止最大规模的蛋白质组学研究揭示葡萄糖代谢蛋白与阿尔兹海默病之间的神秘关联!
doi:10.1038/s41591-020-0815-6
如今我们对阿尔兹海默病的病理生理学机制了解地仍然并不完全,近日,一篇发表在国际杂志Nature Medicine上题为“Large-scale proteomic analysis of Alzheimer's disease brain and cerebrospinal fluid reveals early changes in energy metabolism associated with microglia and astrocyte activation”的研究报告中,来自埃默里大学医学院等机构的科学家们就通过利用定量质谱法和共表达网络分析技术进行了迄今为止最大规模的蛋白质组学研究将机体的葡萄糖代谢蛋白与阿尔兹海默病(AD)疾病生物学特性联系了起来。
蛋白质网络模块能与糖代谢联系起来作为一种最常见的模块,同时成为与AD病理学和机体认知相关最相关的模块之一;这种模块能够富集AD遗传风险因素及与抗炎性状态相关的小胶质细胞和星形胶质细胞蛋白标志物,这就表明,其所代表的生物性功能在AD发病过程中扮演着关键角色,而来自该模块的蛋白质在疾病发病早期的脑脊液中水平会发生升高。这项研究中,研究人员识别出了疾病特异性的蛋白和生物学过程,其或能帮助开发新型的靶向性疗法,此外他们还发现,能调节机体葡萄糖代谢的一组蛋白及在小胶质细胞和星形胶质细胞中扮演保护性角色的蛋白或与阿尔兹海默病的病理学进展及机体认知损伤强烈相关。
【10】Cell Rep:炎症或会诱发阿尔兹海默病的致命性循环
doi:10.1016/j.celrep.2020.02.025
日前,一篇发表在国际杂志Cell Reports上的研究报告中,来自波恩大学等机构的科学家们通过研究发现,大脑中出现的一种免疫反应似乎在阿尔兹海默病发生过程扮演着关键角色,在某种程度上,其或许会“火上浇油”并引发炎症,而且从某种意义上来讲,炎症会不断持续并影响患者机体健康。阿尔兹海默病的主要特点为β淀粉样蛋白(Aβ)的积累,其会在大脑中形成较大的斑块,Aβ就好像某些细菌表面上的分子;在过去数百万年李,有机体会进化出特殊的防御机制来抵御某些结构,这些机制时由基因所决定的,因此其属于所谓的先天性免疫系统的组分,其通常还会导致某些清道夫细胞吸收和消化分子。
在大脑中,小胶质细胞一直承担着这一角色,但这样做就会触发破坏性的过程,这似乎在很大程度上与痴呆症发生直接相关,当与Aβ接触后,诸如炎性小体等特殊的分子复合体就会在小胶质细胞中被激活,随后他们就类似于外部携带酶的轮子一样移动,这就会激活免疫信使分子,并通过将额外的免疫细胞引导至作用部位来诱发炎症。

图片来源:public domain
【11】Neurology:震惊!仅一晚不睡就会增加年轻男性患阿尔兹海默病的风险
doi:10.1212/WNL.0000000000008866
近日,一项刊登在国际杂志Neurology上的研究报告中,来自乌普萨拉大学的科学家们通过研究发现,当年轻男性仅仅一晚上没睡眠时,其机体血液中tau蛋白的水平就要比其夜晚充足睡眠时要高,tau蛋白是阿尔兹海默病的一种关键生物标志物。Tau蛋白是神经元中的一种特殊蛋白,其能形成缠结,同时其会在阿尔兹海默病患者的大脑中积累,在患者疾病症状出现之前,其就开始已经在大脑中形成了;此前对老年人的研究结果表明,睡眠不足(sleep deprivation)会增加机体脑脊液中中tau蛋白的水平,头部创伤也会增加血液中循环tau蛋白的浓度。
医学博士Jonathan Cedernaes指出,我们很多人都会在一生的某个阶段因为时差、熬夜完成项目、轮班工作、加班或工作不稳定而睡眠不足,这项研究中,我们发现,及时是年轻健康人群,少睡一晚也会增加其机体血液中tau蛋白的水平,这就表明,随着时间推移,睡眠不足或许会对机体健康产生有害的影响。
【12】Neuron:疱疹病毒感染真的与阿尔兹海默病发生有关?科学家们提出质疑!
doi:10.1016/j.neuron.2019.11.009
日前,一项刊登在国际杂志Neuron上的研究报告中,来自贝勒医学院的研究人员通过研究反驳了疱疹病毒水平升高与阿尔兹海默病发病风险之间的关联,文章中研究人员提供了一种新型统计学和计算框架来对大规模的测序数据进行分析。目前全球大约有5000万人遭受阿尔兹海默病的折磨,这是一种进行性的老年痴呆症,其会引发记忆、认知能力和言语技能的缺失,而且如今患者数量在不断增加;当前可用的疗法往往只能暂时减缓患者的症状或记忆丧失的速度,从而能最大限度地延长患者独立生活和工作的时间,目前并没有有效的疗法能减缓阿尔兹海默病的进展。
研究者Zhandong Liu说道,与所有类型的痴呆症一样,阿尔兹海默病的主要特征为大量神经元细胞的死亡,识别出神经元为何会在阿尔兹海默病大脑中发生死亡或许有望帮助阐明这种疾病的发病机制并开发出新型疗法。此前有研究理论认为,诸如某些病毒等微生物感染或会诱发阿尔兹海默病,此外,2018年一项研究表明,与健康老龄化受试者或遭受其它形式神经变性疾病的患者的大脑组织相比,研究者对1000多名阿尔兹海默病患者的尸检脑组织进行分析后发现,人类疱疹病毒6A(HHV-6A)和人类疱疹病毒7(HHV-7)的水平增加了。
【13】Science子刊解读!降低YKL-40蛋白表达水平有望延缓阿尔茨海默病进展
doi:10.1126/scitranslmed.aax3519
睡眠中断、白天困倦和其他昼夜节律紊乱的症状是阿尔茨海默病患者常见问题,而且随着疾病的进展,这些问题会越来越严重。但是,阿尔茨海默病和昼夜节律紊乱之间存在关联性的原因还不是很清楚。在一项新的研究中,来自美国华盛顿大学圣路易斯医学院的研究人员表示,一个线索可能在于大脑蛋白YKL-40。他们报道YKL-40既受时钟基因的调控,又参与清除大脑中潜在的阿尔茨海默病蛋白的毒性堆积。此外,他们发现,携带降低YKL-40水平的基因变体的阿尔茨海默病患者比没有携带这种变体的人保持认知能力的时间更长。相关研究结果发表在Science Translational Medicine期刊上。
这些研究结果表明,YKL-40是昼夜节律紊乱和阿尔茨海默病之间的可能联系,靶向这种蛋白的疗法可能会减缓这种疾病的进程。研究者Erik Musiek博士说,“如果你的昼夜节律时钟(circadian clock,即生物钟)多年来都不太正确---你经常遭受夜间睡眠中断和白天打盹的痛苦--慢性失调的累积效应可能会影响炎症途径,从而使你积累更多的淀粉样蛋白斑块。”大脑中的淀粉样蛋白斑块是阿尔茨海默病的早期特征之一。“我们希望更好地了解昼夜节律时钟如何影响YKL-40,可能为减少大脑中的淀粉样蛋白堆积带来新的策略。”
【14】Science:重磅!非典型的转亚硝基化级联反应导致阿尔茨海默病中的突触丢失
doi:10.1126/science.aaw0843
阿尔茨海默病影响了全球约5000万人。在一项新的针对阿尔茨海默病的研究中,来自美国斯克里普斯研究所等研究机构的研究人员揭示了大脑中一个以前不为人知的导致突触破坏的生化级联反应,其中突触是负责记忆和认知的神经细胞之间建立的连接。这些研究结果为发现治疗阿尔茨海默病的药物提供了一个新的角度。相关研究结果发表在Science期刊上。
这种新发现的一系列异常化学事件,被称为“蛋白转亚硝基化反应(protein transnitrosylation reaction)”,导致突触丧失,而突触丧失是阿尔茨海默病患者中的记忆丧失和认知能力下降的主要驱动因素。Lipton解释说,最近开发阿尔茨海默病治疗方法的大多数尝试都是针对称为β淀粉样蛋白的粘性蛋白,这种蛋白在患者的大脑中积累,破坏细胞通信并引起炎症。然而,由于各种原因,这些尝试在临床试验中失败了。
doi:10.1038/s41586-020-2681-2
-阿尔茨海默氏病是一种神经退行性疾病,其特征是大脑中β淀粉样蛋白团块的聚集。揭示导致这些团块(称为斑块)形成的原因以及它们在疾病进展中起什么作用,是目前该领域的研究热点,并且对于制定预防和治疗策略至关重要。最近的研究发现,β-淀粉样蛋白具有抗病毒和抗菌特性,这表明针对感染的免疫反应与阿尔茨海默氏病的发展之间可能存在联系。
研究人员发现了这种联系的明确证据:一种名为IFITM3的蛋白质参与对病原体的免疫反应,同时在斑块中β淀粉样蛋白的积累中也起着关键作用。研究者表示,我们知道免疫系统在阿尔茨海默氏病中起作用,例如它有助于清除大脑中的β-淀粉样斑块。但这是第一个直接证据表明免疫反应促进了β-淀粉样蛋白斑的产生。(生物谷Bioon.com)
生物谷2020年终盘点正在进行!更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


