非转移前列腺癌新药!美国FDA批准拜耳Nubeqa(达罗他胺)处方信息更新:3期临床显著延长生存期!
来源:本站原创 2021-01-12 15:13
与安慰剂相比,Nubeqa显著延长生存期、显著延缓癌症相关症状出现时间、将毒性降至最低。

2021年01月12日讯 /生物谷BIOON/ --拜耳(Bayer)近日宣布,美国食品和药物管理局(FDA)已批准了前列腺癌新药Nubeqa(darolutamide,达罗他胺)的一项补充新药申请(sNDA),将关键3期ARAMIS研究试验的总生存期(OS)和其他次要终点数据添加到Nubeqa的处方信息中。
数据显示,在非转移性去势抵抗性前列腺癌(nmCRPC)患者中,与安慰剂相比,Nubeqa将死亡风险显著降低31%、延长了患者的生存期。其他数据包括疼痛进展时间和启动细胞毒化疗时间。处方信息中也纳入了包括药物相互作用的额外指导。对整个研究人群进行的中位29个月的延长随访的最终分析加强了Nubeqa的安全性。
Nubeqa由拜耳与芬兰制药公司Orion合作开发,已在美国、欧盟及其他多个国家获得批准,用于治疗nmCRPC男性患者。该药是一种口服非甾体雄激素受体(AR)抑制剂,具有独特的化学结构,以高亲和力结合受体,表现出强烈的拮抗活性,从而抑制受体功能和前列腺癌细胞的生长。与其他现有的nmCRPC治疗方法不同,Nubeqa不跨越血脑屏障,因此潜在的药物相互作用以及中枢神经副作用(如癫痫、跌倒和认知障碍)更少。
拜耳制药部门高级副总裁兼肿瘤开发主管Scott Z.Fields医学博士表示:“癌症治疗的一个关键目标是延长患者生命,同时尽量减少副作用。Nubeqa对nmCRPC男性患者具有经证实的疗效和安全性,并在通常无症状男性患者中延缓了疾病进展的影响。此次处方信息更新也让医生们更加确信,在nmCRPC诊断时,应将Nubeqa处方给合适的患者,以帮助确保这些患者获得最佳治疗结果。”

ARAMIS是一项随机、多中心、双盲、安慰剂对照III期试验,共入组了1509例nmCRPC男性患者,这些患者正在接受雄激素剥夺疗法(ADT)治疗,并且具有发生转移性疾病的高风险。研究评估了口服Nubeqa与安慰剂的疗效和安全性。该研究中,患者以2:1的比例随机分配,接受每日两次口服600毫克Nubeqa或安慰剂,同时接受ADT。研究中允许有癫痫病史的患者参与治疗。
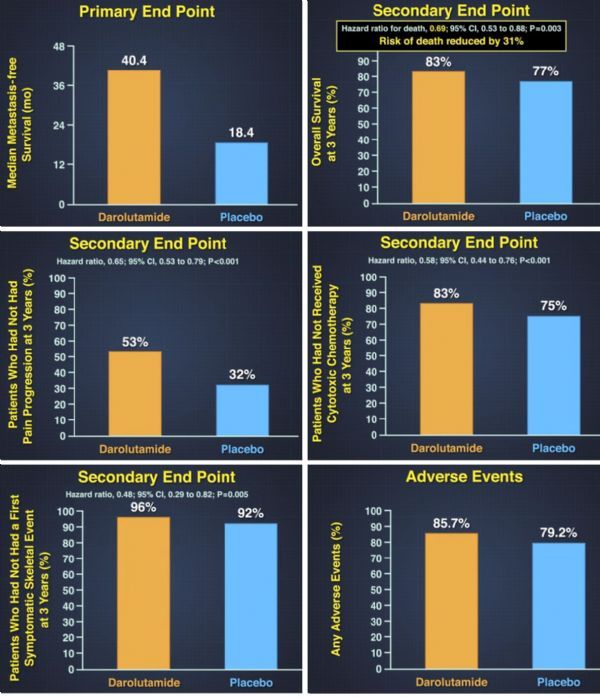
此前公布的主要疗效终点数据显示:与安慰剂+ADT相比,Nubeqa+ADT方案显著延长了无转移生存期(中位MFS:40.4个月 vs 18.4个月,p<0.0001)、将疾病转移或死亡风险显著降低了59%。然而,在进行最终MFS分析时,总生存期(OS)数据尚不成熟。
该研究的最终OS分析的完整结果已于2020年9月发表于《新英格兰医学杂志》(NEJM)。结果显示,与安慰剂相比,Nubeqa显著延长了OS、显著延缓了癌症相关症状的出现时间,同时将毒性降至最低。(详见:Nonmetastatic, Castration-Resistant Prostate Cancer and Survival with Darolutamide)
具体数据为:与安慰剂+ADT相比,Nubeqa+ADT方案将死亡风险显著降低了31%(HR=0.69;95%CI:0.53-0.88;p=0.003),同时显著延迟了疼痛进展时间(HR=0.65,95%CI:0.53-0.79;p<0.0001)、开始首次细胞毒化疗的时间(HR=0.58,95%CI:0.44-0.76;p<0.0001)、首次症状性骨骼事件(SSE)发生时间,所有这些次要终点均具有统计学意义的显著改善。
值得一提的是,尽管安慰剂+ADT治疗组中有超过一半(55%,554例患者中的307例)的患者在最终分析截止日期(2019年11月15日)之前已转向Nubeqa(31%,170例)或另一种延长生命的疗法治疗,但同样观察到了统计学上显著的OS获益。
对整个研究人群进行了中位29个月的扩展随访,Nubeqa继续显示出良好的安全性。与早期分析相比,因不良反应(AE)而中止治疗的情况没有变化,两组患者均有9%发生这种情况。
这项对ARAMIS研究的最新分析也证实了Nubeqa联合ADT对中枢神经系统(CNS)的影响小,发生精神和认知障碍的可能性低。Nubeqa在临床前研究和健康人中观察到的低血脑屏障透过率可以解释这一现象。
前列腺癌(图片来源:hopkinsmedicine.org).png
在全球范围内,前列腺癌是男性中第二大常见恶性肿瘤和第五大癌症死亡原因,主要影响50岁以上的男性,并且随着年龄的增长,风险增加。去势抵抗性前列腺癌(CRPC)是指接受ADT治疗当体内睾酮降至非常低水平时病情仍继续发展的前列腺癌。大约三分之一的非转移(nmCRPC)患者在两年内发生转移,因此,在这种情况下,治疗的首要目标是延迟前列腺癌的转移和扩散,并限制治疗的副作用。
由于患有nmCRPC的男性通常没有任何症状,并且过着积极的生活,因此拥有一些既能延缓癌症进展又能将治疗副作用降到最低的治疗方案非常重要,这将能使他们在几乎没有干扰的情况下维持自己的生活方式。
Nubeqa将为nmCRPC男性患者群体提供一种可显著延长无转移生存期(MFS)和总生存期(OS)的重要治疗选择,该药具有良好的长期安全性,有助于患者持续接受治疗,并实现治疗目标。
除了nmCRPC之外,拜耳和Orion公司也正在推进另一项III期临床研究ARASENS,评估darolutamide治疗转移性激素敏感性前列腺癌(mHSPC)的疗效和安全性。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->