同种异体树突细胞疗法!美国FDA授予ilixadencel再生医学先进疗法(RMAT),治疗肾癌疗效强劲!
来源:本站原创 2020-05-11 16:54
ilixadencel是一种通用型免疫触发剂,将来源于健康献血者的树突状细胞(DC)进行特别激活,可产生大量强有力的免疫刺激因子。
2020年05月11日讯 /生物谷BIOON/ --Immunicum AB是一家致力于开发同种异体、即用型细胞疗法的瑞典生物技术公司,已建立了一种独特的免疫肿瘤学方法,通过发动患者自身的免疫系统对抗癌症,来提高患者生存和改善生活质量。
近日,该公司宣布,美国食品和药物管理局(FDA)已授予其先导候选药物ilixadencel治疗转移性肾细胞癌(mRCC)的再生医学先进疗法(RMAT)资格。ilixadencel是一种同种异体树突状细胞(DC)疗法,目前正被开发为一种通用型(off-the-shelf)癌症免疫触发剂(cancer immune primer),用于多种实体瘤的治疗。
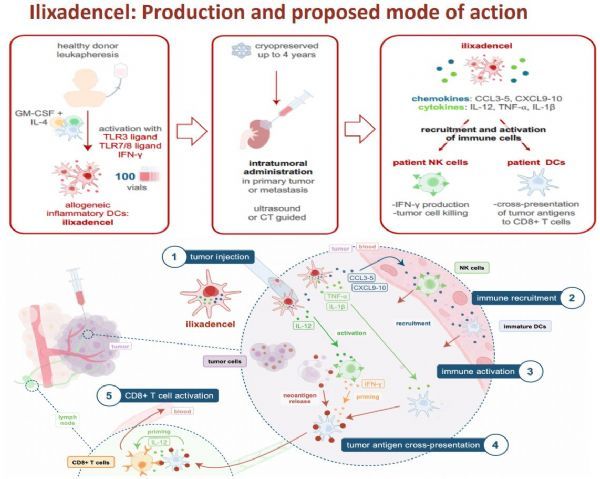
ilixadencel的活性成分是来源于健康献血者的树突状细胞(DC),这些细胞被特别激活,可产生大量强有力的免疫刺激因子。通过肿瘤内注射给药后,这些细胞会引起局部炎症反应,招募和活化患者自身的DC细胞和自然杀伤细胞(NK)进入肿瘤环境中,破坏肿瘤细胞,释放出全套的肿瘤特异性蛋白——新抗原(neoantigen)。这些新抗原将作为抗原来源,导致患者细胞毒T细胞的肿瘤特异性激活,特别是细胞毒性CD8+T细胞,从而产生一种高度个体化的、强效的抗肿瘤反应。
再生医学先进疗法(RMAT)是2016年12月美国修改“21世纪治愈法案(21st Century Cures Act)”的再生医疗条款时,为了加速创新再生疗法的开发和审批而制定的一种Fast track(快速通道)制度。RMAT可以是细胞疗法、治疗性组织工程产品、人类细胞及组织制品,或是其他包含了再生医学技术制品的联合疗法。
在研药物要获得RMAT资格认定,必须要有初步的临床研究数据证明药物在治疗、延缓、逆转或治愈严重或危及生命的疾病或是在未满足医疗需求方具有积极的结果。RMAT资格认定包括了快速通道资格(FTD)和突破性药物资格(BTD)的全部优惠政策,包括与FDA进行早期互动、优先审查、加速审批的可能性。
ilixadencel的制备及作用机制(点击图片查看大图)
此次FDA授予ilixadencel RMAT,基于先前公布的II期MERECA临床试验的结果。该试验评估了ilixadencel联合靶向抗癌药索坦(Sutent,通用名:sunitinib,舒尼替尼;辉瑞研制)一线治疗新诊转移性肾细胞癌(mRCC)患者的疗效和安全性。该试验的最新结果于今年2月在美国佛罗里达州奥兰多市举行的2020年ASCO-SITC临床免疫肿瘤学研讨会上公布。(点击查看:A randomized phase II study with ilixadencel, a cell-based immune primer, plus sunitinib versus sunitinib alone in synchronous metastatic renal cell carcinoma)
结果显示,与术后舒尼替尼治疗相比,术前瘤内注射ilixadencel联合术后舒尼替尼治疗:存活率提高(54% vs 37%)、确认的总缓解率(ORR)提高一倍(42.4% vs 24.0%)、完全缓解率更高(CR:6.7% vs 0%)、缓解更加持久(中位缓解持续时间[DOR]:7.1个月 vs 2.9个月)。目前,两组总生存期(OS)数据尚不成熟。
这些最新结果,进一步支持了ilixadencel作为一种免疫触发剂在肾细胞癌(RCC)和其他实体肿瘤适应症中的持续临床开发潜力。
Immunicum首席执行官Alex Karlsson Parra表示:“我们非常兴奋地收到了ilixadencel治疗肾细胞癌的RMAT资格认定,因为它既认可了我们这款新颖治疗方法的潜力,也强调了采用可行的治疗方法来解决这一难治性疾病的明确需求。作为一个类似于FDA突破性药物资格的资格认定,我们现在也有机会从FDA获得直接指导,这将为关键的开发决策提供信息,并最终使我们更接近于向有需要的患者交付ilixadencel。”
MERECA是一项探索性、国际性、随机、对照、开放标签研究,共入组了88例新诊断的、中危和高危mRCC患者。研究中,患者以2:1的比例随机分组,一组在肾切除术前接受2次瘤内ilixadencel给药并随后在肾切除术后接受舒尼替尼治疗,另一组仅在肾切除术后接受舒尼替尼。研究的主要目标是评估总生存期(OS)和18个月生存率。次要目标是评估安全性和耐受性、肿瘤反应和免疫分析,包括T细胞浸润。
2019年7月公布的结果(涉及70例可评估患者)显示:一线治疗中高危mRCC患者时,与肾切除术后服用舒尼替尼相比,术前瘤内注射ilixadencel和术后服用舒尼替尼联合方案大幅提高了肿瘤完全缓解率(11% vs 4%),2个治疗组中位OS均未达到,18个月生存率相似,ilixadencel治疗组为65%,舒尼替尼对照组为66%。
此次会上公布的截至2019年12月的最新数据显示:Kaplan-Meier生存曲线的分离有利于ilixadencel治疗组,并与2019年7月的预测分离一致。ilixadencel治疗组存活率为54%(30/56)、对照组为37%(11/30)。由于数据尚不成熟,两组OS中位数尚无法计算。Immunicum AB根据最佳总体反应和反应持续时间的数据,要求合同研究机构对确认的总缓解率(ORR,根据RECIST 1.1标准,通过后续扫描确认的肿瘤反应)进行的研究后分析显示:ilixadencel治疗组确认的ORR为42.2%(19/45),是舒尼替尼对照组(24.0%,6/25)的近2倍。
MERECA研究的首席调查员、瑞典乌普萨拉大学医院临床肿瘤学家、副教授Magnus Lindskog表示:“最新的数据强调,与单独使用舒尼替尼相比,ilixadencel和舒尼替尼联合治疗方案的肿瘤反应和患者反应的持久性更好。ilixadencel的加入并没有增加副作用的发生率和严重程度。目前该研究将还需要更长的随访,以确定长期生存率的差异。”(生物谷Bioon.com)
原文出处:Immunicum AB (publ) Receives Regenerative Medicine Advanced Therapy Designation from FDA for Ilixadencel in Kidney Cancer
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->