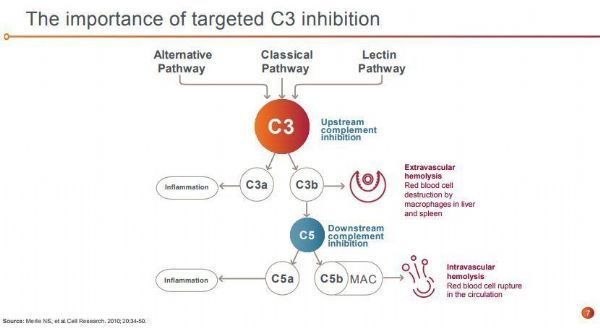
C3抑制剂!欧盟批准Aspaveli:治疗阵发性睡眠性血红蛋白尿症(PNH),疗效优于C5抑制剂!
来源:本站原创 2021-12-17 00:55
Aspaveli(pegcetacoplan)疗效击败重磅C5抑制剂Soliris,将成为PNH新的护理标准!
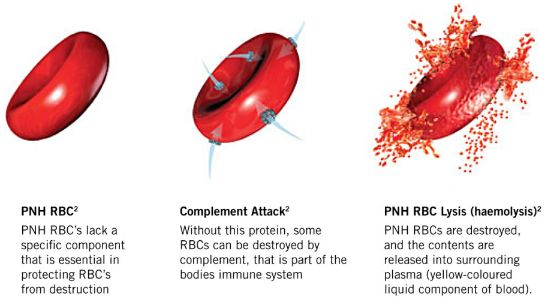
PNH红细胞溶血(图片来源:standardofcare.com)
2021年12月15日讯 /生物谷BIOON/ --Apellis制药公司与瑞典罕见病药商Swedish Orphan Biovitrum AB(Sobi)近日联合宣布,欧盟委员会(EC)已批准Aspaveli(pegcetacoplan),用于治疗接受C5抑制剂至少3个月后贫血的阵发性睡眠性血红蛋白尿症(PNH)成人患者。2021年5月,该药率先在美国获得批准,商品名为Empaveli,可用于先前没有接受过治疗的PNH成人患者,也可用于从C5抑制剂(Soliris和Ultomiris)转换治疗的PNH成人患者。pegcetacoplan的批准上市,有望提升PNH护理标准,重新定义PNH的治疗。
值得一提的是,pegcetacoplan是获得监管批准的第一个也是唯一一个C3靶向疗法。在过去十多年来,治疗PNH的唯一选择是C5抑制剂,但许多患者仍然经历持续性低血红蛋白症,常常导致虚弱的疲劳和频繁的输血。在临床试验中,pegcetacoplan能针对PNH提供广泛的控制,通过增加血红蛋白水平及减少输血需求来改善PNH患者的生活。
pegcetacoplan在美国和欧盟获得监管批准,均基于头对头3期PEGASUS研究(NCT03500549)的结果(详见:PEGASUS Phase 3 Top-Line Results Conference Call Presentation)。该研究达到了主要终点,证明pegcetacoplan优于PNH标准护理药物Soliris:在第16周时血红蛋白水平较基线水平的变化方面优于Soliris,调整后的血红蛋白水平平均增加3.84g/dL(p<0.0001)。
此外,pegcetacoplan与Soliris相比在避免输血终点方面达到了非劣效性。pegcetacoplan治疗组有85%的患者在16周内没有输血,而Soliris治疗组为15%。同时,与Soliris治疗组患者相比,pegcetacoplan治疗组患者的溶血关键标志物正常化率更高,FACIT-疲劳评分具有临床意义的改善。在该研究中,pegcetacoplan的安全性与Soliris相当。
pegcetacoplan作用机制(点击图片,查看大图)
pegcetacoplan是第一个在血红蛋白水平上显示出优于Soliris的疗法,高达85%接受pegcetacoplan治疗的患者没有输血。而目前接受Soliris治疗的PNH患者中,大多数都患有持续性贫血。PEGASUS研究的结果显示,pegcetacoplan有潜力成为PNH患者的新护理标准。
pegcetacoplan是一种靶向C3抑制剂,旨在调节补体过度激活,这是导致许多严重疾病发生和发展的原因。pegcetacoplan是一种合成的环肽,与一种聚乙二醇聚合物结合,特异性地与C3和C3b结合。目前,pegcetacoplan正被开发用于治疗多种疾病,包括PNH、地图样萎缩(GA)和C3肾小球病。在美国,FDA已授予pegcetacoplan治疗PNH和GA的快速通道资格。
目前,尚无治疗GA的药物。Apellis公司计划在2022年提交玻璃体腔注射pegcetacoplan治疗年龄相关性黄斑变性(AMD)继发性GA的新药申请。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->