溃疡性结肠炎(UC)新药!吉利德/Galapagos口服JAK1抑制剂Jyseleca:快速改善症状、持久缓解!
来源:本站原创 2021-07-13 03:13
Jyseleca已在欧盟和日本被批准治疗类风湿性关节炎(RA)。
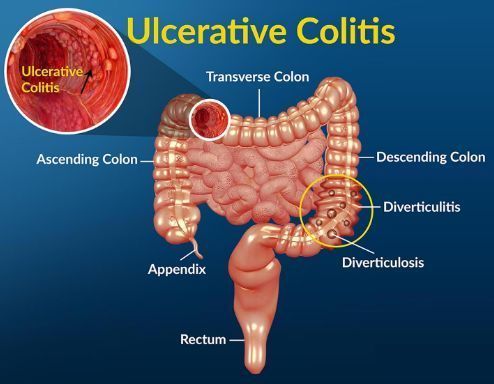
溃疡性结肠炎(UC,图片来源:healthjade.com)
2021年07月12日讯 /生物谷BIOON/ --吉利德科学(Gilead Sciences)合作伙伴Galapagos NV近日在欧洲克罗恩病和结肠炎组织(ECCO)第16届年会上公布了口服抗炎药Jyseleca(filgotinib,200mg)3期SELECTION项目新的事后分析结果。会上公布的数据,支持了Jyseleca作为一种每日口服一次的JAK1优先抑制剂,在治疗中重度活动性溃疡性结肠炎(UC)患者方面的疗效和安全性。
Jyseleca是一种口服选择性JAK1抑制剂,已在欧盟、英国、日本获批上市,用于治疗对一种或多种疾病修饰抗风湿药物(DMARD)应答不足或不耐受的中度至重度类风湿性关节炎(RA)成人患者。用药方面,Jyseleca可作为单药疗法,或与甲氨蝶呤(MTX)联合使用。目前,Jyseleca治疗UC的新适应症申请也正在接受欧盟、英国、日本的监管审查,具体申请为:用于治疗对常规疗法或生物制剂应答不足、失应答、或不耐受的中度至重度活动性溃疡性结肠炎(UC)成人患者。值得注意的是,因为安全性的考虑,美国FDA尚未批准Jyseleca任何适应症。

此次会上,对SELECTION项目诱导研究数据进行的事后分析表明,在中度至重度活动性UC患者中,与安慰剂相比,filgotinib(每日口服一次,200mg)显著改善了排便频率(SF)和直肠出血(RB),该疗效在治疗的第一周就观察到了,并且在生物制剂初治(biologic-naive,先前没有接受过生物制剂)和生物制剂经治(biologic-experienced,先前接受过生物制剂)患者中均观察到。
与安慰剂相比,接受200mg filgotinib治疗的患者中,有更高比例的患者:在诱导研究A中早在第9天就达到综合评定为RB=0和SF≤1(生物制剂初治:filgotinib 200mg组18.8%,安慰剂组9.5%,p<0.05)、在诱导研究B中早在第7天就达到综合评定为RB=0和SF≤1(生物制剂经治;filgotinib 200mg组10.7%;安慰剂组4.2%,p<0.05)。
对SELECTION维持研究的进一步事后分析,报告了在不同时间点无类固醇缓解的患者比例。这些数据表明,在中度至重度活动性UC患者中,与安慰剂相比,filgotinib(每日口服一次,200mg)在第58周减少和消除了皮质类固醇(CS)的使用。在第58周显示无CS缓解的患者中,与安慰剂组相比,filgotinib 200mg组有显著更高比例的患者在前6个月一直处于无CS缓解(27% vs 6%),差异早在前8个月就观察到(fingolimod 200mg组 22% vs 安慰剂组6%)。
来自SELECTION项目的额外安全性分析,合并诱导、维持、长期扩展研究数据(filgotinib 200mg的累积治疗暴露为1207患者年,安慰剂累积治疗暴露为318患者年),安全性结果与最初的诱导和维持研究一致,filgotinib在中度至重度活动期UC患者中耐受性良好。
Galapagos首席医疗官Walid Abi Saab表示:“倾听中度和重度活动性UC患者及治疗他们的医疗专业人员的需求,有助于我们理解找到可同时解决临床症状和患者报告结果的治疗方法的重要性。来自SELECTION和长期扩展研究的新数据表明,与接受安慰剂的患者相比,接受filgotinib 200mg治疗的中度至重度活动性UC患者经历了快速反应、持续的无类固醇缓解、长期的耐受。”
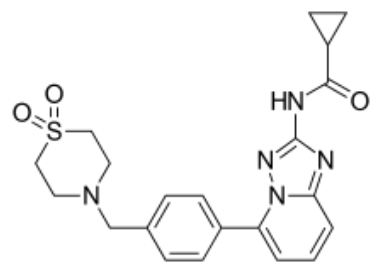
filgotinib分子结构式(图片来源:Wikipedia)
溃疡性结肠炎(UC)是一种慢性炎症性肠病(IBD),该病症状往往是间歇性的,因此患者通常会经历发作期和缓解期。除了对身体造成的影响外,该病还会带来显著的心理影响。
Jyseleca的活性药物成分为filgotinib,这是一种高度选择性JAK1抑制剂,由Galapagos发现和开发。吉利德于2015年12月底与Galapagos达成了一项总额高达20亿美元的协议,在全球共同开发和商业化filgotinib。而由于在美国监管方面遭遇的重大挫折,双方在2020年12月修订了filgotinib的商业化及开发协议内容。Galapagos将负责filgotinib在欧洲的商业化(过渡期预计在2021年底完成),而吉利德将继续负责filgotinib在欧洲以外的地区,包括日本(吉利德在该地区与卫材共同销售filgotinib)。
目前,filgotinib正被开发用于治疗多种炎症性疾病,其中3期研究包括治疗类风湿性关节炎、克罗恩病、溃疡性结肠炎。不过,在JAK抑制剂领域,filgotinib也面临着多个竞争产品,除了2款已上市产品辉瑞Xeljanz和礼来Olumiant之外,更强劲的对手将是艾伯维的Rinvoq(upadacitinib)。
值得注意的是,在今年上半年,美国FDA推迟了多款JAK抑制剂的新适应症审查时间表,包括辉瑞abrocitinib(阿布昔替尼)治疗中重度特应性皮炎(AD)、Xeljanz/Xeljanz XR治疗强直性脊柱炎(AS)、Olumiant治疗中重度AD、Rinvoq治疗中重度AD和活动性PsA。
原因是,在今年1月份公布的一项上市后安全性研究中发现,与传统的TNF抑制剂老药相比,Xeljanz会增加严重心脏相关疾病和癌症的风险。目前,美国FDA正在对JAK抑制剂类别的全部药物进行严格审查。该机构已要求相关药企提供额外的分析数据。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


