鼻咽癌免疫治疗!百济神州抗PD-1疗法替雷利珠单抗(百泽安®)+化疗一线治疗3期临床获得成功!
来源:本站原创 2021-05-24 01:11
截至目前,君实生物拓益®(特瑞普利单抗)是全球唯一被批准治疗鼻咽癌的免疫疗法。

2021年05月24日讯 /生物谷BIOON/ --百济神州(BeiGene)近日宣布,经独立数据检测委员会(IDMC)推荐,评估抗PD-1抗体百泽安®(替雷利珠单抗,tislelizumab)治疗鼻咽癌(NPC)的3期RATIONALE 309临床试验(NCT03924986)在中期分析时达到了主要终点。
RATIONALE 309是一项随机、双盲、安慰剂对照的3期临床试验,旨在比较百泽安®联合化疗(吉西他滨和顺铂)、安慰剂联合化疗(吉西他滨和顺铂)一线治疗复发或转移性NPC患者疗效和安全性。 研究主要终点是意向性治疗(ITT)人群中经独立评审委员会(IRC)评估的无进展生存期(PFS);关键次要终点包括总生存期(OS)、经IRC评估的客观缓解率(ORR)和缓解持续时间(DoR),以及经研究者评估的PFS。该试验共入组了263例亚洲患者,这些患者以1:1的比例随机分配,进入百泽安®+化疗组,或安慰剂+化疗组。
中期分析结果显示,该研究已达到了主要终点:在ITT人群中,根据IRC评估,与安慰剂+化疗相比,百泽安®+化疗治疗显示PFS在统计学上有显著改善。该研究中,百泽安®的安全性与已知的风险一致,与化疗联合用药没有发现新的安全性信号。
百济神州计划与多个监管部门讨论这些数据,并在即将召开的医学会议上公布这些数据。
百济神州肿瘤免疫学首席医学官贲勇医学博士表示:“我们非常兴奋在此项3期临床试验中观察到,百泽安®联合化疗能为鼻咽癌患者的无进展生存期带来具有临床意义的改善。这标志着第5项获得积极结果的百泽安®3 期临床试验,我们同时也正在一项广泛的临床项目中对这款潜在差异化的抗PD-1抗体进行评估。我们十分感激参与该试验的患者和临床医护人员,并期待能为他们提供一项新的治疗选择。”
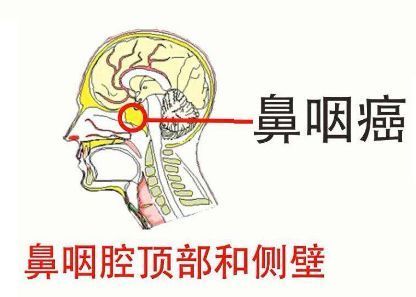
鼻咽癌(图片来源:百度百科)
鼻咽癌(NPC)是一种恶性鳞状细胞癌,起源于鼻咽的上皮细胞,最常见于咽隐窝。2018年,中国有约60558例新增NPC患者,占全球新发病例的46.9%。尽管NPC对中国南方和其他疾病流行地区的公共卫生造成了沉重负担,但对NPC的病因和预防相对较少。鼻咽癌的主要风险因素是遗传易感性、Epstein-Barr病毒(EBV)感染和食用盐腌食物。晚期NPC患者的中位总生存期约为20个月,然而据报道,复发或转移性NPC患者的预后通常逐渐恶化,3年生存率降至大约为7-40%,表明鼻咽癌亟需更有效的治疗方法。
鼻咽癌免疫治疗方面,截至目前,君实生物抗PD-1抗体拓益®(特瑞普利单抗,toripalimab)是全球唯一被批准用于治疗鼻咽癌的免疫疗法。2021年2月,国家药品监督管理局(NMPA)批准拓益®,用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗,成为全球首个获批鼻咽癌治疗的抗PD-1单抗药物,实现了该领域内免疫治疗零的突破。
2021年3月,君实生物向美国FDA滚动提交了特瑞普利单抗用于治疗复发或转移性鼻咽癌的生物制品许可申请(BLA)。特瑞普利单抗成为首个向美国FDA提交上市申请的国产抗PD-1单抗,有望成为在海外市场最早实现商业化的国产抗PD-1单抗药物。
在鼻咽癌治疗领域,特瑞普利单抗已在临床布局方面实现了从一线至后线的“全线贯穿”,包括覆盖后线患者的POLARIS-02研究和针对一线治疗患者的JUPITER-02(NCT03581786)研究。
JUPITER-02研究是迄今为止全球范围内规模最大的免疫检查点抑制剂联合化疗一线治疗复发或转移性鼻咽癌的III期临床研究。根据期中分析结果,特瑞普利单抗联合吉西他滨/顺铂一线治疗复发或转移性鼻咽癌患者,较吉西他滨/顺铂的标准一线治疗,可显著延长患者的无进展生存期。
基于JUPITER-02研究,君实生物于今年2月向国家药品监督管理局(NMPA)提交了特瑞普利单抗联合化疗用于晚期一线未接受过系统性治疗的复发转移性鼻咽癌的新适应症上市申请并获受理。
百泽安®(替雷利珠单抗)是一款人源化lgG4抗程序性死亡受体1(PD-1)单克隆抗体,设计目的是为最大限度地减少与巨噬细胞中的FcγR受体结合。临床前数据表明,巨噬细胞中的FcγR受体结合之后会激活抗体依赖细胞介导杀伤T细胞,从而降低了PD-1抗体的抗肿瘤活性。替雷利珠单抗是第一款由百济神州的免疫肿瘤生物平台研发的候选药物,目前正进行单药及联合疗法临床试验,开发一系列针对实体瘤和血液肿瘤的广泛适应症。
在中国,NMPA已批准百泽安®联合化疗用于治疗一线晚期鳞状非小细胞肺癌(NSCLC)患者。百泽安®另获附条件批准用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者以及PD-L1高表达的含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌患者。针对上述两项适应症的完全批准将取决于正在进行的确证性随机对照临床试验结果。
此外,NMPA药品审评中心(CDE)已受理百泽安的三项新适应症上市申请且正在审评过程中,包括一项联合化疗用于治疗一线晚期非鳞状NSCLC患者,一项用于治疗既往接受铂类化疗后出现疾病进展的二或三线局部晚期或转移性NSCLC患者,一项用于治疗既往经治的不可切除肝细胞癌患者。
目前共有17项百泽安®的注册性临床试验在中国和全球范围内开展,其中包括13项3期临床试验,4项关键性2期临床试验。
2021 年1月,百济神州与诺华达成合作协议,授权诺华在北美、欧洲和日本开发、制造和商业化百泽安®。百泽安®在中国以外国家地区尚未获批。(生物谷Bioon.com)
原文出处:百济神州、君实生物、生物谷
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


