贫血新药!BMS首创红细胞成熟剂Reblozyl在美欧申请扩大适应症:治疗非输血依赖性β地中海贫血!
来源:本站原创 2021-12-15 01:53
Reblozyl是第一个红细胞成熟剂,代表了一类新的疗法,通过调节红细胞成熟后期阶段来帮助患者减少红细胞输注负担。
β地中海贫血(图片来源:glowydowy.com)
2021年12月14日讯 /生物谷BIOON/ --百时美施贵宝(BMS)近日宣布,美国食品和药物管理局(FDA)已受理Reblozyl(luspatercept-aamt)的补充生物制品许可申请(sBLA)并授予了优先审查:该药是一款首创(first-in-class)红细胞成熟剂(EMA),用于非输血依赖型(NTD)β地中海贫血(β-thalassemia)成人患者,治疗贫血。FDA已将该sBLA的《处方药用户收费法(PDUFA)》目标日期定为2022年3月27日。此外,欧洲药品管理局(EMA)已受理Reblozyl用于NTDβ地中海贫血成人患者治疗贫血的II类变更申请。
NTD β地中海贫血是一个术语,用于描述不需要终生定期输注红细胞(RBC)以维持生存的患者,尽管他们可能需要偶尔或稍频繁输注,通常是在规定的时间段内。NTD β地中海贫血患者会经历慢性贫血和铁过载,这可能导致一系列的临床并发症,迫切需要治疗方案。临床试验数据显示,在NTD β地中海贫血成人患者中,无论基线血红蛋白水平如何,Reblozyl均能够提高患者血红蛋白水平,同时改善了患者生活质量。
Reblozyl原本由BMS与Acceleron制药公司合作开发,在默沙东最近完成115亿美元收购Acceleron之后,Reblozyl现在由BMS与默沙东共同开发和商业化。Reblozyl是获得监管批准的第一个用于治疗β-地中海贫血、极低/低/中危骨髓增生异常综合征(MSD)相关贫血的红细胞成熟剂(EMA)。在符合资格的患者群体中,Reblozyl代表了一个重要的治疗类别。需要指出的是,在需要立即纠正贫血的患者中,Reblozyl不适用于作为红细胞输注的替代品。
Reblozyl的活性药物成分为luspatercept,这是一种首创的(first-in-class)红细胞成熟剂(EMA),可调节晚期红细胞的成熟。luspatercept是一种可溶性融合蛋白,由人IgG1的Fc结构域与激活素IIB型受体(ActRIIB)胞外结构域融合而成,作为一种配体陷阱,通过靶向结合可调节晚期RBC成熟的转化生长因子(TGF)-β超家族的特定配体,减少Smad2/3信号通路的激活,改善无效RBC的生成,促进晚期RBC红细胞的成熟,提高血红蛋白水平。
Reblozyl sBLA和II类变更申请,基于关键2期BEYOND研究的安全性和疗效结果。该研究在NTD β地中海贫血成人患者中开展,评估了Reblozyl联合最佳支持护理(BSC)。2021年6月公布的数据显示,Reblozyl+BSC治疗组有77.1%的患者实现血红蛋白水平升高(≥1.0g/dL),而安慰剂+BSC组为0%。此外,与安慰剂组相比,Reblozyl组的患者报告结果也表现出改善。
百时美施贵宝血液学开发高级副总裁Noah Berkowitz博士表示:“非输血依赖型β地中海贫血患者可能不需要终生输血来维持生存,但需要有效的治疗方案,因为他们面临一系列慢性贫血和铁超载引起的临床并发症。Reblozyl是多个国家(包括美国和欧盟)批准用于治疗与β地中海贫血和低风险骨髓增生异常综合征相关贫血的一种重要疗法。我们与默沙东致力于继续推进Reblozyl临床项目,并期待着在审查过程中与FDA密切合作和沟通,为这一服务不足的患者群体带来一种新的治疗选择。”
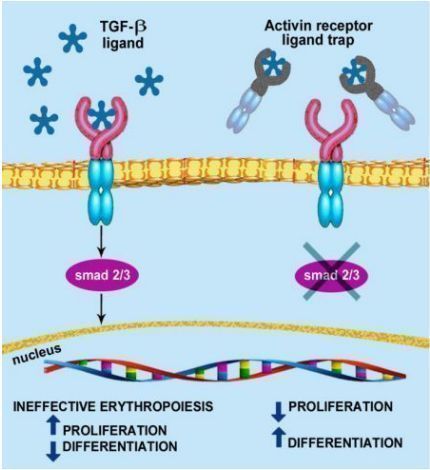
luspatercept作用机制
BEYOND是一项随机、双盲、安慰剂对照、多中心2期研究,在非输血依赖性(NTD)β地中海贫血成人患者中开展,旨在评估Reblozyl相对于安慰剂的疗效和安全性。入组患者为:年龄≥18岁、患有β地中海贫血或血红蛋白(Hb)E β地中海贫血、在随机分组前24周内输注了≤5个红细胞(RBC)单位,平均基线Hb≤10.0克/分升(g/dL)。
研究中,145例患者以2:1的比例被随机分组,接受每3周一次皮下注射Reblozyl(1mg/kg[滴定至1.25mg/kg])或安慰剂,治疗持续≥48周。2组患者继续接受最佳支持护理(BSC),包括RBC输注和铁螯合剂治疗。主要终点是:从第13-24周开始的连续12周内,在没有输注RBC的情况下,平均血红蛋白从基线水平增加1.0 g/dL。次要终点包括:第1-24周内保持无输注的患者比例、血红蛋白水平从基线至第13-24周平均增加≥1.5 g/dL的患者比例、NTD β地中海贫血患者报告结果疲劳和虚弱(NTDT-PRO T/W)评分的平均变化(得分越高反映生活质量[QoL]越差)。
主要终点结果显示:Reblozyl治疗组有77.1%(n=74/96)的患者达到主要终点,安慰剂组为0%(n=0/49),数据具有统计学显著差异(p<0.0001)。在平均基线Hb<8.5g/dL的患者中,Reblozyl治疗组有72.7%(n=40/55)的患者达到主要终点,安慰剂组为0%(p<0.0001);在平均基线Hb≥8.5g/dL的患者中,Reblozyl治疗组有82.9%(n=34/41)的患者达到主要终点,安慰剂组为0%(p<0.0001)。
关键次要终点方面:(1)Reblozyl治疗组有52.1%(n=50/96)的患者实现第13-24周期间平均Hb水平较基线增加≥1.5g/dL,安慰剂组为0%(p<0.0001)。(2)在第1-24周,Reblozyl治疗组有89.6%的患者保持无输注,安慰剂组为67.3%(p=0.0013)。(3)患者报告的生活质量结果(疲劳和虚弱)的改善也与血红蛋白增加相关。
安全性方面,发生在≥5%患者中的任何级别最常见治疗期间出现的不良事件(TEAE)为骨痛(Reblozyl组 vs 安慰剂组:36.5% vs 6.1%)、头痛(30.2% vs 20.4%)和关节痛(29.2% vs 14.3%)。在接受Reblozyl治疗的患者中,没有报告恶性肿瘤或血栓栓塞事件。
BEYOND研究的最新分析将在12月11日至14日举行的第63届美国血液学会(ASH)年会和博览会上公布。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


