CAR-T细胞疗法研究进展(第32期)
来源:生物谷原创 2022-09-30 03:27
近年来,CAR-T免疫疗法除了被用来治疗急性白血病和非霍奇金淋巴瘤之外,经改进后,也被用来治疗实体瘤、自身免疫疾病、HIV感染和心脏病等疾病,具有更广阔的应用空间。
CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被 认为是最有前景的肿瘤治疗方式之一。正如所有的技术一样,CAR-T技术也经历一个漫长的演化过程,正是在这一系列的演化过程中,CAR-T技术逐渐走向成熟。
这种新的治疗策略的关键之处在于识别靶细胞的被称作嵌合抗原受体(chimeric antigen receptor, CAR)的人工受体,而且在经过基因修饰后,病人T细胞能够表达这种CAR。在人体临床试验中,科学家们通过一种类似透析的过程提取出病人体内的一些T细胞,然后在实 验室对它们进行基因修饰,将编码这种CAR的基因导入,这样这些T细胞就能够表达这种新的受体。这些经过基因修饰的T细胞在实验室进行增殖,随后将它们灌注回病人体内。这些T细胞利用它们表达的CAR受体结合到靶细胞表面上的分子,而这种结合触发一种内部信号产 生,接着这种内部信号如此强效地激活这些T细胞以至于它们快速地摧毁靶细胞。
近年来,CAR-T免疫疗法除了被用来治疗急性白血病和非霍奇金淋巴瘤之外,经改进后,也被用来治疗实体瘤、自身免疫疾病、HIV感染和心脏病等疾病,具有更广阔的应用空间。基于此,针对CAR-T 细胞疗法取得的最新进展,小编进行一番盘点,以飨读者。
1.Nature:重大进展!我国科学家开发出非病毒的基因特异性靶向CAR-T细胞,并在临床试验中证实它们可安全有效地治疗复发/难治性B细胞非霍奇金淋巴瘤
doi:10.1038/s41586-022-05140-y
近年来,嵌合抗原受体(CAR)T细胞(CAR-T)疗法迅速发展,它在癌症治疗中显示出巨大的潜力。然而,一些局限性仍然存在,包括目前的CAR-T细胞疗法的复杂制造过程、高生产成本、较长的制备时间和潜在的安全问题。在CAR-T细胞生产中使用病毒是一个令人担忧的领域,因为这种方法的缺点包括插入突变导致的肿瘤产生风险增加。此外,对病毒DNA的特异性反应往往会阻碍CAR的表达,而且病毒制备本身经常会产生高额费用。尽管一些不使用病毒的策略,如使用转座子系统和mRNA转导,正在用来产生CAR-T细胞,但随机整合和CAR表达中断导致的CAR-T细胞同质性较低成为额外的问题。近期,一些研究表明,通过使用腺相关病毒(AAV)载体作为模板,可以应用基因组编辑技术来产生基因座特异性整合的CAR-T细胞。此外,有人提出了一种优选的非病毒策略,以产生可校正点突变和精确插入T细胞受体(TCR)的T细胞产品。
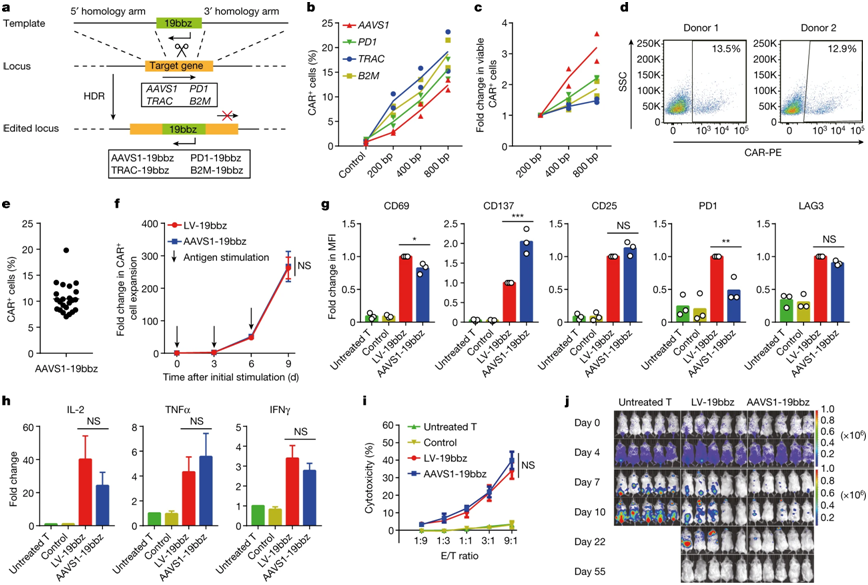
非病毒的将CAR整合到AAVS1基因中的CAR-T细胞有效消除肿瘤细胞。图片来自Nature, 2022, doi:10.1038/s41586-022-05140-y。
为了同时解决病毒使用和随机整合的缺点,来自中国浙江大学和华东师范大学等研究机构的研究人员利用CRISPR-Cas9开发出非病毒的、基因特异性靶向CAR-T细胞,并一项1期开放标签的单臂临床试验中证实它们在治疗8名复发/难治性B细胞非霍奇金淋巴瘤(relapsed/refractory B cell non-Hodgkin lymphoma, r/r B-NHL)患者中的高安全性和有效性。相关研究结果近期发表在Nature期刊上,论文标题为“Non-viral, specifically targeted CAR-T cells achieve high safety and efficacy in B-NHL”。
据这些作者的说法,他们是世界上首次在临床试验中证实非病毒的、基因特异性靶向CAR-T细胞的安全性和有效性的。通过使用非病毒的、将靶向CD19的CAR整合到PD1基因中的CAR-T细胞(PD1-19bbz CAR-T细胞),他们发现接受这些CAR-T细胞治疗的r/r B-NHL患者具有显著的安全性,只有较低的轻度细胞因子释放综合征(CRS)发生率,并且没有发生神经系统毒性。他们的临床前实验也表明不论肿瘤细胞是否较高地表达PD-L1,PD1-19bbz CAR-T细胞都能高效地清除它们。这些研究结果也与之前报道的两项临床试验一致,因而进一步证实了CRISPR-Cas9应用于T细胞治疗的安全性。与此同时,他们观察到较高的完全缓解率和持久的完全缓解。特别是在两名PD-L1高表达的r/r B-NHL患者中发现了反应(尽管后来一名患者发生了CD19-肿瘤复发)。令人惊讶的是,尽管初始的PD1-19bbz CAR-T细胞剂量(没公斤体重输注2×106个细胞)出乎意料地低,或者由于早期和仍然不成熟的制造过程导致CAR+细胞的比例很低,但是在12个月的中位观察期间,8名患者中有7人实现了完全缓解,这表明这些PD1-19bbz CAR-T细胞具有更强的杀死肿瘤细胞的效力。
2.Science子刊:利用TCR-T细胞靶向COL6A3蛋白的一种泛癌表位有望治疗一系列实体瘤
doi:10.1126/scitranslmed.abo6135
尽管过继性T细胞疗法被炒得沸沸扬扬,但要找到在不同肿瘤类型中一致性表达但在健康细胞中不表达的治疗靶标仍是一个挑战。如今,在一项新的研究中,来自美国宾夕法尼亚大学和德国Immatics生物技术公司(下称Immatics公司)的研究人员确定了一种泛癌抗原成分:COL6A3-FLNV,可以满足这两个条件。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题为“Quantitative immunopeptidomics reveals a tumor stroma–specific target for T cell therapy”。
在这项新的研究中,这些作者指出利用T细胞受体(TCR)T细胞(TCR-T)疗法靶向他们发现的一种泛癌抗原成分时,可以减缓小鼠的癌症生长。这种泛癌抗原成分在11种不同类型的实体瘤患者的肿瘤样本中大量存在,但在健康细胞中却很少存在,这使它成为T细胞疗法的主要潜在靶标。如今,Immatics公司计划向美国食品药品管理局(FDA)申请试验性新药,希望能启动1期临床试验。
有了他们的靶标,这些作者着手开发能够识别该表位而不攻击其他肽的TCR。他们再次利用Immatics发现平台的数据来比较肿瘤细胞和正常细胞之间的反应性,开发出高亲和力的TCR-T细胞,并将它们注射到接受人类白血病细胞移植的小鼠体内。癌症的生长速度减慢了,而且小鼠也没有出现严重的副作用。
3.Nat Med:新研究揭示了大B细胞淋巴瘤患者对CAR-T细胞有反应的标志物
doi:10.1038/s41591-022-01959-0
在过去的五年里,对血癌的治疗得到了极大的改善,这要归功于一种叫做CAR-T细胞疗法的新型癌症免疫疗法。这种疗法涉及在实验室中重编程从患者体内提取出的T细胞来杀死癌细胞,然后将它们输注回给患者体内,可治愈大约40%的原本无法治愈的淋巴瘤患者。但也有人出现癌症复发或对这种治疗完全没有反应。
为了了解这种不同反应的分子机制,在一项的研究中,来自美国布罗德研究所、丹娜法伯癌症研究院和麻省总医院的研究人员研究了接受CAR-T细胞疗法的患者的血液样本。他们发现了表明患者对这种治疗作出反应的分子标志物,还确定了可能导致癌症复发的特定类型的免疫细胞。这些研究结果有一天可能帮助医生为他们的病人选择最好的治疗方法,并帮助科学家们优化这些疗法以提高反应率。相关研究结果于2022年9月12日在线发表在Nature Medicine期刊上,论文标题为“Distinct cellular dynamics associated with response to CAR-T therapy for refractory B cell lymphoma”。
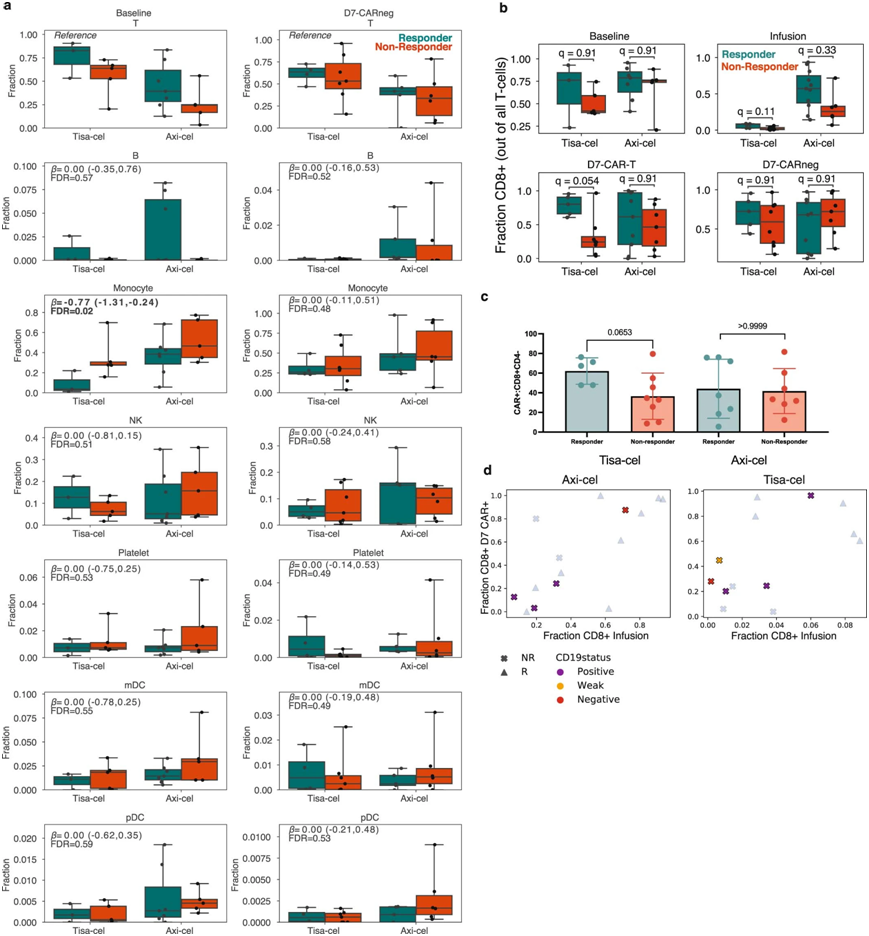
CAR-T细胞灌注前后有反应者和无有反应者之间的外周血单核细胞组成差异。图片来自Nature Medicine, 2022, doi:10.1038/s41591-022-01959-0。
在这项新的研究中,这些作者比较了接受不同CAR-T细胞疗法--- axi-cel和tisa-cel---治疗的大B细胞淋巴瘤的患者的血液样本,以及这些疗法本身。这两种CAR-T细胞疗法是美国食品药品管理局(FDA)在2017年和2018年批准的第一批CAR-T细胞疗法。它们都靶向癌细胞表面的CD19蛋白,在临床上有类似的成功率。
这些作者利用单细胞RNA测序技术,研究了这些疗法中的CAR-T细胞如何随时间变化,时间跨度为从输注到患者血液中之前到治疗后一周。他们发现,这些细胞具有令人惊讶的不同特征。在tisa-cel治疗后,患者血液中的大多数CAR-T细胞来自于一种特殊的T细胞,它有助于免疫系统对特定抗原的记忆。与那些没有反应的患者相比,这些T细胞在对该疗法反应良好的患者中也更为丰富。axi-cel治疗导致了更多T细胞类型的混合。
4.Cell Metab:抑制胞啃作用可提高内源性T细胞和CAR-T细胞的抗肿瘤活性,阻止癌细胞逃避免疫检测
doi:10.1016/j.cmet.2022.08.007
免疫系统不仅要对诸如病毒、细菌和寄生虫之类的外部入侵者,而且要对诸如癌症之类的内部威胁做出反应。然而,恶性肿瘤经常克服免疫系统的防御措施,并逃避免疫检测。在一项新的研究中,来自美国宾夕法尼亚大学等研究机构的研究人员发现了一种详细的机制,利用该机制肿瘤可以避开免疫系统和利用其力量的癌症疗法,如经过基因改造的CAR-T细胞。相关研究结果发表在2022年9月6日的Cell Metabolism期刊上,论文标题为“ATF3 and CH25H regulate effector trogocytosis and anti-tumor activities of endogenous and immunotherapeutic cytotoxic T lymphocytes”。
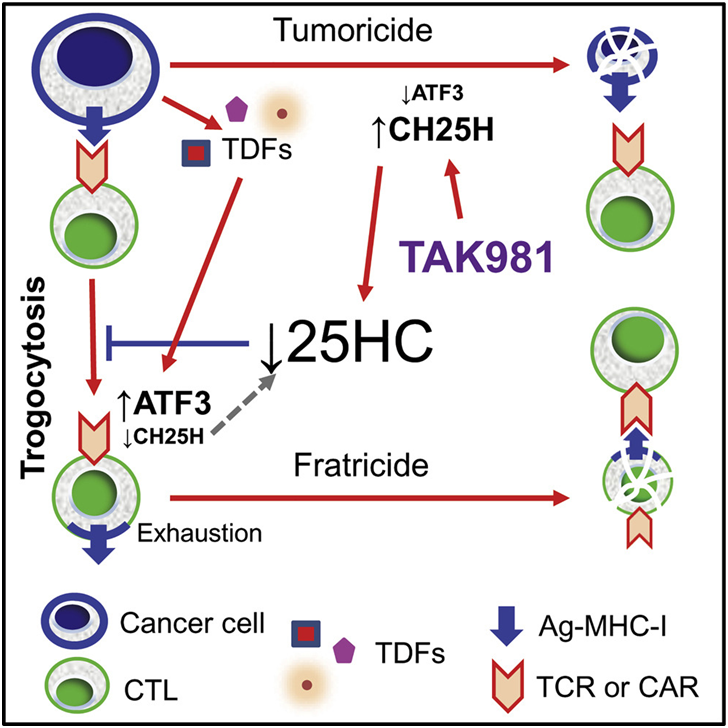
图片来自Cell Metabolism, 2022, doi:10.1016/j.cmet.2022.08.007。
这些作者揭示了肿瘤源性因子如何刺激胞啃作用(trogocytosis)。当T细胞与癌细胞相互作用时,它们有时可以“啃咬”一小片癌细胞膜。当这一小片癌细胞膜段包括一种抗原,即癌症特有的分子时,T细胞就可能开始在自己的细胞表面呈递该抗原,使得它在其他T细胞看来像一个癌细胞。
此前,人们认为胞啃作用与癌症阻碍抗癌免疫的能力有关,但是Fuchs团队确定了这一机制,表明暴露于肿瘤因子的T细胞经历了基因CH25H表达水平的明显下降。众所周知,该基因参与改变细胞的脂质膜,并能抑制两个细胞膜融合在一起,而这种细胞膜融合是发生胞啃作用的必要过程。当他们把CH25H产生的一种代谢物添加回去时,他们可以阻断胞啃作用。对该途径的进一步表征帮助Fuchs团队确定了另一个参与者,即ATF3基因,它拮抗CH25H的活性。消除AFT3能阻止胞啃作用的发生,并恢复了T细胞杀死肿瘤细胞的能力。
这些新的见解不仅为抗癌疗法提出了新的靶标,而且可能对CAR-T细胞疗法具有直接意义。由于胞啃作用可能会损害CAR-T细胞疗法中递送的工程化T细胞的有效性,这些作者推测,阻断这种作用可以提高CAR-T细胞的性能。Fuchs说,“我们想,为什么我们不使用被巧妙地称为‘装甲CAR(armored CAR)’的方法,并在CAR-T细胞中共同表达CH25H。事实证明,这比旧的CAR-T细胞更有效。”
5.Cancer Cell:粘液瘤病毒和CAR-T细胞/TCR-T细胞联手可诱导癌细胞自亡,有望更有效治疗实体瘤
doi:10.1016/j.ccell.2022.08.001
在一项新的研究中,来自美国亚利桑那州立大学和威克森林大学医学院等研究机构的研究人员利用粘液瘤病毒(myxoma virus)将免疫疗法和病毒疗法相结合,为难治性癌症患者提供了新的希望。相关研究结果发表在2022年9月12日的Cancer Cell期刊上,论文标题为“Induction of tumor cell autosis by myxoma virus-infected CAR-T and TCR-T cells to overcome primary and acquired resistance”。论文通讯作者为亚利桑那州立大学的Grant McFadden和威克森林大学医学院的Yong Lu。
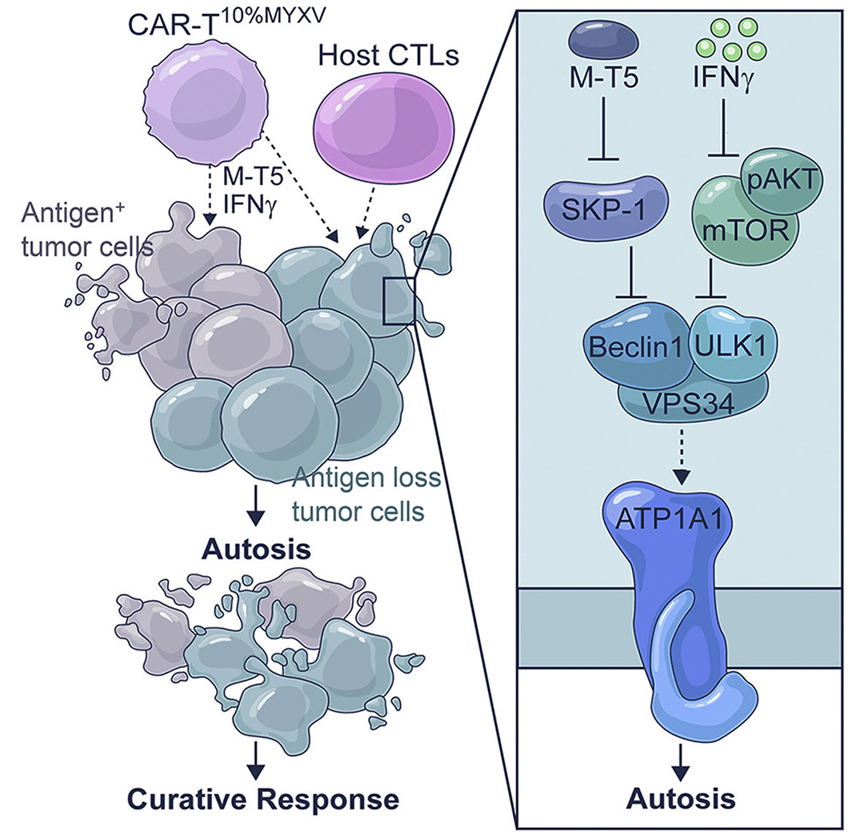
图片来自Cancer Cell, 2022, doi:10.1016/j.ccell.2022.08.001。
该方法涉及到两种方法的结合,这两种方法都对一些癌症显示出相当大的成功。该研究描述了溶瘤病毒疗法(一种使用抗癌病毒的技术)如何与现有的免疫治疗技术协同作用,提高免疫能力,有效地靶向和摧毁癌细胞。
这项新研究强调了免疫疗法与病毒疗法相结合时,能够突破癌症的抵抗力,特别是使用感染了粘液瘤病毒的CAR-T细胞或TCR-T细胞。粘液瘤病毒可以直接靶向并杀死癌细胞,但更有用的是可以诱导一种不寻常的T细胞定向细胞死亡形式,即自亡。这种形式的细胞死亡增强了T细胞诱导的其他两种程序性癌细胞死亡的形式,即细胞凋亡(apoptosis)和细胞焦亡(pyroptosis)。
在粘液瘤病毒介导的自亡期间,这种疗法靶向攻击的癌细胞附近的其他癌细胞也会在一种称为旁观者杀伤(bystander killing)的过程中被摧毁。这种效果可以显著提高这种双重疗法对癌细胞的积极根除效果,即使是在出了名的难以治疗的实体瘤中,也是如此。因此,这种联合使用粘液瘤病毒和免疫疗法的方法有可能将免疫系统无法检测到的“冷肿瘤”变成免疫细胞能够识别和摧毁的“热肿瘤”,从而使CAR-T细胞或TCR-T细胞进入肿瘤环境、增殖并激活。
6.Nat Med:靶向CD19的CAR-T细胞疗法有望治疗难治性红斑狼疮
doi:10.1038/s41591-022-02017-5
虽然红斑狼疮无法治愈,而且现有的治疗方法对美国150万红斑狼疮患者中的许多人不起作用,但一项新的研究显示,一种癌症疗法可能会缓解难以治疗的红斑狼疮。相关研究结果于2022年9月15日在线发表在Nature Medicine期刊上,论文标题为“Anti-CD19 CAR T cell therapy for refractory systemic lupus erythematosus”。
这项小型研纳入五名患有严重红斑狼疮的人,这种疾病累及多个器官,如肾脏、心脏、肺部和关节,对标准疗法没有反应。在一次治疗大约三个月后,患者的症状得到了改善,包括器官受累的缓解和疾病相关的自身抗体的消失。更重要的是,他们不需要任何额外的治疗。
论文通讯作者、德国埃尔朗根-纽伦堡大学的Georg Schett博士说,“严重的[红斑狼疮]对CAR-T细胞治疗非常敏感,[患者]可以进入长期的无药物缓解期。”
7.Cancer Cell:重大进展!新研究开发出可以根据需要开启或关闭的VIPER CAR-T细胞,有望更加安全地治疗癌症
doi:10.1016/j.ccell.2022.08.008
为了使开创性的CAR-T细胞疗法对患者来说风险更小,Wong及其团队正在努力构建一个内置于CAR-T细胞设计中的安全开关。在一项新的研究中,这些作者揭示了一种新型的CAR-T细胞,它们可以被开启或关闭,从而有可能在严重副作用发生之前阻止细胞激活。相关研究结果于2022年9月8日在线发表在Cancer Cell期刊上,论文标题为“High-performance multiplex drug-gated CAR circuits”。

图片来自Cancer Cell, 2022, doi:10.1016/j.ccell.2022.08.008。
他们的新系统被称为VIPER(Versatile ProtEase Regulatable) CAR-T细胞。所设计的VIPER CAR-T细胞可以通过给患者提供一种破坏细胞活性的抗病毒药物来加以控制,减少了传统CAR带来的安全问题。Wong说,“我们把它看作是这种类型疗法的下一代。”
在所有的CAR-T细胞中,CAR的一部分伸出细胞膜外,而另一部分位于细胞内。伸出细胞膜外的这一部分与癌症抗原结合,然后激活T细胞并摧毁癌细胞。VIPER CAR-T细胞在CAR附近插入了一个特殊的蛋白链。这些作者构建出两种不同的系统---一种是在VIPER CAR-T细胞转移回患者体内时开启,另一种是关闭。这两种系统的工作方式略有不同,但都可以通过患者服用美国食品药品管理局(FDA)批准的、通常用于治疗丙型肝炎的药物来关闭或开启。
论文共同第一作者、Wong实验室博士后Li Huishan说,“这是这项研究中最令人兴奋的部分,即抗病毒药物已经被FDA批准。”当给药时,这种药物分子与插入的这种蛋白链相互作用,从而在细胞中启动一系列反应,使它脱离,或激活,这取决于使用的是哪种系统。
doi:10.7554/eLife.79508
近日,一篇发表在国际杂志eLife上题为“Enhancing and inhibitory motifs regulate CD4 activity”的研究报告中,来自亚利桑那大学医学院等机构的科学家们通过研究发现了机体免疫系统内在工作机理的新信息,这或许对于后期开发抵御癌症和其它疾病的新型T细胞疗法具有非常深远的意义。
文章中,研究人员通过分析T细胞随着时间延续进行变化或保持不变的方式,对免疫系统采取了一种独特的进化方式,他们重点对CD4的进化和功能进行了深入研究。Kuhns博士表示,本文研究或能帮助我们绘制出一张蓝图来指示CD4分子如何与T细胞受体协同作用并自然地引导T细胞;CD4分子在抗原识别和T细胞激活方面发挥着非常平等的角色。
相关研究发现或能帮助研究人员为CD4内部的机制描绘出更加准确的进化蓝图,从而使得T细胞疗法的版本更加强大,嵌合抗原受体(CAR)T细胞疗法如今已经被用于治疗多种类型癌症,本文中,研究人员检测了遗传工程化修饰的5个模块CAR-T细胞作为治疗1型糖尿病的可能性。
研究人员分析了从鱼类到人类多种不同样本体内的CD4分子,旨在探索该分子超过4亿年的进化历程,随后他们识别出了对于哺乳动物非常特殊的CD4分子的特定区域;Van Doorslaer博士说道,我们研究了这些蛋白质中的哪些氨基酸会发生改变,以及这些蛋白质中的哪些氨基酸会保持不变,这对于研究蛋白质的功能非常重要。随后研究人员发现了一种称之为基序(motifs)的保守氨基酸序列,并揭示了这些基序增强或抑制CD4分子活性的分子机制,他们设计出了携带突变基序的基因并将其引入到T细胞系统中,随后观察蛋白质的反应,其在细胞中的位置以及会与什么发生相互作用,随后还观察到了其如何影响信号事件和结果;结果发现,不同的基序组合会导致不同程度的上调和下调。
9.JAMA Oncol:检测血液中的NfL蛋白水平可预测哪些癌症患者在接受CAR-T细胞治疗后更可能出现神经毒性
doi:10.1001/jamaoncol.2022.3738
基于细胞的免疫疗法--- CAR-T细胞疗法---已经彻底改变了对几种癌症的治疗。该疗法使用经过基因改造的T细胞来靶向和攻击某些类型的白血病和淋巴瘤。虽然它可以消除一些本来会死于癌症的患者体内的癌症,但它也伴随着一系列副作用的风险,其中的一些副作用会影响大脑功能,甚至可能危及生命。
在一项性能的研究中,来自美国华盛顿大学圣路易斯医学院的研究人员发现在CAR-T细胞治疗开始前进行简单的血液测试,可以确定哪些患者在CAR-T细胞治疗后的几天和几周内容易出现神经毒性副作用。他们在分析CAR-T细胞治疗之前、期间和之后的患者血液样本时发现,一种名为神经丝轻链(neurofilament light chain, NfL)的蛋白的水平在出现神经毒性并发症的患者中较高。高水平的NfL甚至在治疗开始前就存在,而且它的水平在整个治疗过程中和治疗后的一个月内都保持高位。相关研究结果于2022年9月1日在线发表在JAMA Oncology期刊上,论文标题为“Assessment of Pretreatment and Posttreatment Evolution of Neurofilament Light Chain Levels in Patients Who Develop Immune Effector Cell–Associated Neurotoxicity Syndrome”。
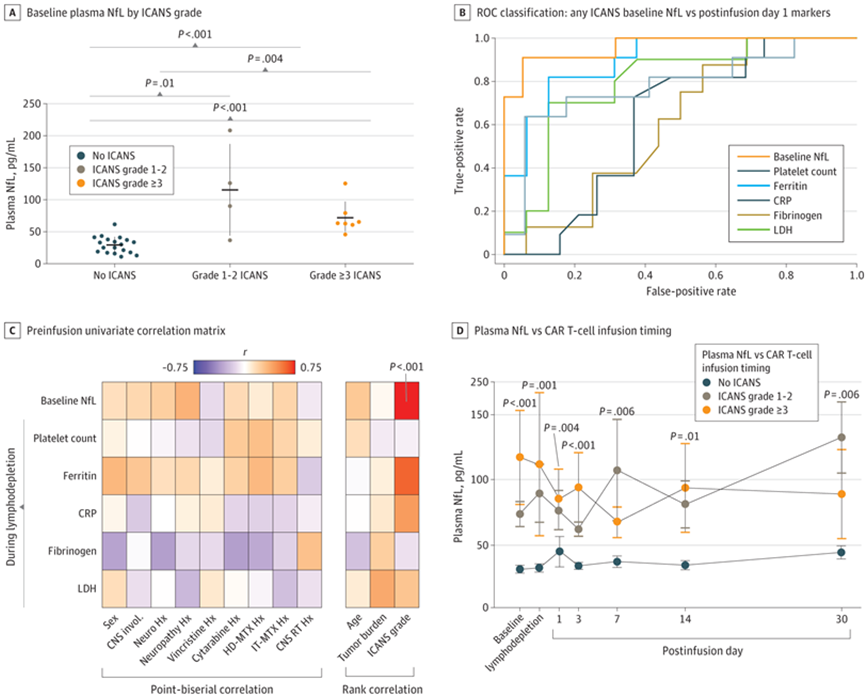
神经纤维轻链(NfL)水平与免疫效应细胞相关神经毒性综合征的关系。图片来自JAMA Oncology, 2022, doi:10.1001/jamaoncol.2022.3738。
这项新的研究可能帮助医生预测这些威胁生命的副作用,并使他们能够在患者接受CAR-T细胞治疗的早期开始给予减少神经毒性的治疗。它还为开发在CAR-T细胞治疗开始前预防这些副作用或降低其风险的方法打开了大门。
10.Blood Cancer Discov:肿瘤免疫微环境中的特定成分可能影响BCMA CAR-T细胞对骨髓瘤的疗效
doi:10.1158/2643-3230.BCD-22-0018
在一项新的研究中,来自美国埃默里大学和宾夕法尼亚大学的研究人员发现肿瘤免疫微环境具有更多样化的基线T细胞库、更少的免疫细胞衰竭标志物以及免疫细胞群体出现明显变化的骨髓瘤患者,在接受靶向BCMA的嵌合抗原受体T(BCMA CAR-T)细胞疗法治疗后更有可能获得更长的无进展生存期(progression-free survival, PFS)。相关研究结果于2022年8月26日在线发表在Blood Cancer Discovery期刊上,论文标题为“Changes in Bone Marrow Tumor and Immune Cells Correlate with Durability of Remissions Following BCMA CAR T Therapy in Myeloma”。
在这项新的研究中,这些作者分析了28份治疗前和治疗后的骨髓样本,这些患者在Cohen及其同事们领导的先前报道的I期临床试验中对靶向BCMA的 CAR-T细胞疗法有临床反应。他们发现在无进展生存期较长的患者中,治疗后骨髓中T细胞的比例增加,而骨髓细胞的比例下降。这些变化在无进展生存期较短的患者中没有观察到。Dhodapkar建议,较高比例的骨髓细胞可能通过促进癌症生长和/或抑制抗肿瘤免疫反应而促成了这些患者的癌症复发。
这些作者还发现,来自无进展生存期较长的患者的治疗后CAR-T细胞(即表达CAR的T细胞)和非CAR T细胞(即不表达CAR的T细胞)具有明显的基因组特征,与无进展生存期较短的患者相比,免疫检查点基因和其他与T细胞衰竭相关的基因表达较低。此外,来自无进展生存期较长的患者的T细胞中与骨髓保留有关的基因表达较高。
基线特征也与无进展生存期有关:在来自无进展生存期较长的患者的治疗前骨髓样本中观察到更大的T细胞受体多样性,更高的干扰素反应基因和成熟血浆基因的肿瘤中表达,以及与上皮-间质转化(epithelial-to-mesenchymal transition, EMT)有关的基因的肿瘤中表达较低。
11.Blood Adv:在批准的临床剂量范围内,更高剂量的CAR-T细胞产品tisagenlecleucel可导致更高的存活率
doi:10.1182/bloodadvances.2022007246
根据一项新的研究,在美国食品药品管理局(FDA)批准的tisagenlecleucel---一种嵌合抗原受体T细胞(CAR-T)产品---剂量范围内,接受较量剂量的年轻人与在该范围内接受较低剂量的人相比,具有明显更高的一年生存率。相关研究结果近期发表在Blood Advances期刊上,论文标题为“Higher doses of tisagenlecleucel associate with improved outcomes: a report from the pediatric real-world CAR consortium”。
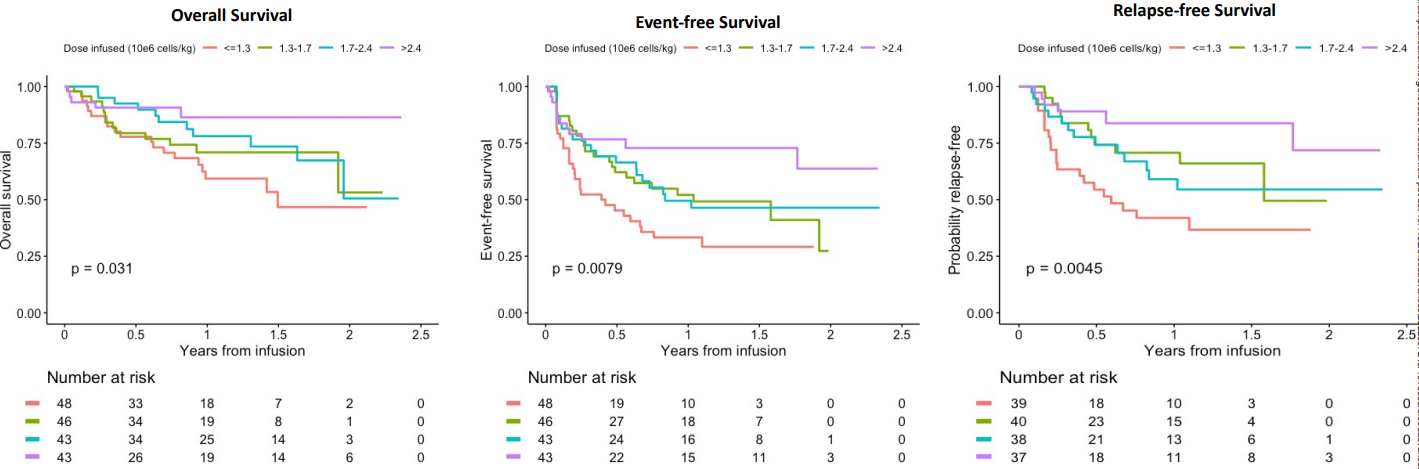
不同CAR-T细胞剂量四分位数的总生存期(OS)、无事件生存期(EFS)和无复发生存期(RFS)。图片来自Blood Advances, 2022, doi:10.1182/bloodadvances.2022007246。
在这项新的研究中,这些作者分析了185名26岁或以下接受tisagenlecleucel治疗的复发或难治性B-ALL患者一年后的总生存率、无事件生存率和无复发生存率。他们发现与接受较低剂量(0至130万个CAR-T细胞/公斤)的患者相比,接受批准范围内较高剂量(240万至510万个CAR-T细胞/公斤)的患者在所有三项指标上的存活率都明显较高。在最高剂量组中,86%的患者在一年后仍然生存,而最低剂量组中,这一数字为59%。这些作者没有观察到任何毒性增加的迹象或更高剂量的安全问题。
这些研究结果表明给送批准范围内较高剂量的tisagenlecleucel可能有助于获得更有效的长期反应,而不会提高毒性风险。Schultz博士说,“很多努力都集中在下一代CAR-T细胞疗法的复杂设计和开发上。这项新的研究旨在探索使用我们目前批准的tisagenlecleucel的临床操纵是否能在该领域取得渐进式的进步。
12.BMC Cancer:杀伤肿瘤细胞!----一种非病毒mcDNA介导的双特异性CAR T细胞
doi:10.1186/s12885-022-09861-1
肝细胞癌(HCC)是全球最常见的癌症之一,其过继性免疫疗法值得研究。CD133是一种癌症干细胞(CSC)抗原,与glypican-3(GPC3)一起已被证明在HCC细胞中高度表达,并且它们可作为作产生嵌合抗原受体(CAR)T细胞的靶标。但在CAR T细胞治疗中存在“脱靶”毒性,存在低转染疗效和抗肿瘤能力弱等局限性。
近段时间来自中国复旦大学附属中山医院的一个研究团队针对一种非病毒mcDNA介导的双特异性CAR T细胞进行了研究,旨在研究其抑制肿瘤增殖能力。
本研究从健康供体获得外周血,通过密度梯度离心分离T细胞。研究人员使用电穿孔系统将抗CD133和抗GPC3单链片段变量(scFv)结构作为靶基因递送到T细胞中。细胞膜由瞬时电流效应打开,靶基因通过非病毒微圆DNA(mcDNA)载体递送到细胞中。采用流式细胞术和蛋白质印迹法检测两种scFv是否同时转染以及该双特异性CAR-T细胞生成方法的转染功效。再通过CCK-8测定和HCC异种移植小鼠模型分别检测了CAR T细胞的体外和体内肿瘤抑制功效。同时含有CD133和GPC3抗原识别位点的CoG133-CAR T细胞是效应细胞。CD133-CAR T细胞和GPC3-CAR T细胞定义为单靶向对照组,正常T和模拟T细胞定义为空白对照组。
mcDNA载体适应两个成功转染的靶基因结构以产生双特异性CAR T细胞。基因水平和蛋白质水平的检测方法证实,CoG133-CAR T细胞具有较强的转染效率,并表现出CD133和GPC3的抗原结合能力。与单靶点CAR T细胞或对照T细胞相比,CoG133-CAR T细胞在体外对CD133和GPC3双阳性HCC细胞系和体内HCC异种移植小鼠具有增强的消除功效。苏木精和曙红(H&E)染色表明CoG133-CAR T细胞和主要器官上不存在致命的“脱靶”组合。
该研究表明,通过非病毒mcDNA载体制备双特异性CAR T细胞具有更高的效率和安全性。CoG133-CAR T细胞通过双重抗原识别和内部激活增强肿瘤抑制能力。它为肝细胞癌(甚至是实体瘤)的CAR-T治疗提供了一种创新策略。
13.JCI:科学家开发出一种能确定CAR-T免疫疗法成功的新技术 或有望改进人类淋巴瘤的治疗
doi:10.1172/JCI159402
在人类抗癌战争中,最关键的战斗之一就是在细胞水平上进行的,因为来自免疫系统的T细胞能在实验室中被改变从而攻击癌细胞,这种称之为嵌合抗原受体T细胞疗法(CAR-T细胞疗法)的免疫疗法就成为了挽救癌症患者的一种疗法,其能成功控制肿瘤十年甚至更长时间。近日,一篇发表在国际杂志Journal of Clinical Investigation上题为“Multidimensional single-cell analysis identifies a role for CD2-CD58 interactions in clinical antitumor T cell responses”的研究报告中,来自休斯顿大学等机构的科学家们通过研究发现了一种新方法,其或能帮助确定哪些患者可能会对CAR-T细胞疗法产生反应,从而就能节省治疗人类淋巴瘤的时间,淋巴瘤对这类免疫疗法的反应最为强烈,这或许就能作为非常有价值的研究结果,因为并非所有的患者都会对CAR-T细胞疗法产生反应,而且有些患者还会经历严重的副作用。
为了确定最佳的患者治疗结局,医学博士Navin Varadarajan等人研究了T细胞和肿瘤细胞之间的动态相互作用,这一研究发现揭示了癌细胞表面名为CD58的配体分子与T细胞上名为CD2的蛋白之间的关联,其相互交流沟通或能激活CD2并使其转变为癌细胞杀手。Varadarajan说道,作为CD2的配体,CD58会在对CAR-T细胞疗法反应较好的淋巴瘤患者的肿瘤中高水平表达,为此我们就发现,T细胞上的CD2或许与细胞的定向迁移有关,而且T细胞上的CD2与淋巴瘤细胞上的CD58之间的相互作用或许会加速杀伤和连续性的杀伤性作用。
这篇研究报告中,研究人员使用TIMING方法(纳米孔网格的延时成像显微技术,Timelapse Imaging Microscopy In Nanowell Grids)剖析了构成患者输注产品和肿瘤之间的动态相互作用,该方法是由Varadarajan的实验室所开发的,其是一种高通量的单细胞技术,能将人工智能与纳米孔成像平台相结合,同时评估单细胞移动、激活、相互作用、杀伤性和生存的状况。通过分析T细胞和肿瘤细胞之间数以千计的单一互动机制,研究人员识别出了CD2和CD58之间的重要相互作用,为了将这一研究结果转化为临床,研究人员对患者开始治疗前所获得的肿瘤进行染色分析,研究者指出,相比肿瘤中并未表达CD58的患者而言,肿瘤组织中表达CD58的患者或许对CAR-T细胞疗法产生强烈的反应。(生物谷Bioon.com)
相关生物谷新闻:
CAR-T细胞疗法研究进展(第31期)
https://news.bioon.com/article/18a5e37253a6.html
CAR-T细胞疗法研究进展(第30期)
https://news.bioon.com/article/9f42e3387698.html
CAR-T细胞疗法研究进展(第29期)
https://news.bioon.com/article/fa2de30910bc.html
CAR-T细胞疗法研究进展(第28期)
https://news.bioon.com/article/421ee25913ae.html
CAR-T细胞疗法研究进展(第27期)
https://news.bioon.com/article/2b8ce2333732.html
CAR-T细胞疗法研究进展(第26期)
https://news.bioon.com/article/6925e22593aa.html
CAR-T细胞疗法研究进展(第25期)
https://news.bioon.com/article/38c6e1997279.html
CAR-T细胞疗法研究进展(第24期)
https://news.bioon.com/article/1d0ce18970c8.html
CAR-T细胞疗法研究进展(第23期)
https://www.bioon.com/article/6790460.html
CAR-T细胞疗法研究进展(第22期)
https://news.bioon.com/article/6787633.html
CAR-T细胞疗法研究进展(第21期)
https://www.bioon.com/article/6786803.html
CAR-T细胞疗法研究进展(第20期)
https://news.bioon.com/article/3288e1261464.html
CAR-T细胞疗法研究进展(第19期)
https://www.bioon.com/article/6783616.html
CAR-T细胞疗法研究进展(第18期)
https://www.bioon.com/article/6781383.html
CAR-T细胞疗法研究进展(第17期)
https://news.bioon.com/article/6778905.html
CAR-T细胞疗法研究进展(第16期)
https://www.bioon.com/article/6759479.html
CAR-T细胞疗法研究进展(第15期)
https://news.bioon.com/article/6758088.html
CAR-T细胞疗法研究进展(第14期)
https://www.bioon.com/article/6756207.html
CAR-T细胞疗法研究进展(第13期)
https://news.bioon.com/article/6751734.html
CAR-T细胞疗法研究进展(第12期)
https://news.bioon.com/article/495b68093975.html
CAR-T细胞疗法研究进展(第11期)
https://www.bioon.com/article/6748552.html
CAR-T细胞疗法研究进展(第10期)
https://www.bioon.com/article/6747291.html
CAR-T细胞疗法研究进展(第9期)
https://www.bioon.com/article/6744554.html
CAR-T细胞疗法研究进展(第8期)
https://news.bioon.com/article/6741848.html
CAR-T细胞疗法研究进展(第7期)
https://www.bioon.com/article/6738997.html
CAR-T细胞疗法研究进展(第6期)
https://news.bioon.com/article/4e27668e7876.html
CAR-T细胞疗法研究进展(第5期)
https://news.bioon.com/article/6728191.html
CAR-T细胞疗法研究进展(第4期)
https://news.bioon.com/article/6722761.html
CAR-T细胞疗法研究进展(第3期)
https://www.bioon.com/article/6713293.html
CAR-T细胞疗法研究进展(第2期)
https://www.bioon.com/article/6709104.html
CAR-T细胞疗法研究进展(第1期)
https://news.bioon.com/article/6702848.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


