卫材减肥药Belviq史上最大规模上市后心血管预后研究达到主要&次要终点
2018年7月19日讯 /生物谷BIOON/ --日本药企卫材(Eisai)近日宣布,评估减肥药Belviq(lorcaserin,洛卡西林)心血管预后的III期临床研究CAMELLIA-TIMI61已获得了积极顶线数据。该研究是一项上市后临床研究,在12000例患者中开展,首要目标是评价安全性。Belviq于2012年6月获得美国食品和药物管理局(FDA)批准,结合低热量饮食及增加体力劳动,用于
难以复制的抗癌奇迹:格列卫诞生之路
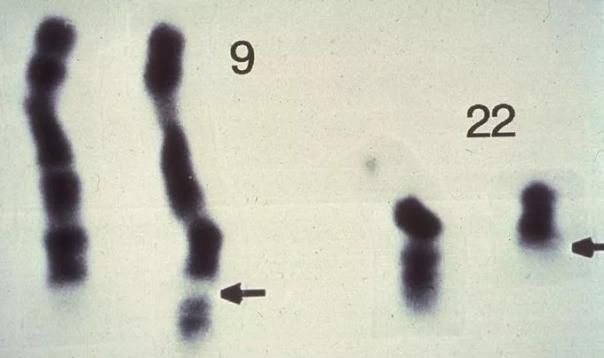
有人将它称为一个奇迹,也有人把它比作是杀死魔物的银色子弹。自2001年获批问世以来,格列卫(Gleevec,imatinib)在慢性白血病的治疗上取得了傲人的成绩,被誉为是人类抗癌史上的一大突破。而在最近,随着一部电影的上映,格列卫这个名字,又再次成为了公众热议的话题。癌症与染色体让我们先把时钟拨回到100年前。当时的科学家们对癌症知之甚少,主流学界也简单地把癌症归因于病毒
冯艳辉:卫材中国的产品战略发展
2018年5月8日,国务院总理李克强对日本进行为期四天的国事访问,今年恰逢进入了中日和平友好条约缔结40周年,总理访日为推动两国关系未来发展勾勒战略规划。在医药领域中,日本的跨国药企在国内始终占有一定的市场份额。卫材株式会社从上世纪90年代初涉中国市场,先后设立了沈阳卫材制药有限公司和卫材(苏州)制药有限公司,于2002年正式更名为卫材(中国)药业有限公司。伴随着中国业务的发展,于2010年在苏州
游戏瘾被世卫组织列为疾病 医学界看法不一
世界卫生组织17日发布最新版《国际疾病分类》,把“游戏障碍”、即通常所说的游戏成瘾列为疾病。【是“病”】根据世卫组织的定义,游戏障碍是一种游戏行为模式,包括玩数码游戏或视频游戏,特点是对玩游戏失去控制力,日益沉溺于游戏,以至于其它兴趣和日常活动都须让位于游戏,即使出现负面后果,仍然继续玩游戏或不断升级。世卫组织说,游戏障碍有持续性和反复性,可对个人、家庭、社会、教育、职业及其他重要功能性领域造成重
国家卫健委:公立医院部分服务可委托给第三方医疗机构
6月19日,国家卫健委发布《关于进一步改革完善医疗机构、医师审批工作的通知》(下称《通知》),为医疗机构与医护人员审批注册流程“松绑”。全面实施医护电子化注册管理、医学检验等服务委托给独立设置医疗机构、医疗机构名字被规范、简化医疗机构审批申请材料、二级及以下医疗机构设置审批与执业登记“两证合一”、妇产科医生“二证合一”,从医疗机构到医生护士,将不再为审批注册所苦。1. “在
艾伯维&卫材在日本推出修美乐(Humira)自动注射笔
2018年6月12日讯 /生物谷BIOON/ --艾伯维(AbbVie)与卫材(Eisai)近日宣布,在日本市场推出抗炎药修美乐(Humira,通用名:adalimumab,阿达木单抗)自动注射递送系统:HUMIRA®皮下注射笔(40mg/0.4mL,80mg/0.8mL)。Humira是一种全人源化抗TNF-α单克隆抗体,于2008年在日本上市,迄今已获批10种适应症,包括:类风湿性关
默沙东HPV疫苗Gardasil 9(加卫苗,9价)获美国FDA优先审查
2018年6月14日讯 /生物谷BIOON/ --美国制药巨头默沙东(Merck & Co)近日宣布,美国食品和药物管理局(FDA)已受理Gardasil 9(加卫苗,9价重组人乳头状瘤病毒疫苗)的一份补充生物制品许可(sBLA)并授予了优先审查资格,其处方药用户收费法(PDUFA)日期为2018年10月6日。该sBLA旨在寻求批准扩大Gardasil 9的年龄适应症,用于27-45岁的男
卫材睡眠障碍新药lemborexant显著改善夜间觉醒及次日清晨姿势稳定性和驾驶性能
2018年6月6日讯 /生物谷BIOON/ --日本药企卫材(Eisai)与普渡制药(Purdue Pharma)近日在美国马里兰州巴尔的摩市举行的第32届美国联合专业睡眠学会年会(SLEEP 2018)上公布了实验性睡眠/觉醒调节剂lemborexant的2个关键性I期临床研究(Study 108,Study 106)的数据。Study 108研究:听觉觉醒阈值评价lemborexant相对于唑
卫材/百健口服BACE抑制剂elenbecestat显著降低大脑中β淀粉样斑块水平
2018年6月6日讯 /生物谷BIOON/ --卫材(Eisai)与合作伙伴百健(Biogen)近日公布了口服BACE抑制剂elenbecestat(研发代码:E2609)治疗阿尔茨海默氏症(AD)II期临床研究Study 202(NCT02322021)的数据。该研究是一项多中心、司机、双盲、安慰剂对照、平行组、18个月研究,在由AD引起的轻度认知损害(MCI)或因AD引起的轻度至中度痴呆的患者
卫材Fycompa新增申请治疗小儿癫痫获FDA优先审批
日前,卫材公司宣布美国食品药品监督管理局(FDA)已接受审查旗下抗癫痫药物Fycompa(perampanel)的补充新药申请(sNDA)。本次申请寻求为该药物新增儿科适应症,以涵盖部分发作性癫痫发作和原发性全身性强直阵挛性发作(PGTC)及癫痫发作的儿科患者。此外,卫材在FDA要求的儿科适应症书面申请中纳入了一项针对这一sNDA的研究,因此FDA已指定此申请进行优先评审,这意味着评审