呋喹替尼获FDA快速通道资格 海外上市进程加速
近日,和黄医药旗下靶向抗癌药呋喹替尼获得了FDA授予的快速通道资格,用于治疗转移性结直肠癌(mCRC)患者。作为FDA建立的加速审评审批程序之一,快速通道资格的获取意味着药品在研发和注册过程将得到FDA更多的关注,缩短新药研发上市的时间。和黄医药呋喹替尼获得FDA授予的快速通道资格,无疑将加快该药在美国的上市进程,为海外的转移性结直肠癌患者带来新
阿斯利康Koselugo在日本获孤儿药资格,已在美国上市!
NF1是一种常常导致毁容的、罕见的遗传病,导致肿瘤在神经上生长,Koselugo是一种口服、强效、选择性MEK1/2激酶抑制剂。
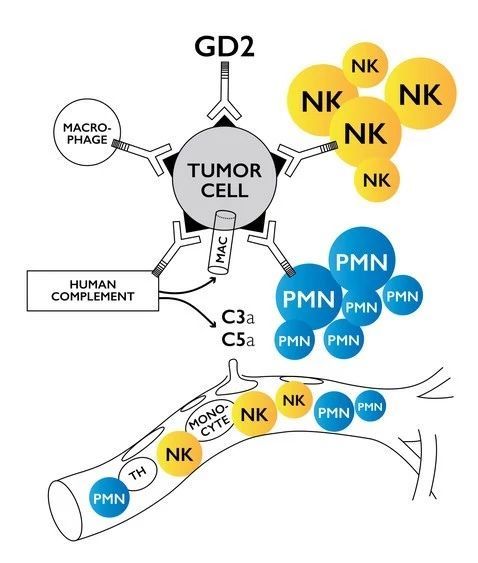
创新GD2抗体获FDA优先审评资格
Y-mAbs Therapeutics宣布,该公司为GD2抗体naxitamab递交的生物制品许可申请(BLA)已被美国FDA接受并授予优先审评资格,适应症为复发/难治性高危神经母细胞瘤患者。FDA预计将在今年11月30日前做出回复。FDA还表示,目前不计划召开咨询委员会会议讨论该申请。Naxitamab是一款靶向GD2抗原的人源化单克隆抗体。G
Rhythm遗传性肥胖症疗法获FDA优先审评资格 有望今年上市
Rhythm Pharmaceuticals公司宣布,美国FDA已经接受其开发的MC4R激动剂setmelanotide,治疗阿片促黑皮质素原(POMC)和瘦素受体(leptin receptor,LEPR)缺陷型肥胖症患者的新药申请(NDA),并同时授予其优先审评资格,预计将在今年11月27日做出回复。Pomc和LEPR缺乏性肥胖症是极其罕见的
阿斯利康/第一三共靶向药物Enhertu获美国FDA授予第三个突破性药物资格!
目前,针对HER2m NSCLC患者,尚无药物获得批准。Enhertu有潜力成为第一个被批准用于治疗NSCLC的HER2导向疗法。
美国FDA授予Moderna公司疫苗产品mRNA-1273快速通道资格,初夏进入III期临床!
2020年05月13日讯 /生物谷BIOON/ --新冠肺炎疫情正在全球迅速蔓延。根据百度《新型冠状病毒肺炎疫情实时大数据报告》,截止2020年05月13日11时,全球累计确诊超过434万例,国外累计确诊超过425万例、死亡超过28.8万例。美国累计确诊293万例,死亡8.3万例。疫苗被认为是对抗新冠肺炎的终极武器。目前,已有相当多的企业投身疫苗研发领域,而
美国FDA授予阿斯利康Enhertu突破性药物资格,将重新定义胃癌治疗!
Enhertu将成为治疗HER2阳性胃癌的第一个抗体药物偶联物(ADC)药物,将为这类毁灭性癌症带来一个重要的新疗法。
安进新型心肌肌球蛋白激活剂omecamtiv mecarbil获美国FDA快速通道资格!
2020年05月09日讯 /生物谷BIOON/ --安进(Amgen)与合作伙伴Cytokinetics近日联合宣布,美国食品和药物管理局(FDA)已授予omecamtiv mecarbil快速通道资格(FTD),该药是一种新型选择性心肌肌球蛋白激活剂,目前正开发用于治疗射血分数降低的慢性心力衰竭(HFrEF)。快速通道资格(FTD)旨在加速针对严重疾病的药