Cell:40年来首次,治愈急性白血病的方法近在咫尺
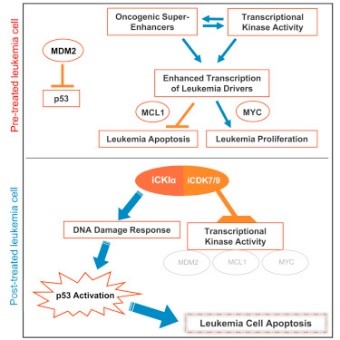
2018年8月25日讯 /生物谷BIOON /——文章亮点:研究人员开发了一种同时靶向CKIα和CDK7/9的口服活性小分子抑制剂;晶体学分析为共靶向不同激酶的作用提供了结构基础;这种抑制剂可以选择性杀死AML前体细胞并治愈AML小鼠;治疗的机理包括p53激活以及超级增强子(super-enhancers,SE)关闭。图片来源:Cell清除CKIα会导致p53激活,而CKIα降解是来那度胺治疗白血
Nature医学:维生素B3或可治疗急性肾损伤?
8月20日,《Nature Medicine》期刊发表了这一篇题为“De novo NAD+ biosynthetic impairment in acute kidney injury in humans”文章,由Beth Israel Deaconess医学中心的肾病学家和首席研究员Samir M. Parikh领导的多学科研究小组最新证实,一种维生素B3有望预防急性肾损伤。急性肾损伤是一组临
Nature子刊颁布CAR-T疗法指南 关联儿童急性淋巴细胞白血病
去年8月,FDA批准CAR-T疗法用于治疗急性淋巴细胞白血病(ALL)。一年后,德克萨斯大学MD Anderson癌症中心联合儿科急性肺损伤和脓毒症研究者网络(PALISI)的科学家们发布了关于儿童接受CAR-T细胞治疗的全面共识指南。指南汇集顶级专家在识别治疗相关毒性的早期迹象和症状方面吸取的经验教训,并详细介绍了应对这些症状的方法。8月6日,《Nature Review
AcelRx公司止痛药Dzuveo(舒芬太尼舌下片)获欧盟批准,管理急性中重度疼痛
2018年6月29日讯 /生物谷BIOON/ --AcelRx Pharma是一家专注于开发创新疗法用于医疗监管情景的特种药公司。近日,该公司近日宣布,欧盟委员会(EC)已批准Dzuveo(美国品牌名为Dsuvia)用于医疗监测环境中成人急性中度至重度疼痛的管理。目前,该药也在接受美国FDA的审查,其处方药用户收费法(PDUFA)目标日期为2018年11月3日。Dzuveo是一种舌下含片,含有30
Vyxeos即将上市欧盟,治疗2种特定的急性髓性白血病(AML)
2018年6月30日讯 /生物谷BIOON/ --Jazz制药公司近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布积极意见,推荐批准Vyxeos 44mg/100mg输液用浓缩粉末,用于2种新诊成人急性髓性白血病(AML):治疗相关性急性髓性白血病(t-AML)或伴骨髓增生异常相关改变的急性髓性白血病(AML-MRC)。之前,欧盟委员会已授予Vyxeos孤儿药资格,CHMP还
辉瑞glasdegib被美国FDA授予优先审查,一线治疗急性髓性白血病(AML)
2018年6月27日讯 /生物谷BIOON/ --制药巨头辉瑞(Pfizer)近日宣布,美国FDA已受理靶向药物glasdegib的新药申请(NDA)并授予了优先审查资格,其处方药用户收费法(PDUFA)目标日期为2018年12月。该药是一种实验性口服Smoothened蛋白(SMO)抑制剂,目前正被评估联合低剂量阿糖胞苷(LDAC)化疗,用于既往未接受治疗的(初治)急性髓性白血病(AML)成人患
对抗移植后急性免疫反应 Incyte发布首创新药积极数据
近日,Incyte公司宣布其正在进行的关键性2期REACH1试验取得了积极的成果,该试验评估了Jakafi?(ruxolitinib,鲁索利替尼)联合皮质类固醇治疗类固醇难治性急性移植物抗宿主病(GVHD)的效果。2016年,Incyte和礼来修订ruxolitinib的授权、开发和商业化协议,使Inycte能够独立开发和商业化该药物用于GVHD的治疗。今年4月,Incyt
Jakafi治疗类固醇难治性急性移植物抗宿主病(GVHD)II期临床获得成功
2018年06月22日/生物谷BIOON/--Incyte公司近日公布了Jakafi(ruxolitinib,鲁索替尼)联合皮质类固醇治疗类固醇难治性急性移植物抗宿主病(GVHD)的关键性II期临床研究REACH1的顶线结果。数据显示,该研究达到了主要终点,治疗第28天时的总缓解率(ORR)达到了55%(n=39/71)。此外,最佳总缓解率(BORR,即研究期间任何时间点获得缓解的患者比例)为73
Leukine获美国FDA批准治疗急性放射综合征
6月6日,商业化阶段生物制药公司Partner Therapeutics(PTx)公布称,美国FDA已于近日批准Leukine? (sargramostim)用于治疗急性暴露于骨髓抑制剂量放射物成人和儿童的治疗,该疾病也被称为急性辐射综合征(H-ARS)。Leukine是第一种在辐射照射后48小时才开始使用依然可以改善生存率的H-ARS治疗药物。H-ARS有时称为辐射毒性或
美国FDA批准Leukine(沙格司亭)治疗急性辐射综合征造血异常(H-ARS)
2018年6月8日讯 /生物谷BIOON/ --美国生物技术公司Partner Therapeutics近日宣布,美国食品和药物管理局(FDA)已批准Leukine(sargramostim,沙格司亭)用于急性暴露于骨髓抑制剂量辐射的儿童和成人患者,治疗急性放射综合征造血异常(H-ARS),以提高生存率。值得一提的是,Leukine是首个在辐射暴露48小时后用药能够明显提高生存率的H-ARS治疗药