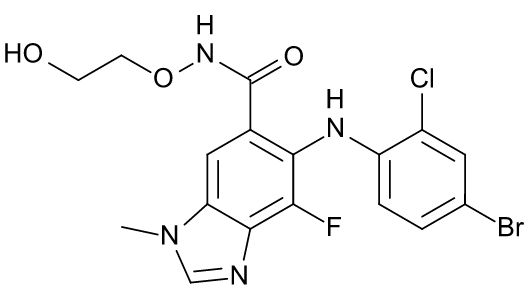
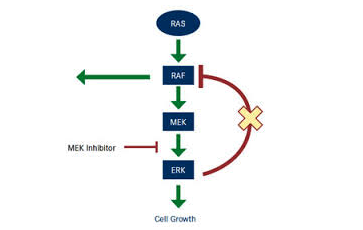
基石药业自主研发的MEK抑制剂CS3006在中国获得临床试验批件
中国苏州,2018年7月30日——基石药业(苏州)有限公司(以下简称“基石药业”)今日宣布,其自主研发的小分子MEK1/2抑制剂CS3006的临床试验申请已获得国家药品监督管理局(“国家药监局”)的批准,自今年国家药监局4月宣布受理CS3006的临床试验申请日期仅3个月时间。CS3006研发团队基石药业首席执行官江宁军博士表示:“我们非常高兴国家药监局授予CS3006特殊审
阿斯利康MEK抑制剂selumetinib被授予治疗1型神经纤维瘤病(NF1)的孤儿药资格
2018年08月03日讯 /生物谷BIOON/ --英国制药巨头阿斯利康(AstraZeneca)近日宣布,欧洲药品管理局(EMA)已授予selumetinib治疗1型神经纤维瘤病(NF1)的孤儿药资格。在美国方面,FDA在今年2月也授予了selumetinib治疗NF1的孤儿药资格。孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在欧洲,罕见病是
基石药业PD-1抑制剂CS1003获国家药监局批准临床
基石药业(苏州)有限公司(以下简称“基石药业”或“公司”)今日宣布其自主研发的抗程序性死亡受体-1 (PD-1) 抗体 CS1003 注射液的临床试验申请已获得国家药品监督管理局(“国家药监局”)批准。CS1003 的临床试验申请被国家药监局授予特殊审批流程,从临床申请获国家药审中心受理到批准仅用时不到4个月。基石药业将于近期启动一项多中心、I期临床试验,以评估CS1003
ESMO:MEK抑制剂selumetinib无法延长Kras突变NSCLC患者生存期
本月召开的ESMO公布了阿斯利康的MEK抑制剂selumetinib联合多烯紫杉醇治疗Kras突变NSCLC的临床试验数据,表明该组合疗法无法有效延长患者的无进展生存期或者总体生存期。
FDA批准罗氏MEK抑制剂Cotellic
【新闻事件】:今天FDA批准了罗氏的MEK抑制剂Cotellic (通用名cobimetinib),和BRAF抑制剂Zelboraf (通用名vemurafenib)联用用于治疗BRAF V600E或 V600K变异的晚期黑色素瘤。这是继葛兰素的Taf/Mek组合之后的第
Cancer Cell:MEK抑制剂联用尼罗替尼克服CML耐药
11月8日,英国癌症研究所宣布,根据他们发表在美国最新一期学术刊物Cancer Cell上的研究论文"Nilotinib and MEK inhibitors induce synthetic lethality through paradoxical activation of RAF in drug-resistant chronic myeloid leukaemia"...
Cancer Discovery:携带BRAF L597和K601突变的黑色素瘤对MEK抑制剂药物治疗敏感
在一项新研究中,研究人员发现发生罕见BRAF基因突变的黑色素瘤患者对MEK抑制剂药物作出反应,这就为开展日常筛选和治疗携带BRAF L597突变的黑色素瘤患者提供理论基础。 在大约40%到50%的黑色素瘤中,经常发生BRAF V600E或KIT突变。阻断或抑制BRAF V600E的药物最近被批准用来治疗携带这些突变的黑色素瘤患者。
BJC:联合使用ALK和MEK抑制剂治疗非小细胞肺癌
非小细胞肺癌(Non-small-cell carcinoma )包括鳞癌、腺癌、大细胞癌,与小细胞癌相比其癌细胞生长分裂较慢,扩散转移相对较晚,约占肺癌总敉的80-85%。 近日,BJC(British Journal of Cancer)发表了日本近畿大学医学院和达纳法伯癌症研究所研究人员在非小细胞肺癌领域的研究成果。