Biotronik新型冠状动脉支架登陆美国
著名医疗器械公司Biotronik最近宣布,公司已经收到FDA通知,批准其开发的新型冠状动脉支架产品PRO-Kinetic钴铬合金冠状动脉系统登陆美国市场。这一产品被批准治疗直径在2.25毫米-4毫米的新生或复发冠状动脉血栓。
单链DNA介导的人工限制性内切酶PfAgo或可用于捕获基因簇
限制性内切酶是一识别DNA序列并在识别序列或识别序列附近进行切割的细菌蛋白。大多数限制性内切酶如II型限制酶,只能识别较短的DNA序列(如4-8bp),这大大限制了这种酶在DNA重组技术中的应用。为了克解决以上难题,
IBM Watson Health将与FDA协作研究,如何借助区块链技术实现医疗保健数据的安全交换
近日,IBM Watson人工智能医疗保健解决方案部门——IBM Watson Health已与美国食品和药物管理局 (FDA) 签署了一项研究计划,旨在如何借助区块链技术实现医疗保健数据的安全、高效和可扩展性。IBM和FDA将联合探索如何
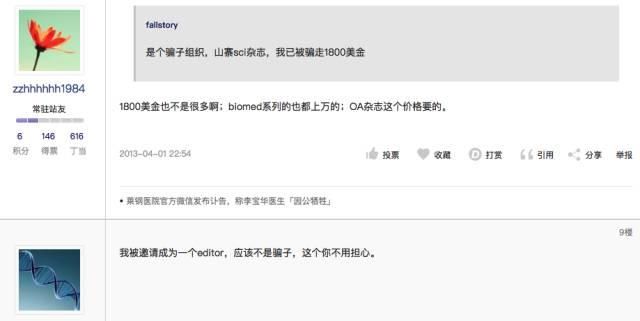
全球学术刊物欺诈的隐秘生意链:3 小时发论文到国际期刊
Kevin Carey俄亥俄州立大学 MPA约翰霍普金斯大学 教育政策 讲师New America 教育政策总监《纽约时报》教育版作者《纽约时报》发表了美国高等教育政策之神凯文 (Kevin Carey)在去年的最后一天曝光了一个重大彩蛋,在
美敦力SOLITAIRE(TM)取栓支架获美国FDA许可扩大其适应症
上海2016年12月27日电 /美通社/ -- 美敦力公司近日宣布美国食品药监局(FDA)已经批准扩大对Solitaire?取栓支架的适应症。FDA现允许对Solitaire?取栓支架进行市场销售,并将其作为对于存在前循环、近端大动脉
刘青博士:全降解血管支架及其3D打印技术
12月16日,由生物谷主办的“2016年医用新材料与植入修复技术创新峰会”进入第二天。为了让参会者对3D打印行业有更深刻的了解,主办方邀请到北京阿迈特医疗器械有限公司刘青博士,他将从3D打印血管支架的维度解析3D打印医疗器械的发展态势。
FDA批准美敦力支架产品Solitaire增添新适应症降低中风致残风险
医疗器械巨头美敦力公司最近再次收获了一个利好消息。公司开发的Solitaire血栓摘取支架产品获得了FDA批准扩大其适应症范围,增加用于治疗患者因为急性缺血性脑卒中而引发的多种并发症如近端前循环或大血管阻塞、或较小区域核心梗死甚至残疾等适应症,包括。该产品最初于2012年3月获得FDA批准用于清除患者脑部血管中血块以恢复血流并治疗中风。此次FDA的新决定进一步扩大了该产品的潜在市场。