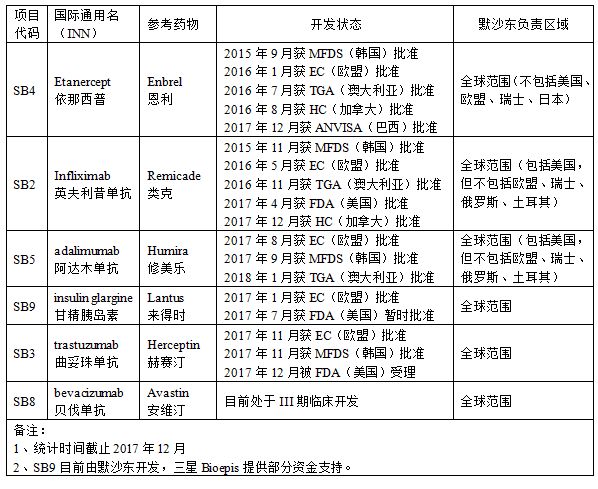
默沙东在英国推出赫赛汀生物仿制药Ontruzant(曲妥珠单抗)
2018年03月09日讯 /生物谷BIOON/ --美国制药巨头默沙东(Merck & Co)近日宣布在英国推出生物仿制药Ontruzant(trastuzumab,曲妥珠单抗),该药是瑞士制药巨头罗氏品牌药Herceptin(赫赛汀,通用名:trastuzumab,曲妥珠单抗)的生物仿制药,适用于Herceptin的全部适应症,包括:早期乳腺癌、转移性乳腺癌、转移性胃癌。赫赛
首款赫赛汀生物类似药获批 用于治疗胃癌和乳腺癌
Mylan和Biocon公司今天宣布,美国FDA批准两家公司共同开发的Ogivri(trastuzumab-dkst)上市。Ogivri是一款赫赛汀(商品名Herceptin,药物名trastuzumab)的生物类似药(biosimilar),被批准用于治疗赫赛汀标签中的所有适应症,包括过度表达HER2的乳腺癌和转移性胃癌(胃或食管胃交界部腺癌)。这也是针对这两种特定癌症的第一款生物类似药。Ogi
辉瑞起诉告强生扼杀生物类似药竞争
在周三向宾州法院提出的诉讼中,辉瑞指出,强生“阻扰美国患者获得治疗选择,并损害了创新,对不断增长的生物制品市场中强大的价格竞争有害无益。”辉瑞在诉讼中称,强生故意打击其治疗类风湿关节炎的生物药,类克(Remicade)生物类似药的竞争对手,违反了反垄断法律和破坏“联邦生物制品价格竞争与创新法案(BPCIA)”的主要目标。据悉,强生与保险公司签订合同,要求患者在使用生物类似药的替代品之前
勃林格殷格翰阿达木单抗生物类似药CYLTEZO(R)获CHMP正面意见
欧洲药品管理局人用药品委员会(CHMP)对Cyltezo® (阿达木单抗生物类似药)用于多项慢性炎症疾病的治疗给予正面意见 这项推荐是基于Cyltezo® /BI 695501与修美乐®之间在大量的药学分析、药理学、非临床和临床数据上体现出的相似性而得出 在获得这项积极意见之前,Cyltezo®已获美国食品药品监督管理局批准上市1 德国殷格翰2017年9月22日电
生物类似药与原研药的相互替换性成焦点
在这周举行的RAPS监管大会上,生物类似药和生物原研药的相互替换性(interchangeable)成了监管当局和业界人士的聚焦热点。美国食品和药物管理局(FDA)最近发布的FDA关于互换性的行业准则草案,概述了生物类似药获得互换性所需的研究,包括使用切换研究(Switching Study),FDA治疗生物制剂办公室副主任Leah Christl在会上介绍了这个草案。她指出,首先,生
罗氏赫赛汀安维汀生物类似药获批
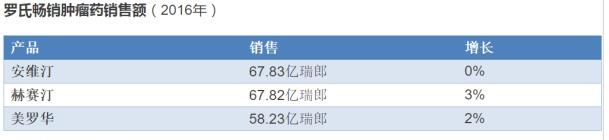
肿瘤药咨询委员会一致赞成,批准贝伐单抗和曲妥单抗的生物类似药。这个专家评审结果,将是生物类似药领域的里程碑。在周四举行的评审会议上,美国食品和药物管理局(FDA)的肿瘤药物咨询委员会(ODAC)投票,全票支持批准罗氏最畅销的癌症药物安维汀(贝伐单抗)和赫赛汀(曲妥单抗)两种生物仿制药。2016年全年的销售额来看,安维汀最多,为67.83亿瑞士法郎,约合70.11亿美元,赫赛汀紧随其后,67.82亿
生物类似药研发应用需保持谨慎稳健态度
在中国,生物类似药是指在质量、安全性和有效性方面与已获准注册的参照药具有相似性的治疗用生物制品。生物类似药的生产工艺和要求比化学仿制药难度高很多其制造商必须开发新的细胞系,独立重新制定整个制造过程。并需要对原研药相似的疗效和安全性进行验证。 近日在广州召开的“生物类似药专家顾问委员会”上,面对患者是否能用上越来越多价格低廉的“仿制“生物类以及这些药是否与原研药等效等问题,多位业内专家表示:生物类似
生物类似药进世卫目录
世界卫生组织将启动一项预认证试点,让在中低收入国家的患者能用上最昂贵的癌症疗法。世界卫生组织(WHO)周四表示,今年将开启一项预认证,Pre-Qualification试点,针对两种抗肿瘤的生物类似药。WHO计划在今年9月,邀请生物类似药生产药企,提交两种生物制品的生物仿制药生产资格:一个是利妥昔单抗, 主要治疗非霍奇金淋巴瘤和慢性淋巴细胞性白血病, 另一个是曲妥珠单抗,用于治疗乳腺癌。利妥昔和曲
生物制剂和生物类似药的非专利名称:FDA指南最终定稿
与WHO和欧洲命名生物制剂不同,美国FDA在上周四敲定了期待已久的指南文件,关于如何为生物类似药和生物参考对照产品命名,名称应包括附在非专利名称末尾的四个字母的FDA指定后缀。本指南的完稿过程不仅有数次反复(