ESC 2019:诺华Entresto治疗射血分数保留心力衰竭(HFpEF)在亚组中显示更大临床受益!
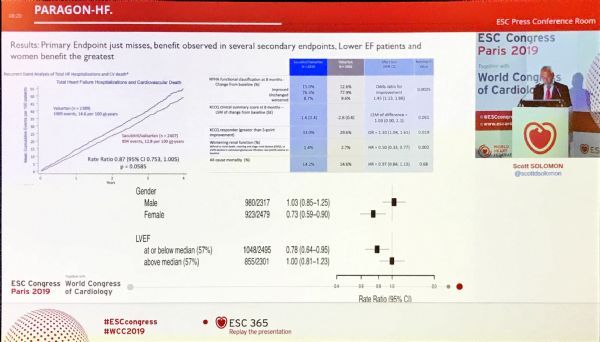
2019年09月02日讯 /生物谷BIOON/ --瑞士制药巨头诺华(Novartis)近日公布了心衰药物Entresto(中文商品名:诺欣妥,sacubitril/valsartan)全球性III期临床研究PARAGON-HF的全部结果。该研究在射血分数保留的心力衰竭(HFpEF)患者中开展,评估了Entresto相对于缬沙坦(valsartan)的疗效和安全性。结果显示,与缬沙坦相比,Entr
福泰制药$9.5亿收购Semma,开发干细胞衍生胰岛β细胞移植疗法
2019年09月04日讯 /生物谷BIOON/ --福泰制药(Vertex)是囊性纤维化(CF)治疗领域的全球领导者。近日,该公司宣布已签订一项最终协议,将以9.5亿美元收购Semma Therapeutics,这是一家私营生物技术公司,开创性地使用干细胞衍生的人类胰岛作为治疗1型糖尿病(T1D)的潜在治愈性疗法。根据收购条款,Vertex将以9.5亿美元现金收购Semma公司所有已发行股本,Se
诺华每月一次ofatumumab头对头III期临床疗效击败赛诺菲口服药Aubagio!
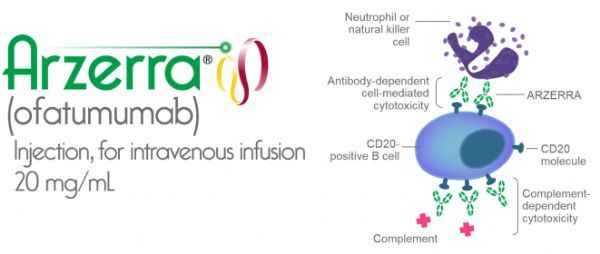
2019年08月31日讯 /生物谷BIOON/ --瑞士制药巨头诺华(Novartis)近日公布了ofatumumab(OMB157)治疗多发性硬化症的2项III期临床研究(0ASCLEPIOS I,II)的积极结果。这2项研究均为头对头(head-to-head,H2H),在复发型多发性硬化症(RMS)患者中开展,评估了每月一次皮下注射20mg剂量ofatumumab与口服药物每日一次口服Aub
紧追诺华Cosentyx!礼来新型抗炎药Taltz获美国FDA批准第三个适应症,治疗强直性脊柱炎(AS)
2019年08月27日讯 /生物谷BIOON/ --制药巨头礼来(Eli Lilly)近日宣布,美国食品和药物管理局(FDA)已批准抗炎药Taltz(ixekizumab)80mg/mL注射液,用于活动性强直性脊柱炎(AS,也称为放射性中轴型脊柱关节炎[r-axSpA])成人患者的治疗。值得一提的是,此次批准也标志着Taltz在美国监管方面获准的第三个适应症,该药于2016年3月首次获批,用于治疗
安进/艾尔建利妥昔单抗生物仿制药疗效对比研究成功
当地时间8月22日,安进与艾尔建公布了利妥昔单抗生物仿制药ABP798疗效比较研究JASMINE(NCT02747043)的积极顶线结果。这是一项随机、双盲、比较研究,评估了ABP798与罗氏美罗华(Rituxan)治疗CD20阳性B细胞非霍奇金淋巴瘤患者的疗效、安全性和免疫原性。研究共入组了256例成人患者,这些患者随机分为两组,分别接受ABP798和美罗华治疗,剂量为375mg/m
预防偏头痛 诺华重量级新药在中国获批临床
8月1日,中国国家药监局药品审评中心最新公告,由诺华(中国)生物医学研究公司递交用于预防成人偏头痛的erenumab注射液获得临床试验默示许可。Erenumab是FDA批准的第一个预防性偏头痛治疗药物,由诺华(Novartis)和安进(Amgen)联合开发,去年5月在美国获批上市,通过阻断降钙素基因相关肽(CGRP,一种参与偏头痛发作的分子)的活性发挥作用。该药曾入选科睿唯安出品的《2018最值得
“4+7”带量采购政策下的中国仿制药创新之路
2018年国家出台的“4+7”带量采购政策无疑是中国医药界的一场地震。其影响力之大,远超想象。“4+7”集采的实施,不仅显着降低中标药品价格,大幅减少药品流通费用,压缩药企的盈利空间,还将从根本上改变医院以药养医的局面,影响医疗和医药行业人才的培育和走向,改善医患关系,进而推动医药产业回归本质:由销售为王,逐渐转向以创新、质量和成本为核心竞争力。药采新政下,中国仿制药企业如
梅斯医访谈 | 对话绿叶制药集团副总裁姜华:任重道远,25年国际创新路
住友制药Latuda(盐酸鲁拉西酮)在日申请上市,今年1月获中国批准
2019年08月07日讯 /生物谷BIOON/ --住友制药(Sumitomo Dainippon Pharma)近日宣布,已在日本提交非典型抗精神病药物lurasidone HCl(盐酸鲁拉西酮片,英文商品名:Latuda,中文商品名:罗舒达®)的一份新药申请,寻求批准在日本生产和销售该药,用于治疗精神分裂症和双相抑郁症。lurasidone(鲁拉西酮)是一种非典型抗精神病药物,由住友
太阳制药银屑病新药tildrakizumab在日本申请上市
2019年08月02日讯 /生物谷BIOON/ --印度药企太阳制药(Sun Pharma)近日宣布,其全资子公司已向日本药品和医疗器械管理局(PMDA)提交了抗炎新药tildrakizumab治疗中度至重度银屑病和银屑病关节炎的生产和营销许可申请。日本是一个关键的医药市场,目前约有43万人患有银屑病和银屑病关节炎。tildrakizumab用药方案为:在第0、4周分别进行一次皮下注射100mg,