总局通报:20批药品不合格
元旦假期回来,不合格药品通报天天有,其中还不乏大企业、大品种,可见,新年伊始,药监严查力度再度升级。▍20批药品被查不合格1月5日,国家食药监总局发布《关于20批次药品不合格的通告(2018年第5号)》,标示为江西永升生化制药有限责任公司等12家企业生产的20批次药品不合格。根据通告,不合格项目包括装量、含量测定、水分、微生物限度等,对于不合格药品已采取查封扣押等控制措施,要求企业暂停销售使用、召
食药监总局关于发布动物源性医疗器械注册技术审查指导原则
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了《动物源性医疗器械注册技术审查指导原则(2017年修订版)》(见附件),现予发布。特此通告。附件:动物源性医疗器械注册技术审查指导原则(2017年修订版)附件动物源性医疗器械注册技术审查指导原则(2017年修订版)本指导原则旨在指导注册申请人对动物源性医疗器械的注册申报资料进行准备。某些医疗器械可能含
52个药品主动申请暂停销售
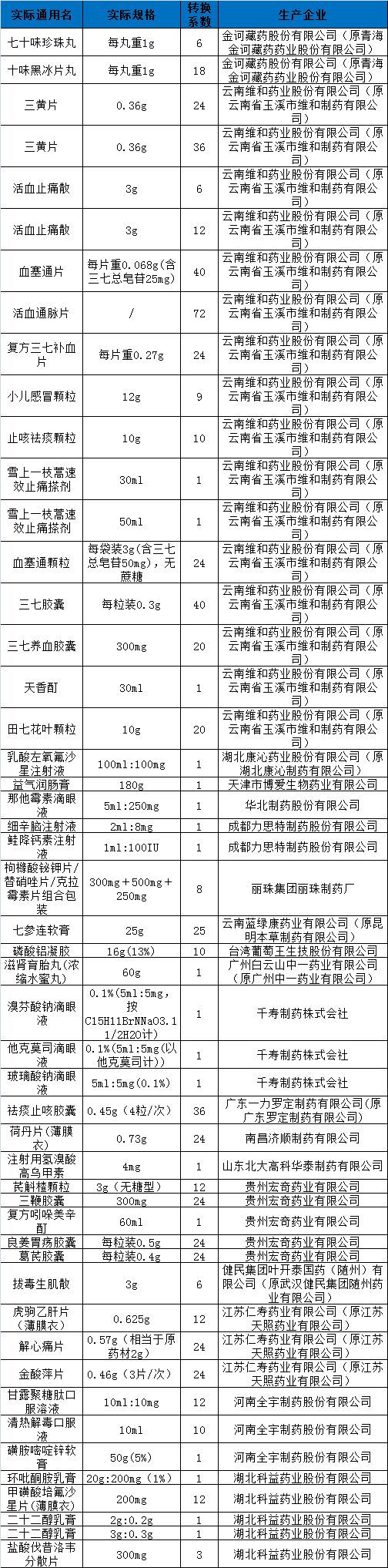
元旦假期回来,又有52个药品主动申请暂停销售,不玩了!▍湖北:50药品撤销挂网昨日(1月3日),湖北省药械集中采购服务平台发布《企业申请撤销挂网信息公示》,包括血塞通片、小儿感冒颗粒、乳酸左氧氟沙星注射液等50个药品,均是企业主动申请撤销挂网。从撤销挂网的名单,我们可以发现,很多都是廉价药、低价药。具体如下:▍云南:2品规不能供应1月2日,云南省药品集中采购平台发布《关于非基本药物暂停交易资格》,
各大省市发文按病种付费 药品营销即将颠覆
在医药代表备案制的喧嚣下,一项十分重要的政策悄然在四川、湖南、黑龙江、海南、武汉、济南等省市落地。2018年多地公立医院已开始实行按病种付费。所谓按病种收费标准,即患者入院,按病种治疗管理流程接受规范诊疗最终达到临床疗效标准出院,整个过程所发生的诊断、治疗、检验、检查、手术、麻醉、床位、护理、药品、医用耗材等各项费用,以及医疗机构要求或者推荐患者外购并在医院使用的药品、医用耗材等费用,不包括患者在
食药监总局公开征求《药品检查办法(征求意见稿)》意见
为进一步规范药品检查行为,保证检查质量,根据《中华人民共和国药品管理法》和《中华人民共和国药品管理法实施条例》及有关规定,食品药品监管总局组织起草了《药品检查办法》,现向社会公开征求意见。请于2018年1月29日前,将意见反馈至食品药品监管总局药化监管司。电子邮箱:yhjgs@CFDA.gov.cn附件:1.药品检查办法(征求意见稿)2.反馈意见表附件1药品检查办法(征求意见稿)第一章
食药监总局举行医疗器械网络销售监督管理办法新闻通气会
1月10日,国家食品药品监管总局举行新闻通气会,总局医疗器械监管司相关负责人就总局最新公布的《医疗器械网络销售监督管理办法》(第38号总局令,以下简称《办法》)的主要内容、医疗器械网络经营的监管形势,进行解读和分析。相关负责人介绍,随着医疗器械网络销售的飞速发展,利用网络非法销售未经注册的医疗器械、虚假夸大宣传、欺骗消费者的问题不断出现。例如,在网络电商平台、直营网站或移动客户端非法销售未经注册的
全国17万个药品文号,医院在卖的也就2万多个……
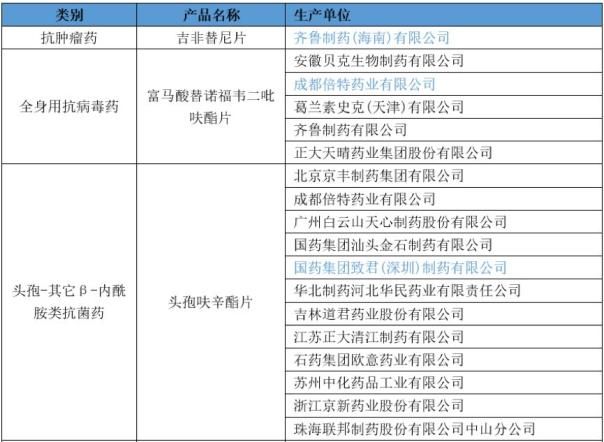
第一批通过一致性评价的17个药品清单公布之后,朋友圈一片欢欣鼓舞。不知道大家有没有注意到这么一个数据:通过一致性评价的17个药品中,只有4个在289品种清之列。也就是说,在距离2018年底大限还剩不到1年的时候,289品种的17740个药品文号只有0.023%确定通过了一致性评价。如果把数据再放大一些,全国现有药品文号约17万个(国产+进口),已经被《中国上市药品目录集》收录的只有203个,这个比
数百亿药品市场将重构 这些外企危险了
CFDA国家总局日前发布《总局关于发布通过仿制药质量和疗效一致性评价药品的公告(第一批)(2017年第173号)》,公布了12个通用名、17个品规的仿制药通过了一致性评价。至此,关于“仿制药一致性”评价的工作进入了一个新的阶段。▍通过品种大部分原研厂家销售辉煌一时根据笔者检索,12个通用名品种涉及的同剂型原研厂家有9个品种的自2005年以来全球销售数据资料,大多数品种的峰值出现在2010年及以前。
总局发布鼓励药品创新实行优先审评审批的意见 7类药品优先
刚刚,食品药品监管总局发布了《关于鼓励药品创新实行优先审评审批的意见》,对优先审评审批的范围、程序和要求给出了明确说明。此外,通知在优先审评审批的范围部分明确提出,防治下列7类疾病且具有明显临床优势的药品注册申请优先:1.艾滋病;2.肺结核;3.病毒性肝炎;4.罕见病;5.恶性肿瘤;6.儿童用药品;7.老年人特有和多发的疾病。附公告原文:总局关于鼓励药品创新实行优先审评审批的意见食药监药化管〔20
《生物制品批签发管理办法》发布
《生物制品批签发管理办法》已于2017年12月20日经国家食品药品监督管理总局局务会议审议通过,现予公布,自2018年2月1日起施行。局长:毕井泉2017年12月29日生物制品批签发管理办法第一章 总 则第一条 为加强生物制品监督管理,规范生物制品批签发行为,保证生物制品安全、有效,根据《中华人民共和国药品管理法》(以下简称《药品管理法》)有关规定,制定本办法。第二条 本办