拜耳子宫内膜异位症新药Visanne(地诺孕素)获中国批准
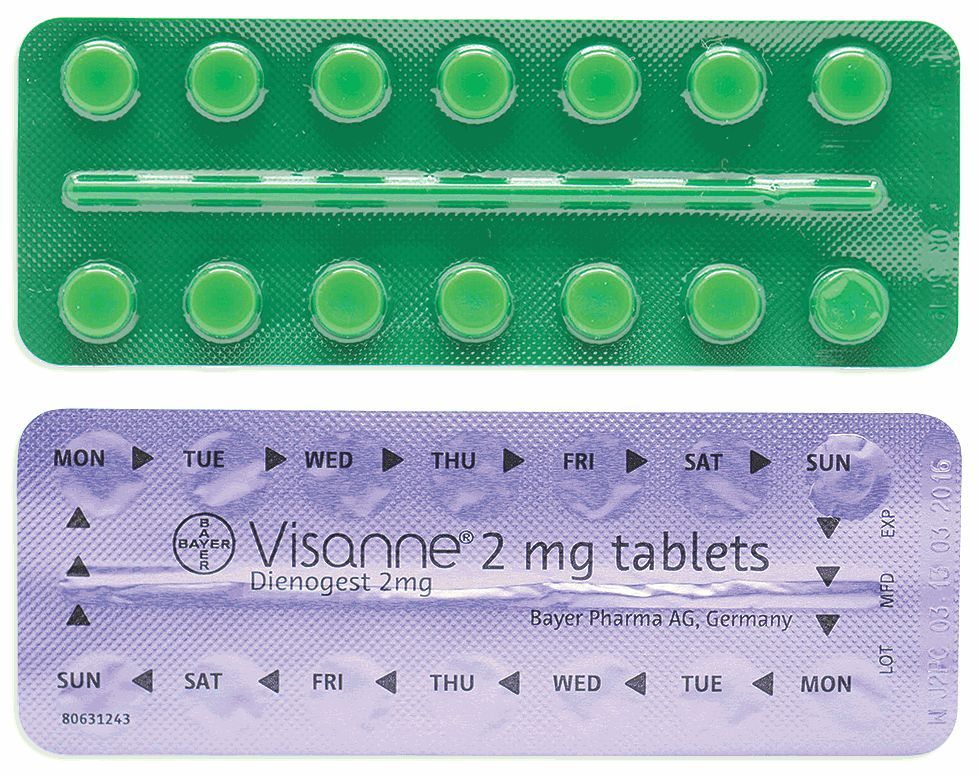
2018年12月22日讯 /生物谷BIOON/ --德国制药巨头拜耳(Bayer)近日宣布,妇科新药Visanne(dienogest)已获中国监管部门批准用于治疗子宫内膜异位症(EMs)。Visanne是每日一次的口服片剂,含有2mg地诺孕素(dienogest),专门用于治疗EMs这种慢性妇科疾病。Visanne是一款新型选择性孕激素受体激动剂,能抑制卵巢机能及子宫内膜细胞的增殖,从而减轻EM
罕见病新药!美国FDA批准首个长效C5补体抑制剂Ultomiris,治疗阵发性睡眠性血红蛋白尿症(PNH)
2018年12月24日讯 /生物谷BIOON/ --Alexion是一家致力于罕见病新药研发的美国制药公司。近日,该公司宣布,美国食品和药物管理局(FDA)已批准Ultomiris(ravulizumab-cwvz),该药是第一种也是唯一一种每8周给药一次的长效C5补体抑制剂,用于治疗阵发性睡眠性血红蛋白尿症(PNH)成人患者。Ultomiris今年6月,Alexion在向FDA递交Ultomir
口服多发性硬化症新药!百健向美国FDA提交Vumerity上市申请,打造升级版Tecfidera!
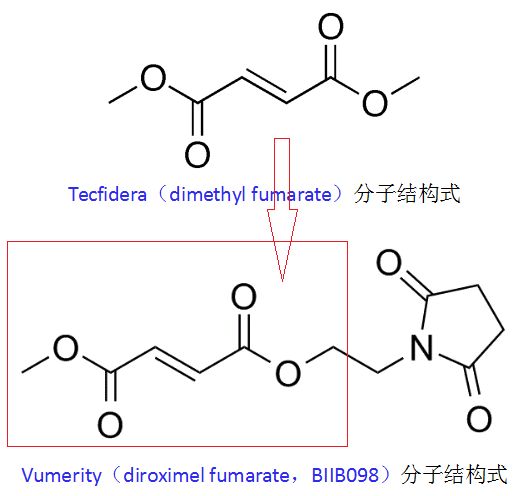
2018年12月19日/生物谷BIOON/--百健(Biogen)与合作伙伴Alkermes近日联合宣布,双方已向美国食品和药物管理局(FDA)提交了diroximel fumarate(BIIB098)的新药申请(NDA),该药是一种新型口服富马酸药物,开发用于复发型多发性硬化症(RMS)的治疗。BIIB098由Alkermes研制,已授权给百健,该药属于免疫抑制剂,每日口服2次,属于控释剂型的
脊髓性肌萎缩症(SMA)新药!罗氏口服药物risdiplam获欧盟优先药物资格(PRIME)
2018年12月18日/生物谷BIOON/--瑞士制药巨头罗氏(Roche)近日宣布,欧洲药品管理局(EMA)已授予risdiplam(RG7916)治疗脊髓性肌萎缩症(SMA)的优先药物资格(PRIME)。目前,罗氏正在开展3项全球性多中心III期临床研究(FIREFISH[NCT02913482]、SUNFISH[NCT02908685]、JEWELFISH[NCT03032172]),评估r
产后抑郁不怕啦!全球首个产后抑郁症药物Zulresso将于2019年6月上市!
2018年11月24日讯 /生物谷BIOON/ --Sage Therapeutics是一家临床阶段的生物制药公司,专注于开发创新药物用于中枢神经系统(CNS)疾病的治疗。近日,该公司宣布,美国食品和药物管理局(FDA)已将Zulresso(brexanolone注射液)治疗产后抑郁症(PPD)的审查时间延长了3个月,其处方药用户收费法(PDUFA)目标日期由之前的2018年12月19日延长至20
升血小板新药!安进Nplate获美国FDA批准,用于免疫性血小板减少症(ITP)儿科患者
2018年12月16日讯 /生物谷BIOON/ --生物技术巨头安进(Amgen)近日宣布,美国食品和药物管理局(FDA)已批准Nplate(romiplostim)的补充生物制品许可申请(sBLA),用于免疫性血小板减少症(ITP)持续至少6个月并且对皮质类固醇、免疫球蛋白或脾切除术应答不足的1岁及以上儿科患者。之前,FDA已授予该sBLA优先审查资格。ITP儿科患者因血小板计数低,存在严重出血
相比抗抑郁药物 锻炼和饮食等天然疗法也能有效改善抑郁症患者的症状
2018年11月27日 讯 /生物谷BIOON/ --近年来,人群中抑郁症的发病状况正在不断恶化,在美国,因自杀的死亡人数远超于枪杀人数,而且美国各个州的自杀率都在上升,据美国CDC数据显示,从1999年以来,自杀死亡的人群数量增加了30%,而且目前加拿大也出现了类似的趋势。研究人员表示,这些发病率和死亡率的增长恰恰发生在抗抑郁药物使用激增的一段时间内(增加了65%),截止到2014年,12岁以上
多篇文章解读抑郁症领域重要研究成果!
据WHO数据显示,目前抑郁症是全球第四大疾病负担,也是导致患者功能残疾的主要原因之一,大约有1/7的人会在人生的某个阶段遭受抑郁症困扰。预计到2020年,抑郁症将成为仅次于心血管病的第二大疾病。而在中国,抑郁症的发病率约为6%,目前已确诊的抑郁症患者为3000万人左右。近年来,科学家们在抑郁症研究方面投入了大量精力,当然也取得了很多可喜的研究成果,本文中,小编就对相关研究成果进行整理,分享给大家!
产后抑郁症新药Zulresso获FDA批准上市
日前,Sage Therapeutics公司宣布,FDA咨询委员会以17:1的投票结果,推荐FDA批准该公司研发的用于治疗产后抑郁症(PPD)的Zulresso(brexanolone)上市。如果获得批准,这将是第一款针对PPD的获批药物。PPD是分娩之后最常见的医学并发症,据统计在美国每9名分娩妇女中就有一位受到PPD的困扰。每年大约有40万名女性受到这一并发症的影响。PPD的症状包
骨质疏松症新药!安进/优时比Evenity即将面临美国FDA专家委员会审查
2018年12月03日/生物谷BIOON/--美国生物技术巨头安进(Amgen)与合作伙伴优时比(UCB)近日联合宣布,美国食品和药物管理局(FDA)骨骼、生殖和泌尿药物咨询委员会(BRUDAC)已计划在2019年1月16日对Evenity(romosozumab)治疗存在骨折高风险的绝经后女性骨质疏松症的生物制品许可申请(BLA)进行审查。Evenity是一种全人源化单克隆抗体,通过抑制骨硬化蛋