美国FDA批准Qelbre(维洛沙嗪):10年来注意力缺陷多动障碍(ADHD)第一个非兴奋剂疗法!
Qelbree是一种5-羟色胺-去甲肾上腺素调节剂(SNMA),用于治疗6-17岁ADHD儿科患者。
加速批准 新药监管的新挑战
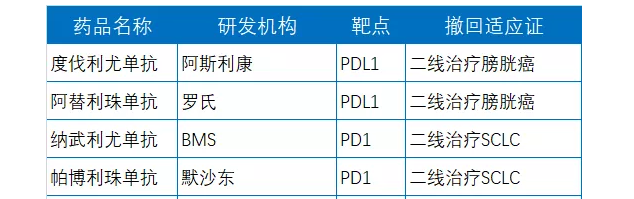
PD-1/L1药物的商业价值毋庸置疑,2020年全球市场规模已经接近300亿美元,默沙东Keytruda更是以143.8亿美元的销售收入位居畅销肿瘤药榜首,也是当前仅次于Humira的全球销售额第2高产品,有望接过“药王”的称号。然而2021年伊始,PD-1/L1领域却传来了不好的消息,K药、I药、T药分别撤回了之前被FDA加速批准的
美国FDA批准Vyxeos用于≥1岁儿科群体:治疗2种特定的急性髓性白血病(AML)
Vyxeos用于治疗年龄≥1岁、新诊断的、治疗相关性急性髓性白血病(t-AML)或伴骨髓增生异常相关改变的急性髓性白血病(AML-MRC)儿科患者。
首款复发性心包炎药物获FDA批准上市
Kiniksa公司宣布,美国食品和药物管理局(FDA)已批准该公司开发的重组融合蛋白ARCALYST (rilonacept) 上市,每周皮下注射1次,用于治疗12岁及以上儿童和成人患者复发性心包炎和降低心包炎复发风险。rilonacept是FDA批准的首个治疗复发性心包炎的药物。复发性心包炎是一种疼痛性自身炎症性心血管疾病,典型表现为胸痛,通常与心电传导改
FDA批准Zegalogue注射剂治疗严重低血糖症的糖尿病患者
日前,Zealand Pharma宣布,美国FDA已批准Zegalogue(dasiglucagon)注射剂用于治疗6岁及以上的小儿和成年糖尿病患者的严重低血糖症。FDA批准Zegalogue主要是基于在6至17岁儿童和成人1型糖尿病患者中进行的3项随机、双盲、安慰剂对照的多中心3期研究的功效结果。所有研究的主要疗效终点是血糖水平恢复
泰诺麦博TNM002单抗成功获美国FDA批准IND
3月16日,珠海泰诺麦博生物技术有限公司(Trinomab Biotechnology Co., Ltd.,简称“泰诺麦博”及“Trinomab”)宣布,其自主研发的重组抗破伤风毒素单抗药物TNM002的临床试验申请(IND)正式获得美国食品药品管理局(FDA)批准,这是继2020年11月获得澳洲HREC/TGA批准后的又一次临床申请